
| A、铝和氧化铁用镁带引燃 |
| B、氯气和氢气混合后与光发生爆炸 |
| C、工业上用焦炭制水煤气 |
| D、Ba(OH)2?8H2O晶体与NH4Cl晶体的反应 |


科目:高中化学 来源: 题型:
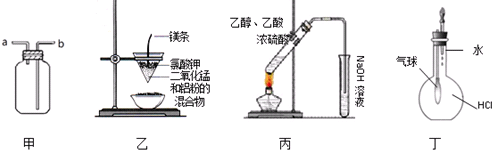
| A、装置甲:气体从a口进入,收集CO2 |
| B、装置乙:可制得金属锰 |
| C、装置丙:实验室制取乙酸乙酯 |
| D、装置丁:验证HCl气体在水中的溶解性 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、νA=2mol/L?min (正反应速率);νA=2mol/L?min(逆反应速率) |
| B、νA=2mol/L?min(正反应速率);νC=2mol/L?min(逆反应速率) |
| C、νA=1mol/L?min (正反应速率);νB=2mol/L?min(逆反应速率) |
| D、νA=1mol/L?min(正反应速率);νC=1.5mol/L?min(逆反应速率) |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com