
【题目】煤燃烧排放的烟气含有SO2和NOx,形成酸雨、污染大气,采用NaClO2溶液作为吸收剂可同时对烟气进行脱硫、脱硝,回答下列问题:
(1)在鼓泡反应器中通入含有含有SO2和NO的烟气,反应温度为323 K,NaClO2溶液浓度为5×103mol·L1。反应一段时间后溶液中离子浓度的分析结果如下表:
离子 | SO | SO | NO | NO | Cl |
c/(mol·L1) | 8.35×104 | 6.87×106 | 1.5×104 | 1.2×105 | 3.4×103 |
①写出NaClO2溶液脱硝过程中主要反应的离子方程式__________增加压强,NO的转化率__________(填“提高”“不变”或“降低”)。
②随着吸收反应的进行,吸收剂溶液的pH逐渐______________(填“增大”“不变”或“减小”)。
③由实验结果可知,脱硫反应速率__________脱硝反应速率(填“大于”或“小于”)。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是___________。
(2)在不同温度下,NaClO2溶液脱硫、脱硝的反 应中,在反应ClO![]() +2SO
+2SO![]() ==2SO
==2SO![]() +Cl的平衡常数K表达式为__________。
+Cl的平衡常数K表达式为__________。
(3)如果采用NaClO、Ca(ClO)2替代NaClO2,也能得到较好的烟气脱硫效果。已知下列反应:
SO2(g)+2OH(aq)==SO![]() (aq)+H2O(l)ΔH1
(aq)+H2O(l)ΔH1
ClO(aq)+SO![]() (aq)==SO
(aq)==SO![]() (aq)+Cl(aq)ΔH2
(aq)+Cl(aq)ΔH2
CaSO4(s)==Ca2+(aq)+SO![]() (aq)ΔH3
(aq)ΔH3
则反应SO2(g)+Ca2+(aq)+ClO(aq)+2OH(aq)==CaSO4(s)+H2O(l)+Cl(aq)的ΔH=____________。
【答案】(1)①4OH—+3ClO![]() +4NO=4NO
+4NO=4NO![]() +3Cl-+2H2O提高;②减小(2分);③大于(2分);NO溶解度较低或脱硝化反应的活化能较高(2分)
+3Cl-+2H2O提高;②减小(2分);③大于(2分);NO溶解度较低或脱硝化反应的活化能较高(2分)
(2)![]() (2分)(3)△H1+△H2-△H3(2分)
(2分)(3)△H1+△H2-△H3(2分)
【解析】
试题分析:(1)①亚氯酸钠具有氧化性,分析题给数据知NaClO2溶液脱硝过程中主要生产硝酸根和氯离子,利用化合价升降法结合原子守恒和电荷守恒配平,该反应的离子方程式为2OH-+3ClO2-+4NO==4NO3-+3Cl-+2H2O;该反应正反应是气体体积减小的,则增加压强,平衡正向移动,NO的转化率提高。
②根据反应的方程式2H2O+ClO2-+2SO2==2SO42-+Cl-+4H+、2H2O+3ClO2-+4NO==4NO3-+3Cl-+4H+可知随着吸收反应的进行氢离子浓度增大,吸收剂溶液的pH逐渐减小。
③由实验结果可知,在相同时间内硫酸根离子的浓度增加的多,因此脱硫反应速率大于脱硝反应速率。原因是除了SO2和NO在烟气中的初始浓度不同,还可能是NO溶解度较低或脱硝反应活化能较高或SO2的溶解度大于NO或二氧化硫的还原性强,易被氧化。
(2)化学平衡常数是在一定条件下,当可逆反应达到平衡状态时,生成物浓度的幂之积和反应物浓度的幂之积的比值,则根据反应ClO2+2SO32=2SO42+Cl写出反应的平衡常数K表达式为K=![]() 。
。
(3)已知:①.SO2(g)+2OH(aq)==SO32(aq)+H2O(l)ΔH1;
②.ClO(aq)+SO32(aq)==SO42(aq)+Cl(aq)ΔH2;
③.CaSO4(s)==Ca2+(aq)+SO42(aq)ΔH3
根据盖斯定律知①+②-③可得反应
SO2(g)+Ca2+(aq)+ClO(aq)+2OH(aq)=CaSO4(s)+H2O(l)+Cl(aq)的ΔH=△H1+△H2-△H3。


科目:高中化学 来源: 题型:
【题目】将 0.4mol/L AgNO3 溶液,0.3mol/L MgCl2 溶液和 0.2mol/L 的 AlCl3 溶液按 3:2:1 的体积相混合静置后, 上层清夜中 Cl-的浓度为(混合后溶液体积变化不计)
A. 0.2mol/L B. 0.1mol/L C. 0.6mol/L D. 0.3mol/L
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定条件下,某容器中各微粒在反应前后变化的示意图如下,其中![]() 和
和![]() 代表不同元素的原子。
代表不同元素的原子。

关于此反应说法错误的是( )
A. 一定属于吸热反应 B. 一定属于可逆反应
C. 一定属于氧化还原反应 D. 一定属于分解反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列条件下,两瓶气体所含分子数一定相等的是
A.同质量、不同密度的N2和CO B.同温度、同体积的H2和N2
C.同体积、同密度的O3和O2 D.同压强、同体积的N2O和CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Na2SO3应用广泛。利用工业废碱渣(主要成分Na2CO3)吸收硫酸厂尾气中的SO2制备无水Na2SO3的成本低,优势明显,其流程如下。
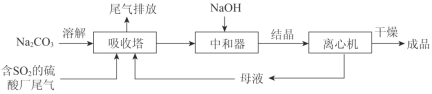
(1)举例说明向大气中排放SO2导致的环境问题:_________。
(2)下图为吸收塔中Na2CO3溶液与SO2反应过程中溶液组成变化。则初期反应(图中A点以前)的离子方程式是_________。
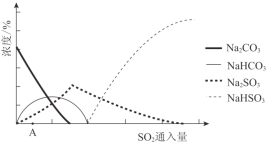
(3)中和器中发生的主要反应的化学方程式是_________。
资料显示: Ⅰ.Na2SO3在33℃时溶解度最大,将其饱和溶液加热至33℃以上时,由于溶解度降低会析出无水Na2SO3,冷却至33℃以下时析出Na2SO3·7H2O; Ⅱ.无水Na2SO3在空气中不易被氧化,Na2SO3·7H2O在空气中易被氧化。 |
(4)为了降低由中和器所得溶液中Na2SO3的溶解度,从而提高结晶产率,中和器中加入的NaOH是过量的。
①请结合Na2SO3的溶解平衡解释NaOH过量的原因_________。
②结晶时应选择的最佳操作是_________(选填字母)。
A.95~100℃加热蒸发,直至蒸干
B.维持95~100℃蒸发浓缩至有大量晶体析出
C.95~100℃加热浓缩,冷却至室温结晶
(5)为检验Na2SO3成品中是否含少量Na2SO4,需选用的试剂是_________、_________。
(6)KIO3滴定法可测定成品中Na2SO3的含量:室温下将0.1260g 成品溶于水并加入淀粉做指示剂,再用酸性KIO3标准溶液(x mol/L)进行滴定至溶液恰好由无色变为蓝色,消耗KIO3标准溶液体积为y mL。
①滴定终点前反应的离子方程式是:![]() IO3-+
IO3-+![]() SO32- =
SO32- =![]() _______ +
_______ +![]() _______(将方程式补充完整)。
_______(将方程式补充完整)。
②成品中Na2SO3(M = 126 g/mol)的质量分数是_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在25℃、1.01×105Pa下,将22gCO2通入到750mL1.0mol/L的NaOH溶液中充分反应,放出xkJ热量。已知该条件下,1mol CO2通入到2L1.0mol/LNaOH溶液中充分反应,放出y kJ的热量.则CO2与NaOH溶液反应生成NaHCO3的热化学方程式正确为
A. CO2(g)+NaOH(aq)=NaHCO3(aq)△H=-(2y-x)kJ/mol
B. CO2(g)+NaOH(aq)=NaHCO3(aq)△H=-(4x-y)kJ/mol
C. CO2(g)+NaOH(aq)=NaHCO3(aq)△H=-(2x-y)kJ/mol
D. CO2(g)+NaOH(aq)=2NaHCO3(aq)△H=-(8x-2y)kJ/mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】
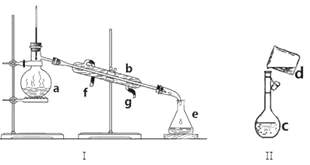
(1)写出下列仪器的名称:
a. b. c. e.
(2)若利用装置I分离四氯化碳和酒精的混合物,还缺少的仪器是 。冷凝水由 (填f或g)口通入。
(3)现需配制0.1mol/LNaOH溶液450mL,装置II是某同学转移溶液的示意图。
①图中的错误是 。
②根据计算得知,用托盘天平所需称量NaOH的质量为 g。
③配制时,其正确的操作顺序是(用字母表示,每个字母只能用一次)________。
A.用30mL水洗涤烧杯2-3次,洗涤液均注入容量瓶 |
B.称量计算出的氢氧化钠固体于烧杯中,再加入少量水(约30mL),用玻璃棒慢慢搅动,使其充分溶解并冷却至室温 |
C.将溶解的氢氧化钠溶液沿玻璃棒注入500mL的容量瓶中 |
D.将容量瓶盖紧,振荡,摇匀 |
E.改用胶头滴管加水,使溶液凹面恰好与刻度相切
F.继续往容量瓶内小心加水,直到液面接近刻度2~3cm处
(4)物质的量浓度误差分析:(填偏高、偏低、无影响)
①用滤纸称量氢氧化钠 ;
②定容时,若眼睛俯视刻度线,则所配制的溶液浓度将 ;
③未冷却到室温就注入容量瓶定容 ;
④配好的溶液转入干净的试剂瓶时,不慎溅出部分溶液 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,将1.000mol/L盐酸滴入20.00mL1.000mol/L氨水中,溶液pH和温度随加入盐酸体积变化曲线如下图所示。下列有关说法正确的是

A.a点由水电离出的c(H+)=1.0×10-14mol/L
B.b点时c(NH4+)+c(NH3·H2O)=c(Cl-)
C.c点时消耗的盐酸体积:V(HCl)<20.00mL
D.d点后,溶液温度略下降的主要原因是NH3·H2O电离吸热
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图是甲、乙、丙三种不同物质(不含结晶水)的溶解度曲线图。下列有关叙述正确的是()
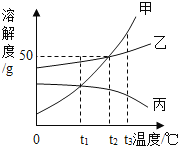
A. t1℃时,分别取出相同质量的甲、丙两种饱和溶液升温到t2℃时,甲和乙溶质的质量分数相等
B. t2℃时,将甲、乙两种饱和溶液分别恒温蒸发等质量的水,析出晶体的质量可能不等
C. 将三种饱和溶液分别从t3℃降低到t2℃时,甲和乙溶质的质量分数减小,丙的溶质的质量分数不变
D. 当甲的饱和溶液中含有少量乙时,可以采取冷却热饱和溶液的办法提取乙
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com