
【题目】为测定CuSO4溶液的浓度,甲、乙两同学设计了两个方案。回答下列问题:
Ⅰ.甲方案
实验原理:![]()
实验步骤:
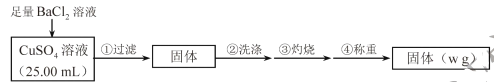
(1)判断![]() 沉淀完全的操作为____________。
沉淀完全的操作为____________。
(2)步骤②判断沉淀是否洗净所选用的试剂为_____________。
(3)步骤③灼烧时盛装样品的仪器名称为__________。
(4)固体质量为wg,则c(CuSO4)=________molL-1。
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,则测得c(CuSO4)_________(填“偏高”、“偏低”或“无影响”)。
Ⅱ.乙方案
实验原理:![]() ,
,![]()
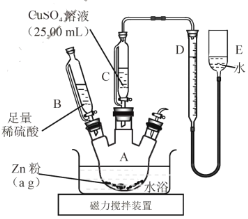
实验步骤:
①按右图安装装置(夹持仪器略去)
②……
③在仪器A、B、C、D、E…中加入图示的试剂
④调整D、E中两液面相平,使D中液面保持在0或略低于0刻度位置,读数并记录。
⑤将CuSO4溶液滴入A中搅拌,反应完成后,再滴加稀硫酸至体系不再有气体产生
⑥待体系恢复到室温,移动E管,保持D、E中两液面相平,读数并记录
⑦处理数据
(6)步骤②为___________。
(7)步骤⑥需保证体系恢复到室温的原因是________(填序号)。
a.反应热受温度影响 b.气体密度受温度影响 c.反应速率受温度影响
(8)Zn粉质量为ag,若测得H2体积为bmL,已知实验条件下![]() ,则c(CuSO4)______molL-1(列出计算表达式)。
,则c(CuSO4)______molL-1(列出计算表达式)。
(9)若步骤⑥E管液面高于D管,未调液面即读数,则测得c(CuSO4)________(填“偏高”、“偏低”或“无影响”)。
(10)是否能用同样的装置和方法测定MgSO4溶液的浓度:_________(填“是”或“否”)。
【答案】向上层清液中继续滴加BaCl2溶液,无白色沉淀生成,则沉淀完全 AgNO3溶液 坩埚 ![]() 偏低 检查装置气密性 b
偏低 检查装置气密性 b 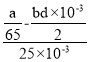 偏高 否
偏高 否
【解析】
甲方案是利用溶液中的硫酸铜与氯化钡反应生成硫酸钡沉淀,经灼烧、洗涤、称重后得到的固体是硫酸钡,利用硫酸根守恒,计算出硫酸铜的物质的量,从而计算出浓度;乙方案是利用锌与稀硫酸反应释放出氢气的体积,换算成质量,计算出与稀硫酸反应的锌的物质的量,再利用锌的总的物质的量减去与酸反应的锌的物质的量,得到与硫酸铜反应的锌的物质的量,根据锌和硫酸铜的物质的量关系,计算出硫酸铜的物质的量,根据![]() 得到硫酸铜的浓度,据此分析。
得到硫酸铜的浓度,据此分析。
Ⅰ.(1)硫酸根离子的检验是滴加氯化钡溶液,若产生白色沉淀,证明溶液中含有硫酸根离子,故判断![]() 沉淀完全的操作向上层清液中继续滴加BaCl2溶液,无白色沉淀生成,则沉淀完全;
沉淀完全的操作向上层清液中继续滴加BaCl2溶液,无白色沉淀生成,则沉淀完全;
(2)步骤②判断沉淀是否洗净所选用的试剂为AgNO3溶液,硫酸钡沉淀中可能附着有氯化钡,为了证明还有没氯离子,需要加入硝酸银溶液,若产生白色沉淀,证明没有洗净;
(3)步骤③灼烧时盛装样品的仪器为坩埚;
(4)固体质量为wg,为硫酸钡的质量,硫酸钡的物质的量为n=![]() ,根据硫酸根守恒可知,CuSO4~BaSO4,则c(CuSO4)=
,根据硫酸根守恒可知,CuSO4~BaSO4,则c(CuSO4)=![]() =
= =
=![]() molL-1;
molL-1;
(5)若步骤①从烧杯中转移沉淀时未洗涤烧杯,会使固体的质量偏小,物质的量偏小,根据![]() 可知,则测得c(CuSO4)偏低;
可知,则测得c(CuSO4)偏低;
Ⅱ.(6)加入药品之前需检查装置的气密性;步骤②为检查装置气密性;
(7)气体的体积受温度和压强的影响较大,气体的质量不随温度和压强的变化而改变,密度也受温度和压强的影响,步骤⑥需保证体系恢复到室温的原因是气体密度受温度影响;反应热不受温度的影响,只与反应物和生成物自身的能量有关,不随温度压强而改变;反应速率受温度影响,温度越高,反应速率越快,步骤⑥需保证体系恢复到室温与反应速率无关;
(8)Zn粉质量为ag,若测得H2体积为bmL,已知实验条件下![]() ,氢气的质量=
,氢气的质量=![]() ,利用氢气的质量得到氢气的物质的量n=
,利用氢气的质量得到氢气的物质的量n=![]() ,根据
,根据![]() ,与酸反应的锌的物质的量为
,与酸反应的锌的物质的量为![]() ,锌的总物质的量为
,锌的总物质的量为![]() ,与硫酸铜反应的锌的物质的量为
,与硫酸铜反应的锌的物质的量为![]() ,根据
,根据![]() ,则c(CuSO4)=
,则c(CuSO4)=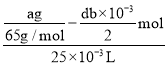 ;
;
(9)若步骤⑥E管液面高于D管,未调液面即读数,得到氢气的体积偏小,与硫酸反应的锌的质量偏小,与硫酸铜反应的锌的质量偏大,则测得c(CuSO4)偏高;
(10) 不能用同样的装置和方法测定MgSO4溶液的浓度,硫酸镁不和锌发生置换反应。


科目:高中化学 来源: 题型:
【题目】下图有机物的正确命名为 ( )

A.2-乙基-3,3-二甲基戊烷B.3,3-二甲基-4-乙基戊烷
C.3,3,4-三甲基己烷D.3,4,4-三甲基己烷
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某同学利用Cl2氧化K2MnO4制备KMnO4的装置如下图所示(夹持装置略):
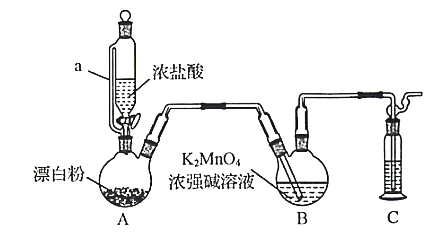
已知:锰酸钾(K2MnO4)在浓强碱溶液中可稳定存在,碱性减弱时易发生反应:
![]()
回答下列问题:
(1)装置A中a的作用是______________;装置C中的试剂为________________;装置A中制备Cl2的化学方程为______________。
(2)上述装置存在一处缺陷,会导致KMnO4产率降低,改进的方法是________________。
(3)KMnO4常作氧化还原滴定的氧化剂,滴定时应将KMnO4溶液加入___________(填“酸式”或“碱式”)滴定管中;在规格为50.00mL的滴定管中,若KMnO4溶液起始读数为15.00mL,此时滴定管中KMnO4溶液的实际体积为______________(填标号)。
A.15.00 mL B.35.00mL C.大于35.00mL D.小于15.00m1
(4)某FeC2O4﹒2H2O样品中可能含有的杂质为Fe2(C2O4)3、H2C2O4﹒2H2O,采用KMnO4滴定法测定该样品的组成,实验步骤如下:
Ⅰ.取mg样品于锥形瓶中,加入稀H2SO4溶解,水浴加热至75℃。用 c mol﹒L-1的KMnO4溶液趁热滴定至溶液出现粉红色且30s内不褪色,消耗KMnO4溶液V1mL。
Ⅱ.向上述溶液中加入适量还原剂将Fe3+完全还原为Fe2+,加入稀H2SO4酸化后,在75℃继续用KMnO4溶液滴定至溶液出现粉红色且30s内不褪色,又消耗KMnO4溶液V2mL。
样品中所含![]() 的质量分数表达式为_________________。
的质量分数表达式为_________________。
下列关于样品组成分析的说法,正确的是__________(填标号)。
A.![]() 时,样品中一定不含杂质
时,样品中一定不含杂质
B.![]() 越大,样品中
越大,样品中![]() 含量一定越高
含量一定越高
C.若步骤I中滴入KMnO4溶液不足,则测得样品中Fe元素含量偏低
D.若所用KMnO4溶液实际浓度偏低,则测得样品中Fe元素含量偏高
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将NO2、NH3、O2混合气22.4L通过稀硫酸后,溶液质量增加了26.7g,气体体积缩小为4.48L。(气体体积均在标况下测定)剩余气体能使带火星的木条着火,则混合气体的平均相对分子质量为(4NO2+O2+2H2O=4HNO3)
A.28.1B.30.2C.33.1D.34.0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】我国科学家研制出一种催化剂,能在室温下高效催化空气中甲醛的氧化,其反应为HCHO+O2![]() CO2+H2O。下列有关说法正确的是( )
CO2+H2O。下列有关说法正确的是( )
A.反应物和生成物都是非极性分子
B.0.5 mol HCHO含有1 mol σ键
C.HCHO、CO2分子中中心原子杂化类型相同
D.HCHO能溶解在H2O中
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】天然产物H具有抗肿瘤、镇痉等生物活性,可通过以下路线合成。

已知: (
(![]() 等)
等)
回答下列问题:
(1)A的链状同分异构体可发生银镜反应,写出这些同分异构体所有可能的结构:__________。
(2)在核磁共振氢谱中,化合物B有________组吸收峰。
(3)化合物X的结构简式为___________。
(4)D→E的反应类型为___________。
(5)F的分子式为_______,G所含官能团的名称为___________。
(6)化合物H含有手性碳原子的数目为_____,下列物质不能与H发生反应的是_______(填序号)。
a.CHCl3 b.NaOH溶液 c.酸性KMnO4溶液 d.金属Na
(7)以 和
和![]() 为原料,合成
为原料,合成![]() ,写出路线流程图(无机试剂和不超过2个碳的有机试剂任选)_______________。
,写出路线流程图(无机试剂和不超过2个碳的有机试剂任选)_______________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图所示分别为氯化钠、氯化铯、氟化钙的晶胞模型,请认真观察后完成表格。___________
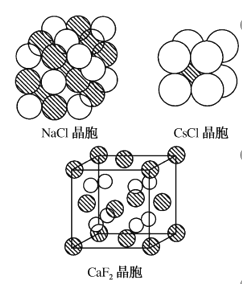
离子晶体 | 晶体结构粒子 | 晶胞所含粒子数 | 配位数 | 阴阳离子个数之比 | ||
阴离子 | 阳离子 | 阴离子 | 阳离子 | |||
氯化钠 | ||||||
氯化铯 | ||||||
氟化钙 | ||||||
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】红热的炭与浓硫酸可发生反应。
(1)写出该化学反应方程式;并用“双线桥”标出该反应中电子的转移的方向和数目___。
(2)现欲设计一个实验以验证此反应所生成的各种产物。实验中可供使用的试剂有:浓硫酸、稀硫酸、澄清石灰水、NaOH溶液、品红溶液、酸性高锰酸钾溶液、无水硫酸铜固体和碱石灰。有一个同学按气体的流动方向设计了一个实验过程,其所使用的试剂次序可表示为:气体产物→试剂Ⅰ→试剂Ⅱ→试剂Ⅲ→试剂Ⅱ→试剂Ⅳ
①试剂Ⅰ、Ⅱ、Ⅲ、Ⅳ分别为___,___,___,___;
②说出试剂Ⅱ使用两次的作用分别是___,___;
③写出气体产物通过试剂Ⅳ时的离子方程式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】中草药秦皮中含有的七叶树内酯(每个折点表示一个碳原子,氢原子未画出),具有抗菌作用。若1 mol七叶树内酯分别与浓溴水和NaOH溶液完全反应,则消耗的Br2和NaOH的物质的量分别为( )

A.2mol Br2、3mol NaOH B.3mol Br2、3mol NaOH
C.3mol Br2、4mol NaOHD.4mol Br2、4mol NaOH
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com