
| A�� | ���¶��£�a��ʱ��3 v����CO2��=v����H2�� | |
| B�� | ���ߢ��Ӧ�������ı�����dz��뺤�� | |
| C�� | ���ߢ��Ӧ�������ı�����ǽ����¶� | |
| D�� | �ӷ�Ӧ��ʼ��a�㣬v ��CO2��=0.6 mol•L-1•min-1 |
���� A������֮�ȵ��ڻ�ѧ������֮�ȣ�
B�����º����³��뺤������Ӧ���������Ũ�Ȳ��䣬ƽ�ⲻ�ƶ���
C�������¶ȣ���Ӧ���ʼ���������ӦΪ���ȷ�Ӧ��ƽ�������ƶ���
D������v=$\frac{��c}{��t}$����v��H2�����ٸ�������֮�ȵ��ڻ�ѧ������֮�ȼ���v��CO2����
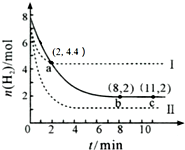
��� �⣺A������֮�ȵ��ڻ�ѧ������֮�ȣ��ʸ��¶��£�a��ʱ3 v����CO2��=v����H2������A��ȷ��
B�����º����³��뺤������Ӧ���������Ũ�Ȳ��䣬ƽ�ⲻ�ƶ��������ߢ����ʼӿ죬�����������٣�ƽ�������ƶ�����B����
C�������¶ȣ���Ӧ���ʼ���������ӦΪ���ȷ�Ӧ��ƽ�������ƶ������������ʵ�����С�������ߢ�ƽ���ʱ�����̣���Ӧ���ʼӿ죬ƽ��ʱ���������ʵ�������ƽ�����淴Ӧ�ƶ�������Ӧ���ȷ�Ӧ��˵���������¶ȣ���C����
D����ͼ��֪��a�����������ʵ���Ϊ4.4mol���μӷ�Ӧ�����������ʵ���Ϊ8mol-4.4mol=3.6mol��������Ũ�ȱ仯��Ϊ$\frac{3.6mol}{2L}$=1.8mol/L����v��H2��=$\frac{1.8mol/L}{2min}$=0.9mol•L-1•min-1������֮�ȵ��ڻ�ѧ������֮�ȣ���v��CO2��=$\frac{1}{3}$v��H2��=0.3mol•L-1•min-1����D����
��ѡ��A��
���� ���⿼�黯ѧƽ�������Ӱ�����ء���Ӧ���ʼ��㡢���ʵ���Ũ����ʱ��仯���ߵȣ��Ѷ��еȣ������ڻ���֪ʶ�Ĺ��̣�


 ��ְٷְټ���ϵ�д�
��ְٷְټ���ϵ�д� �����ƻ���ĩ��̶�100��ϵ�д�
�����ƻ���ĩ��̶�100��ϵ�д� �ܿ���ȫ��100��ϵ�д�
�ܿ���ȫ��100��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
 ij����С������ͼ��ʾװ����ȡ��ˮ������ʢ�б�����ˮ���ձ��м���̼��ƣ�����ߴ������Ũ�ȣ�ͼ�з�Һ©��A��ʢŨ���ᣬB�Ƕ������̣���
ij����С������ͼ��ʾװ����ȡ��ˮ������ʢ�б�����ˮ���ձ��м���̼��ƣ�����ߴ������Ũ�ȣ�ͼ�з�Һ©��A��ʢŨ���ᣬB�Ƕ������̣����鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
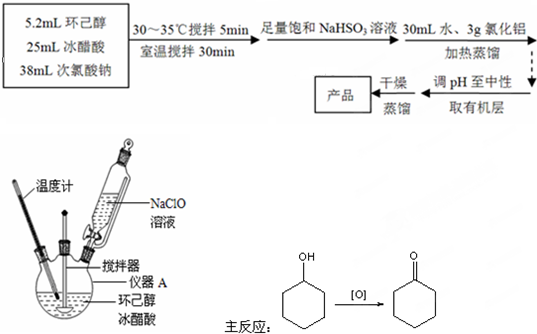
 ij�о���ѧϰС��Ϊ�ϳ�1-�������������ϵ�֪һ���ϳ�·�ߣ�
ij�о���ѧϰС��Ϊ�ϳ�1-�������������ϵ�֪һ���ϳ�·�ߣ��鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
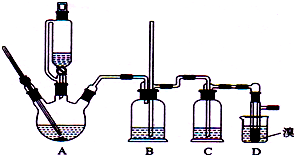 ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�
ʵ�����Ʊ�1��2-��������ķ�Ӧԭ�����£�| �Ҵ� | 1��2-�������� | ���� | |
| ״̬ | ��ɫҺ�� | ��ɫҺ�� | ��ɫҺ�� |
| �ܶ�/g•cm-3 | 0.79 | 2.2 | 0.71 |
| �е�/�� | 78.5 | 132 | 34.6 |
| �۵�/�� | һl30 | 9 | -1l6 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 0-10min�ڣ���A��ʾ��ƽ����Ӧ������0.05mol•L-1•min-1 | |
| B�� | 0-10min�ڣ���B��ʾ��ƽ����Ӧ������0.01mol•L-1•min-1 | |
| C�� | �ֱ���B��C��D��ʾ��Ӧ�����ʣ����ֵ��4��3��1 | |
| D�� | ���ŷ�Ӧ�Ľ��У�����������ѹǿʼ�ձ��ֲ��� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
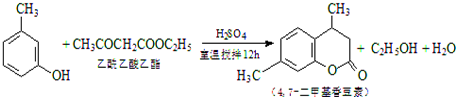
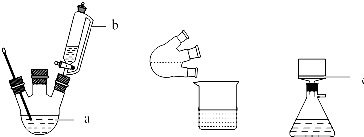
 CH3COOCH2CH3+H2O���ñ��͵�̼������Һ����ҩƷ���ƣ��ռ��ֲ�Ʒ���÷�Һ����������ƣ��ķ����Ѵֲ�Ʒ���룮
CH3COOCH2CH3+H2O���ñ��͵�̼������Һ����ҩƷ���ƣ��ռ��ֲ�Ʒ���÷�Һ����������ƣ��ķ����Ѵֲ�Ʒ���룮�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ȡһ�������壬�ܽ⣬����Һ��ͨ��������CO2���۲쵽�о���������˵��ԭ������һ������Na2CO3 | |
| B�� | ȡһ�������壬�ܽ⣬����Һ�м�������CaO��ĩ����ַ�Ӧ��۲쵽�а�ɫ�������ɣ�˵��ԭ������һ������Na2CO3 | |
| C�� | ȡһ�������壬�ܽ⣬����Һ�еμ�����AgNO3��Һ���۲쵽�а�ɫ�������ɣ�˵��ԭ������һ������NaCl | |
| D�� | ��ȡ3.80g���壬���������أ�����������0.620g��������ϡ�����ܽ�������壬��ַ�Ӧ���ռ���0.880g���壬˵��ԭ�����н�����Na2CO3��NaHCO3 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | CH2=CH2 | B�� | CH3CH=CH2 | C�� | CH3CH3 | D�� | CH3CH2CH=CH2 |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com