
下列事实一定能说明HF是弱酸的是
①常温下NaF溶液的pH大于7 ②用HF溶液做导电性实验,灯泡很暗
③HF与NaCl不能发生反应 ④常温下0.1mol/L的HF溶液的pH为2.3
⑤HF能与Na2CO3溶液反应,产生CO2气体 ⑥HF与水能以任意比混溶
⑦1mol/L的HF水溶液能使紫色石蕊试液变红
A.①②⑦ B.②③⑤ C.③④⑥ D.①④
D
【解析】
试题分析:①常温下NaF溶液的pH大于7,说明氟离子发生水解,使溶液呈碱性,则HF是弱酸,正确; ②用HF溶液做导电性实验,灯泡很暗,说明HF溶液中的离子浓度较小,但不能证明HF是弱酸,错误;
③HF与NaCl不能发生反应,不能证明HF是弱酸,错误;④常温下0.1mol/L的HF溶液的pH为2.3>1,说明HF未完全电离,说明HF是弱酸,正确;⑤HF能与Na2CO3溶液反应,产生CO2气体,说明HF比碳酸的酸性强,不能说明HF是弱酸,错误;⑥HF与水能以任意比混溶,溶解性与酸的强弱无关,错误;⑦1mol/L的HF水溶液能使紫色石蕊试液变红,说明HF的溶液显酸性,不能说明其为弱酸,错误,答案选D。
考点:考查弱酸的判断


科目:高中化学 来源:2014-2015江苏省高二上学期期末考试化学试卷(解析版) 题型:选择题
分子式为C7H16的烷烃中,含有3个甲基的同分异构体的数目是
A.2 B.3 C.4 D.5
查看答案和解析>>
科目:高中化学 来源:2014-2015江苏省宿迁市高二下学期学业水平模拟化学试卷(解析版) 题型:选择题
下列关于物质性质的描述错误的是
A.硝酸是易挥发的强酸
B.纯碱溶液能使酚酞溶液显红色
C.CO是无色难溶于水的气体
D.Fe3+可以与KSCN溶液反应生成血红色沉淀
查看答案和解析>>
科目:高中化学 来源:2014-2015学年四川省德阳市四校高三3月联合考试理综化学试卷(解析版) 题型:选择题
设NA为阿伏伽德罗常数的值,下列说法正确的是
A.1 mol [Cu(NH3)4]2+ 中含有σ键的数目为12NA
B.0.1mol铁粉与足量水蒸气反应生成的H2分子数目为0.1NA
C.分子数目为0.1NA的N2和NH3混合气体,原子间含有的共用电子对数目为0.3NA
D.用惰性电极电解CuSO4溶液一段时间后,若加入0.05mol的Cu2(OH)2CO3固体恰好能使溶液恢复到原来的浓度,则该电解过程中转移电子的数目为0.2NA
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三上学期期末考试化学B试卷(解析版) 题型:填空题
(10分,每空2分)A、B、C、D是四种短周期元素,它们的原子序数依次增大。其中A、D元素同主族且A是原子半径最小的元素,B、C元素同周期,B的最外层电子数是次外层电子数的2倍;由A、B、C、D中的两种元素可形成原子个数比为1:1的多种化合物,甲、乙、丙为其中的三种,它们的元素组成如下表所示:
化合物 | 甲 | 乙 | 丙 |
组成元素 | B、C | A、C | C、D |
常温下,甲物质为气体,密度略小于空气;乙物质为液体;丙物质为固体且为离子化合物。请填写下列空白:
(1)乙的化学式为 ,丙物质的化学式为 ,其中丙中阴离子与阳离子的个数之比为 。
(2)某同学设计了一个CH3OH燃料电池,并用该电池电解200mL一定浓度的NaCl与CuSO4的混合溶液,其装置如下图:

①写出ⅰ中通入甲醇这一极的电极反应式 。
②理论上ⅱ中两极所得气体的体积随时间变化的关系如坐标图所示(气体体积已换算成标准状况下的体积),写出在t1后,石墨电极上的电极反应式 。
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三上学期期末考试化学B试卷(解析版) 题型:选择题
下列描述正确的是
A.氯气、活性炭都能使品红溶液褪色,它们的漂白原理相同
B.滴加石蕊试液显红色的溶液:Fe3+、NH4+、I-可能大量共存
C.某溶液中加入盐酸酸化的氯化钡产生白色沉淀,原溶液中一定含有SO42-
D.Fe(NO3)2溶液中滴加少量稀硫酸会变黄色
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省菏泽市高三上学期期末考试化学B试卷(解析版) 题型:选择题
下列说法正确的是
A.在加碘食盐中,碘以单质形式存在
B.纳米材料是指一种称为“纳米”的新物质制成的材料
C.光导纤维是以二氧化硅为主要原料制成的
D.绿色食品是指不含任何化学物质的食品
查看答案和解析>>
科目:高中化学 来源:2014-2015学年山东省德州市高三2月期末统考化学试卷(解析版) 题型:选择题
仅用下表提供的玻璃仪器(非玻璃仪器和药品任选),不能实现相应实验目的的是
选项 | 实验目的 | 玻璃仪器 |
A. | 验证Na2CO3和NaHCO3的热稳定性 | 酒精灯、试管、导气管 |
B | 实验室用浓氨水和生石灰制备氨气 | 普通漏斗、烧杯、玻璃棒 |
C | 测定NaOH溶液浓度 | 滴定管、锥形瓶、烧杯 |
D | 分离乙醇和乙酸乙酯的混合物 | 分液漏斗、烧杯 |
查看答案和解析>>
科目:高中化学 来源:2014-2015学年湖北省仙桃天门潜江高三上学期期末联考理综化学试卷(解析版) 题型:实验题
(14分)4,7—二甲基香豆素(熔点:132.6℃)是一种重要的香料,广泛分布于植物界中,由间—甲苯酚为原料的合成反应如下: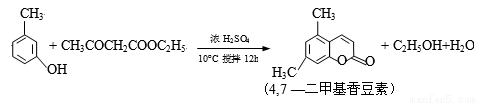
实验装置图如下:

主要实验步骤:
步骤1.向装置a中加入60mL浓硫酸,并冷却至0℃以下,搅拌下滴入间—甲苯酚30mL(0.29mol)和乙酰乙酸乙酯26.4mL (0.21mol)的混合物。
步骤2.保持在10℃下,搅拌12h,反应完全后,将其倒入冰水混合物中,然后抽滤、水洗得粗产品
步骤3.粗产品用乙醇溶解并重结晶,得白色针状晶体并烘干,称得产品质量为33.0g。
(1)图中仪器名称:a 。
(2)简述装置b中将活塞上下部分连通的目的 。
(3)浓H2SO4需要冷却至0℃以下的原因是 。
(4)反应需要搅拌12h,其原因是 。
(5)本次实验产率为 。
(6)实验室制备乙酸乙酯的化学反应方程式 ,用 (填药品名称)收集粗产品,用 (填操作名称)的方法把粗产品分离。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com