
【题目】下列两种物质混合、静置后,可以用分液漏斗分离的是
A. 酒精和水 B. 碘和汽油
C. 水和四氯化碳 D. 食盐和水
 新思维假期作业寒假吉林大学出版社系列答案
新思维假期作业寒假吉林大学出版社系列答案科目:高中化学 来源: 题型:
【题目】周期表中有A、B、C三种原子序数依次增大的元素,A是地壳中含量最多的金属元素,B的价层电子排布为nsn-1npn+1,C是生活中的一种常用金属且其原子的外围电子排布为3d104s1。

(1)A基态原子的电子排布式为__________________。
(2)一氧化碳(与N2互为等电子体)分子中σ键与π键数目之比为________。
(3)C的单质和某化合物甲的微观部分结构分别如图所示,C微粒周围等距离且距离最近的C微粒有________个;甲的化学式为________(用M、N表示)。
(4)金属C在加热时与B的最高价氧化物对应水化物的浓溶液反应的化学方程式为____________。
(5)C元素的最高价氧化物的水化物能溶于氨水,该反应的化学方程式为__________________。
(6)联氨(N2H4)是航天飞船常用的高能燃料,可以用尿素为原料制取,方法是在KMnO4催化剂存在下,尿素[CO(NH2)2]和次氯酸钠、NaOH溶液反应生成联氨、Na2CO3、H2O及另外一种产物,写出该反应的化学方程式:____________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下表是元素周期表的一部分,列出11种元素在周期表中的位置,填写下列空白。

(1)第三周期元素中,原子半径最大的元素是(稀有气体除外)______,离子半径最小的是____(写元素符号)。
(2)J的简单离子的结构示意图__________。
(3)D、E、F、K四元素的最高价氧化物对应水化物,按碱性依次减弱顺序排列为(写化学式)____。
(4)比较G、H两元素的最高价氧化物对应水化物的酸性______(写化学式,下同)。比较C、G两元素的气态氢化物稳定性_________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对下列实验的描述不正确的是( )
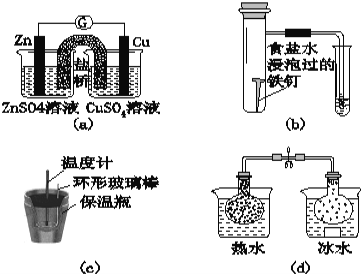
A.图(a)所示的实验:根据检流计(G)中指针偏转的方向比较Zn、Cu的金属活泼性
B.图(b)所示的实验:根据小试管中液面的变化判断铁钉发生析氢腐蚀
C.图(c)所示的实验:根据温度计读数的变化用稀盐酸和稀NaOH溶液反应测定中和热
D.图(d)所示的实验:根据两烧瓶中气体颜色的变化判断2NO2(g)![]() N2O4(g)是放热反应
N2O4(g)是放热反应
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在稀硫酸和稀硝酸的混合溶液中,加入铜粉。
(1)若将100mL 2mol/L HNO3和100mL 1mol/L H2SO4混合后,加入19.2g 铜粉,微热,充分反应。
①若忽略溶液体积变化,溶液中铜离子物质的量浓度为 mol/L
②生成气体折合成标准状况下体积 L;
③若使铜粉全部溶解,还需加入1mol/L H2SO4 mL
(2)若c(SO![]() )+c(NO
)+c(NO![]() )=5.0 mol·L-1。取200 mL该混合酸,则能溶解铜的最大质量为 g
)=5.0 mol·L-1。取200 mL该混合酸,则能溶解铜的最大质量为 g
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氮化钠(Na3N)是科学家制备的一种重要的化合物,它与水作用可产生NH3。请回答下列问题:
(1)Na3N的电子式是______,该化合物由______键形成。
(2)Na3N与盐酸反应生成________种盐,其电子式分别是________。
(3)Na3N与水的反应属于____________反应(填基本反应类型)。
(4)比较Na3N中两种粒子的半径:r(Na+)________r(N3-)(填“>”“=”或“<”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ksp(CaSO4)=9×10-6,常温下,CaSO4在水中的沉淀溶解平衡曲线如图所示。下列判断错误的是
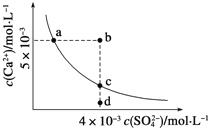
A.a、c两点均可以表示常温下CaSO4溶于水所形成的饱和溶液
B.a点对应的Ksp等于c点对应的Ksp
C.b点将有沉淀生成,平衡后溶液中c(SO42-)一定不等于3×10-3molL-1
D.向d点溶液中加入适量CaCl2固体可以变到c点
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氢氧化钠标准溶液因保存不当,吸收了少量的二氧化碳,若有1%的NaOH转变为Na2CO3,以此NaOH溶液滴定未知浓度的盐酸,选用甲基橙作指示剂;盐酸浓度的测定结果会( )
A.偏低1% B.偏高1% C.无影响 D.偏高0.1%
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com