
铁及其化合物在国民经济的发展中起着重要作用。
(1)已知:4Fe(s)+3O2(g)=2Fe2O3(s) △H=-1641.0 kJ·mol-1
C(石墨)+1/2O2(g)=CO(g) △H=-110.5 kJ·mol-1
则Fe2O3(s)+3C(石墨)=2Fe(s)+3CO(g)的△H= kJ·mol-1。
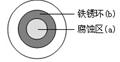 (2)将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色 (b),如右图所示。液滴中心是 区(填“正极”或“负极”),其电极反应式为 。为减缓钢铁的腐蚀,可与锌块相连,该方法称为 。
(2)将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆周中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色 (b),如右图所示。液滴中心是 区(填“正极”或“负极”),其电极反应式为 。为减缓钢铁的腐蚀,可与锌块相连,该方法称为 。
(3)铁钛合金是一种不锈钢材料,某同学在探究该合金的性质时,往含有TiO2+、Fe3+溶液中加入铁屑至溶液显紫色,该过程中发生的反应有:
①2TiO2+(无色)+Fe+4H+=2Ti3+(紫色)+Fe2++2H2O
②Ti3+(紫色)+Fe3++H2O= TiO2+(无色)+Fe2++2H+
③ 。
 小学夺冠AB卷系列答案
小学夺冠AB卷系列答案 ABC考王全优卷系列答案
ABC考王全优卷系列答案科目:高中化学 来源: 题型:
在一支25 mL的酸式滴定管中盛入0.1 mol·L-1 HCl溶液,其液面恰好在5 mL的刻度处,若把滴定管中的溶液全部放入烧杯中,然后以0.1 mol·L-1 NaOH溶液进行中和,则所需NaOH溶液的体积( )
A.大于20 mL B.小于20 mL C.等于20 mL D.等于5 mL
查看答案和解析>>
科目:高中化学 来源: 题型:
“ZEBRA”蓄电池的结构如图所示,电极材料多孔Ni/NiCl2和金属钠之间由钠离子导体制作的陶瓷管相隔。下列关于该电池的叙述错误的是( )
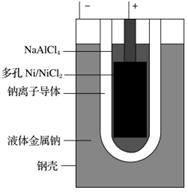
A.电池反应中有NaCl生成
B.电池的总反应是金属钠还原三价铝离子
C.正极反应为NiCl2+2e-===Ni+2Cl-
D.钠离子通过钠离子导体在两电极间移动
查看答案和解析>>
科目:高中化学 来源: 题型:
若NA表示阿伏加德罗常数,下列有关叙述正确的是
A.标准状况下,44.8L苯中分子数为2NA
B.1mol水中含氢离子数为NA
C.5.6g铁与足量稀硫酸完全反应失去电子数为0.3NA
D.16 g CH4与18 g NH4+ 所含电子数均为10NA
查看答案和解析>>
科目:高中化学 来源: 题型:
下列关于有机化合物的说法正确的是
A.苯在常温下可与溴水发生取代反应
B.糖类、油脂和蛋白质都能发生水解反应
C.乙醇和乙酸都能与金属钠反应
D.葡萄糖能发生氧化反应和银镜反应
查看答案和解析>>
科目:高中化学 来源: 题型:
从A出发,发生图示中的系列反应,其中B分子核磁共振氢谱有三组峰,峰面积比为1:2:2,F的苯环上一氯代物只有一种,Z和G均不能与金属钠反应,且互为同分异构体。

回答下列问题:
(1)F的化学名称为 。
(2)反应④的化学方程式为 ,在①~⑦的反应中,属于取代反应的有 。
(3)B的结构简式为 ,其所含官能团名称为 。
(4)E和F反应生成G的化学方程式为 。
(5)与B互为同分异构体,属于酚类且苯环上只有对位两取代的化合物有 种,写出可能的结构简式 , , , ,。
查看答案和解析>>
科目:高中化学 来源: 题型:
有关l3C、15N的下列说法正确的是
A.13C与15N有相同的中子数 B.13C与C60互为同素异形体
C. 15N与14N互为同位素 D.15N和14N的化学性质不同
查看答案和解析>>
科目:高中化学 来源: 题型:
(Ⅰ)硫、碳、硅是三种重要的非金属元素,请回答下列问题:
(1)它们的非金属性由强到弱的顺序是 (用元素符号表示),
| |
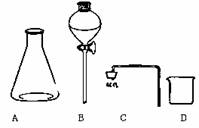
(2)请你用题中所给仪器设计一套装置证明(1)中的结论,在右边方框
中画出装置图;仪器B的名称是 。
(3)实验过程中在仪器B 中应装入的试剂是 ,烧杯中出现的现
象是 。若锥形瓶中装的是一种能溶于水的正盐,则
其中发生反应的离子方程式为 。
| |
(1)在右边方框中画出装置图。
(2)若实验时,M上有气泡,N上没气泡,则M的最高价氧化物对应
的水化物的碱性比N的最高价氧化物对应的水化物的碱性比
(填“强”或“弱”),外电路中电子由 (填M或N)极流
向 (填M或N)极。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com