
| A. | 72 | B. | 19 | C. | 53 | D. | 125 |
 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:选择题
| A. | 铝放入烧碱溶液中溶解:2Al+2OH-+2 H2O═2 AlO2-+3H2↑ | |
| B. | 碳酸钙溶于醋酸溶液:CaCO3+2H+═Ca2++CO2↑+H2O | |
| C. | 稀硫酸中加氢氧化钡溶液至中性:H++OH-═H2O | |
| D. | NaHCO3溶液中加入稀盐酸:CO32-+2H+═CO2↑+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )
金银花的有效成分为绿原酸,具有广泛的杀菌、消炎功能,其结构简式如图.下列有关绿原酸的说法中不正确的是( )| A. | 绿原酸分子中有4个手性碳原子(碳旁边连接4个不同的原子或原子团) | |
| B. | 绿原酸能发生显色反应、取代反应和加成反应 | |
| C. | 每摩尔绿原酸最多与4 mol NaOH反应 | |
| D. | 绿原酸分子中所有碳原子都能在同一平面上 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②⑤正确 | B. | 都不正确 | ||
| C. | ④正确,其他不正确 | D. | 仅①不正确 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
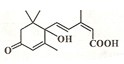 北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )
北京奥运会期间对大量盆栽鲜花施用了S-诱抗素制剂,以保持鲜花盛开.S-诱抗素的分子结构如图,下列关于该分子说法正确的是( )| A. | 其分子式为C15H20O4 | |
| B. | 该物质含三种官能团 | |
| C. | 能发生加成反应、取代反应、氧化反应、酯化反应、加聚反应 | |
| D. | 1mol该物质与足量NaOH溶液反应,最多消耗1molNaOH |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 甲酸 | B. | 乙酸 | C. | 丙酸 | D. | 乙二酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
 短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上)戊、己分别是空气、地壳中含量最多的元素,下列判断正确的是( )
短周期元素甲、乙、丙、丁、戊、己、庚在周期表中的相对位置如图(甲不一定在丁、庚的连线上)戊、己分别是空气、地壳中含量最多的元素,下列判断正确的是( )| A. | 甲一定是金属元素 | |
| B. | 气态氰化物的稳定性庚>己>戊 | |
| C. | 乙、丙、丁的最高价氧化物对应水化物可以相互反应 | |
| D. | 庚的最高价氧化物水化物酸性最强 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com