

| A. | 电子从b流出,经外电路流向a | |
| B. | HS在硫氧化菌作用下转化为SO42-的反应是HS-+4H2O-8e-═SO42-+9H+ | |
| C. | 如果将反应物直接燃烧,能量的利用率不会变化 | |
| D. | 若该电池电路中有0.4mol电子发生转移,则有0.5mol H+通过质子交换膜 |
分析 由图可知硫酸盐还原菌可以将有机物氧化成二氧化碳,而硫氧化菌可以将硫氢根离子氧化成硫酸根离子,所以两种细菌存在,就会循环把有机物氧化成CO2 放出电子,负极上HS-在硫氧化菌作用下转化为SO42-,失电子发生氧化反应,电极反应式是HS-+4H2O-8e-=SO42-+9H+;正极上是氧气得电子的还原反应4H++O2+4e-=2H2O,根据原电池的构成和工作原理知识来回答.
解答 解:A、b是电池的正极,a是负极,所以电子从a流出,经外电路流向b,故A错误;
B、负极上HS-在硫氧化菌作用下转化为SO42-,失电子发生氧化反应,电极反应式是HS-+4H2O-8e-=SO42-+9H+,故B正确;
C、如果将反应物直接燃烧,高温下微生物被杀死,效率更低,故C错误;
D、根据电子守恒,若该电池有0.4mol电子转移,有0.4molH+通过质子交换膜,故D错误,
故选B.
点评 本题考查原电池工作原理以及应用知识,注意知识的迁移应用是解题的关键,难度中等.


科目:高中化学 来源: 题型:选择题
| A. | W、X形成的化合物只含有离子键 | B. | 原子半径:Y>Z>W | ||
| C. | 还原性:W2->Y2- | D. | 氧化物的水化物酸性:Y<Z |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
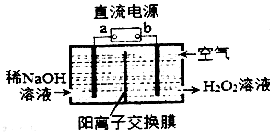 H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示:
H2O2是一种常用绿色氧化剂,工业上利用电解法制备H2O2的装置如图所示:查看答案和解析>>
科目:高中化学 来源: 题型:选择题
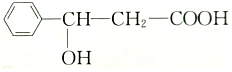 ,对该有机物的下列说法中正确的是( )
,对该有机物的下列说法中正确的是( )| A. | 含有羟基、苯基、羧基三种官能团 | B. | 属于芳香烃 | ||
| C. | 在一定条件下,能发生酯化反应 | D. | 属于羧基,也属于酚类 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ${\;}_{19}^{40}$K 与${\;}_{19}^{39}$K | B. | T2O与H2O | ||
| C. | CH3CH2CH2CH3与 | D. | CH3CH3与CH3CH3CH3 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
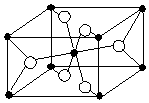 纳米级TiO2是一种光催化材料,可处理甲醛、氮氧化物等污染物,工业上也可用其催化乙醇脱氢制备乙醛:CH3CH2OH$\stackrel{TiO_{2}}{→}$CH3CHO+H2↑.
纳米级TiO2是一种光催化材料,可处理甲醛、氮氧化物等污染物,工业上也可用其催化乙醇脱氢制备乙醛:CH3CH2OH$\stackrel{TiO_{2}}{→}$CH3CHO+H2↑.查看答案和解析>>
科目:高中化学 来源:2016-2017学年江苏省徐州市高二上第一次月考化学试卷(解析版) 题型:选择题
某有机物Z具有较广泛的抗菌作用,其生成机理可由X与Y相互作用:



X Z
下列有关叙述中不正确的是( )
A.Z结构中有4个手性碳原子
B.Y的分子式为C9H8O3
C.1 mol Z与足量NaOH溶液反应,最多消耗8 mol NaOH
D.Z与浓溴水既能发生取代反应又能发生加成反应
查看答案和解析>>
科目:高中化学 来源:2016-2017学年河南省新乡市高二上第一次月考化学卷(解析版) 题型:选择题
对于反应:2X(g)+Y(g)  2Z(g)在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n(Z)和反应时间t的关系如右图所示,下列判断正确的是( )
2Z(g)在不同温度(T1和T2)及压强(p1和p2)下,产物Z的物质的量n(Z)和反应时间t的关系如右图所示,下列判断正确的是( )
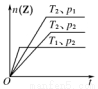
A.T1<T2,p1<p2,正反应为放热反应
B.T1>T2,p1>p2,正反应为吸热反应
C.T1>T2,p1>p2,正反应为放热反应
D.T1>T2,p1<p2,正反应为吸热反应
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com