
ŌŚĻĀĮŠČÜŅŗÖŠ·Ö±š¼ÓČėŅ»¶ØĮæµÄNa2O2¹ĢĢ壬²»»į³öĻÖ»ė×ĒµÄŹĒ£Ø £©
A£®±„ŗĶNa2CO3ČÜŅŗ
B£®Ca£ØHCO3£©2Ļ”ČÜŅŗ
C£®Na2SO3Ļ”ČÜŅŗ
D£®±„ŗĶCaCl2ČÜŅŗ
 ¼¤»īĖ¼Ī¬ÓżÓæĪĢĆĻµĮŠ“š°ø
¼¤»īĖ¼Ī¬ÓżÓæĪĢĆĻµĮŠ“š°ø »īĮ¦ŹŌ¾ķĻµĮŠ“š°ø
»īĮ¦ŹŌ¾ķĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğ½Ī÷Ź”¼Ŗ°²ŹŠøßŅ»ĻĀѧʌʌĩ»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ÓŠA”¢BĮ½ÖÖĢž£¬ŗ¬ĒāµÄÖŹĮæ·ÖŹżĻąĶ¬£¬ĻĀĮŠ¹ŲÓŚAŗĶBµÄŠšŹöÖŠ“ķĪóµÄŹĒ
A. AŗĶBæÉÄÜŹĒĶ¬·ÖŅģ¹¹Ģå
B. AŗĶB²»Ņ»¶ØŹĒĶ¬ĻµĪļ
C. AŗĶBĶźČ«Č¼ÉÕŗóÉś³ÉµÄĖ®µÄÖŹĮæĻąµČ
D. AŗĶBŗ¬Ģ¼µÄÖŹĮæ·ÖŹżĻąĶ¬
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½¶«Ź”øßŅ»6ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹĀŹµÄÜÅŠ¶Ļ½šŹōŌŖĖŲ¼×µÄ½šŹōŠŌŅ»¶Ø±ČŅŅĒæµÄÓŠ£Ø £©
¢Ł¼×µ„ÖŹÄÜÓėŅŅŃĪµÄČÜŅŗ·“Ó¦
¢Ś¼×”¢ŅŅĮ½Ö÷×åŌŖĖŲŌ×ÓµÄ×īĶā²ćµē×ÓŹżĻąĶ¬£¬ĒŅ¼×µÄŌ×Ó°ė¾¶Š”ÓŚŅŅ
¢Ū¼×”¢ŅŅĮ½¶ĢÖÜĘŚŌŖĖŲŌ×ӵĵē×Ó²ćŹżĻąĶ¬£¬ĒŅ¼×µÄŌ×ÓŠņŹżŠ”ÓŚŅŅ
¢Ü¼×”¢ŅŅĮ½ŌŖĖŲµÄµ„ÖŹŗĶŃĪĖį×é³ÉŌµē³Ų£¬ŅŅµ„ÖŹ±ķĆęÉś³ÉĒāĘų
¢ŻĮ½µ„ÖŹ·Ö±šÓėĀČĘų·“Ó¦Ź±Éś³ÉµÄŃōĄė×Ó£¬ŅŅŹ§Č„µÄµē×ÓŹż±ČŅŅ¶ą
A. Č«²ææÉŅŌ B. ½ö¢Ś²»æÉŅŌ C. ½ö¢Ś¢Ż²»æÉŅŌ D. ¢Ū¢ÜæÉŅŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½¶«Ź”ø߶žĻĀѧʌĮłŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĶʶĻĢā
A”¢B”¢C”¢DŹĒ֊ѧ»Æѧ³£¼ūµÄµ„ÖŹ£¬¼×”¢ŅŅ”¢±ūĪŖ»ÆŗĻĪļ£¬ŅŅŌŚ³£ĪĀ³£Ń¹ĻĀĪŖĪŽÉ«ĪŽĪ¶µÄŅŗĢ壬ŌŖĖŲAÓŠæɱä»ÆŗĻ¼Ū£¬ĖüĆĒÖ®¼ä“ęŌŚČēĻĀĶ¼µÄĖłŹ¾µÄ×Ŗ»Æ¹ŲĻµ”£ÓÉ“ĖĶʶĻ£ŗ

£Ø1£© ¼×µÄ»ÆѧŹ½ĪŖ________£¬±ūµÄ»ÆѧŹ½ĪŖ_________”£
£Ø2£©Š“³ö¼×ŗĶD·“Ó¦µÄ»Æѧ·½³ĢŹ½_______________________”£
£Ø3£©ŅŃÖŖDÄÜÓėÉÕ¼īČÜŅŗ·“Ó¦£¬Š“³öDÓėÉÕ¼īČÜŅŗ·“Ó¦µÄĄė×Ó·½³ĢŹ½_______________”£
£Ø4£©ĪŖ¼ģŃé»ÆŗĻĪļ¼×ÖŠŌŖĖŲµÄ»ÆŗĻ¼Ū£¬ŠčŅŖÓƵ½µÄŅ©Ę·ÓŠ___________
A£®Ļ”ĮņĖį
B£®ŃĪĖį
C£®ĮņĒč»Æ¼ŲČÜŅŗ
D£®øßĆĢĖį¼ŲČÜŅŗ
£Ø5£©ĪŖ²ā¶ØAŗĶŅŅøßĪĀ·“Ó¦ŗóĖłµĆ¹ĢĢåÖŠ»ÆŗĻĪļ¼×µÄÖŹĮæ·ÖŹż”£Č”·“Ó¦ŗóĖłµĆ¹ĢĢå²¢Éč¼ĘŅŌĻĀŹµŃé£ŗ

»ÆŗĻĪļ¼×µÄÖŹĮæ·ÖŹżĪŖ______”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½¶«Ź”ø߶žĻĀѧʌĮłŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
³£ĪĀĻĀ£¬²»ČÜÓŚÅØH2SO4£¬Ņ²²»ČÜÓŚÅØHNO3ŗĶÅØNaOHČÜŅŗµÄ½šŹōŹĒ £Ø £©
A£®Ģś B£®ÄĘ C£®Ć¾ D£®Ķ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½¶«Ź”ø߶žĻĀѧʌĮłŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻĀĮŠŹµŃéÄܳɹ¦µÄŹĒ £Ø £©
¢ŁÓĆ×ĘÉշؼų±šNa2CO3¹ĢĢåŗĶNaHCO3¹ĢĢå
¢ŚÓĆ¹Ū²ģ·ØĒų±šNa2O·ŪÄ©ŗĶNa2O2·ŪÄ©
¢ŪÓĆAlCl3ČÜŅŗ¼ų±šNa2CO3ČÜŅŗŗĶNaOHČÜŅŗ
¢ÜÓĆ³ĪĒåŹÆ»ŅĖ®¼ų±šNa2CO3ČÜŅŗŗĶNaHCO3ČÜŅŗ
A£®Č«²æ B£®¢Ł¢Ś¢Ü C£®¢Ś¢Ū¢Ü D£®¢Ł¢Ś¢Ū
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĖÄ“ØŹ”³É¶¼ŹŠøßŅ»ĻĀ4ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĶʶĻĢā
X”¢Y”¢Z”¢WŹĒŌ×ÓŠņŹżŅĄ“ĪŌö“óµÄ¶ĢÖÜĘŚŌŖĖŲ£¬ĒŅ»„²»Ķ¬×壻ĘäÖŠÖ»ÓŠĮ½ÖÖĪŖ½šŹō£»XŌ×ÓµÄ×īĶā²ć×ÓŹżÓė“ĪĶā²ćµē×ÓŹżĻąµČ£»XÓėW”¢YÓėZÕāĮ½¶ŌŌ×ÓµÄ×īĶā²ćµē×ÓŹżÖ®ŗĶ¾łĪŖ9£®µ„ÖŹYŗĶW¶¼æÉÓėÅصÄNaOHČÜŅŗ·“Ó¦£®Ēė»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Y”¢Z”¢WµÄŌ×Ó°ė¾¶ÓÉŠ”µ½“óµÄĖ³Šņ £®
£Ø2£©ZW2µÄµē×ÓŹ½ŹĒ £®
£Ø3£©ŹµŃéŹŅÖʱøYµÄ×īøß¼ŪŃõ»ÆĪļµÄĖ®»ÆĪļµÄĄė×Ó·½³ĢŹ½ŹĒ
£Ø4£©XÓėY»ÆѧŠŌÖŹĻąĖĘ£¬ŌņXÓėÅصÄNaOHČÜŅŗ·“Ó¦µÄ»Æѧ·½³ĢŹ½ŹĒ
£Ø5£©0.1molµÄµ„ÖŹWÓė50mL 1.5mol/LµÄFeBr2ČÜŅŗ·“Ó¦£¬Ōņ±»Ńõ»ÆµÄFe2+ŗĶBr©µÄĪļÖŹµÄĮæÖ®±ČŹĒ £®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016ѧğĖÄ“ØŹ”³É¶¼ŹŠøßŅ»ĻĀ4ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
A”¢B”¢C¾łĪŖÖÜĘŚ±ķÖŠµÄ¶ĢÖÜĘŚµÄŌŖĖŲ£¬ĖüĆĒŌŚÖÜĘŚ±ķµÄĪ»ÖĆČēĻĀĶ¼£®ŅŃÖŖB”¢CĮ½ŌŖĖŲŌŚÖÜĘŚ±ķÖŠ×åŹżÖ®ŗĶŹĒAŌŖĖŲ×åŹżµÄ2±¶£»B”¢CŌŖĖŲµÄŌ×ÓŠņŹżÖ®ŗĶŹĒA ŌŖĖŲµÄŌ×ÓŠņŹżµÄ4±¶£¬ŌņA”¢B”¢CĖłŌŚµÄŅ»×éŹĒ £Ø £©
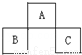
A£®Be”¢Na”¢Al B£®P”¢O”¢Cl C£®O”¢P”¢Cl D£®C”¢Al”¢P
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2015-2016Ń§ÄźÉ½Ī÷“óѧø½ÖŠø߶žĻĀ3ŌĀŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ĖÄÖÖ¶ĢÖÜĘŚŌŖĖŲA”¢B”¢C”¢D£¬A”¢B”¢CĶ¬ÖÜĘŚ£¬C”¢DĶ¬Ö÷×壬EŹĒ¹ż¶ÉŌŖĖŲ£®AµÄŌ×Ó½į¹¹Ź¾ŅāĶ¼ĪŖ£ŗ £¬BŹĒĶ¬ÖÜĘŚµŚŅ»µēĄėÄÜ×īŠ”µÄŌŖĖŲ£¬CµÄ×īĶā²ćÓŠČżøö³Éµ„µē×Ó£¬EµÄĶāĪ§µē×ÓÅŲ¼Ź½ĪŖ3d64s2£®»Ų“šĻĀĮŠĪŹĢā£ŗ
£¬BŹĒĶ¬ÖÜĘŚµŚŅ»µēĄėÄÜ×īŠ”µÄŌŖĖŲ£¬CµÄ×īĶā²ćÓŠČżøö³Éµ„µē×Ó£¬EµÄĶāĪ§µē×ÓÅŲ¼Ź½ĪŖ3d64s2£®»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£©Š“³öĻĀĮŠŌŖĖŲµÄ·ūŗÅ£ŗA B
£Ø2£©ÓĆ»ÆѧŹ½±ķŹ¾ÉĻŹöĪåÖÖŌŖĖŲÖŠ×īøß¼ŪŃõ»ÆĪļ¶ŌÓ¦Ė®»ÆĪļĖįŠŌ×īĒæµÄŹĒ £®
£Ø3£©ÓĆŌŖĖŲ·ūŗűķŹ¾DĖłŌŚÖÜĘŚµŚŅ»µēĄėÄÜ×ī“óµÄŌŖĖŲŹĒ £®
£Ø4£©DµÄĒā»ÆĪļ±ČCµÄĒā»ÆĪļµÄ·Šµć £ØĢī”°øß”°»ņ”°µĶ”°£©£¬ŌŅņŹĒ £®
£Ø5£©EŌŖĖŲŌ×ÓµÄŗĖµēŗÉŹżŹĒ £¬EŌŖĖŲŌŚÖÜĘŚ±ķµÄµŚ ×壮ŌŖĖŲÖÜĘŚ±ķæÉ°“µē×ÓÅŲ¼·ÖĪŖsĒų”¢pĒųµČ£¬ŌņEŌŖĖŲŌŚ Ēų£®
£Ø6£©»³öDµÄŗĖĶāµē×ÓÅŲ¼Ķ¼ £¬ÕāŃłÅŲ¼×ńŃĮĖ¹¹ŌģŌĄķ”¢ ŌĄķŗĶ ¹ęŌņ£®
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com