
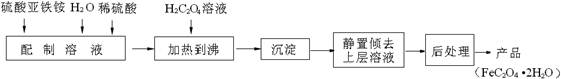
 6H2O��Һʱ���������ϡ���ᣬĿ����________________________________________________________��
6H2O��Һʱ���������ϡ���ᣬĿ����________________________________________________________��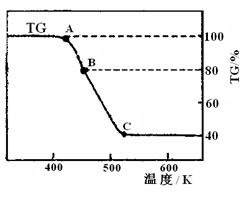
 B������Ӧ�Ļ�ѧ����ʽΪ
B������Ӧ�Ļ�ѧ����ʽΪ Fe(s)+CO2(g)��Ӧƽ�ⳣ��K=0.4����÷�Ӧ��ƽ��ʱ��FeO��ת����Ϊ���٣�____________________________��
Fe(s)+CO2(g)��Ӧƽ�ⳣ��K=0.4����÷�Ӧ��ƽ��ʱ��FeO��ת����Ϊ���٣�____________________________�� ����ѵ�����⿼ϵ�д�
����ѵ�����⿼ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
 2NH3(g) ��H����92.4kJ��mol��1����ش�
2NH3(g) ��H����92.4kJ��mol��1����ش� H2��NH3����������Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ��
H2��NH3����������Ӧ������ʱ��Ĺ�ϵ����ͼ��ʾ��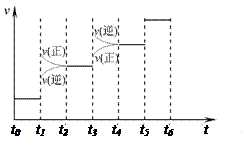
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ������
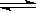 2CO(g)ƽ�ⳣ��K�ı���ʽΪ ��
2CO(g)ƽ�ⳣ��K�ı���ʽΪ ��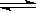 CO(g)+H2(g)��ƽ�ⳣ��ΪK1��H2(g)��CO2(g)
CO(g)+H2(g)��ƽ�ⳣ��ΪK1��H2(g)��CO2(g) 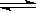 CO(g)��H2O(g)��ƽ�ⳣ��ΪK2 ����K��K1��K2���ߵĹ�ϵΪ ��
CO(g)��H2O(g)��ƽ�ⳣ��ΪK2 ����K��K1��K2���ߵĹ�ϵΪ �� 2SO3����ƽ�ⳣ��K=19
2SO3����ƽ�ⳣ��K=19 ��1������Ӧ�ڸ��¶���SO2ת����Ϊ80��ʱ���÷�Ӧ (��ǡ���)�ﵽ��ѧƽ��״̬����δ�ﵽ���� (�����Ӧ�����淴Ӧ��) ������С�
��1������Ӧ�ڸ��¶���SO2ת����Ϊ80��ʱ���÷�Ӧ (��ǡ���)�ﵽ��ѧƽ��״̬����δ�ﵽ���� (�����Ӧ�����淴Ӧ��) ������С� cC(g)+dD(g) ��H = a kJ��mol-1��
cC(g)+dD(g) ��H = a kJ��mol-1���鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2AB(g) �ﵽ��ѧƽ��ı�־�ǣ� ��
2AB(g) �ﵽ��ѧƽ��ı�־�ǣ� ��| A����λʱ��������nmolA2ͬʱ����nmolB2 |
| B����λʱ��������nmol A2ͬʱ������nmolB2 |
| C��ѹǿ����ʱ��仯���ı� |
| D����λʱ�����nmol A��A���ۼ�ͬʱ����nmol A��B���ۼ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 2C(g)+xD(g)��5s�ﵽƽ�⡣�ﵽƽ��ʱ��������2molC�����ⶨD��Ũ��Ϊ0.5mol/L�������ж���ȷ����
2C(g)+xD(g)��5s�ﵽƽ�⡣�ﵽƽ��ʱ��������2molC�����ⶨD��Ũ��Ϊ0.5mol/L�������ж���ȷ����| A��x="1" | B��B��ת����Ϊ20% |
| C��ƽ��ʱA��Ũ��Ϊ1.50mol/L | D��B��ƽ����Ӧ����Ϊ0��2 mol/��L��s�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 CO2+H2����ƽ�����CO2Ϊ0.75 mol��ͨ��6 molˮ�������ﵽ�µ�ƽ���CO2��H2�����ʵ���֮�Ϳ���Ϊ
CO2+H2����ƽ�����CO2Ϊ0.75 mol��ͨ��6 molˮ�������ﵽ�µ�ƽ���CO2��H2�����ʵ���֮�Ϳ���Ϊ| A��1.2 mol | B��1.5 mol | C��1.8 mol | D��2.5 mol |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��

 2SO3��g�������ﵽƽ�⡣��������У�����������������䣬����������ѹǿ���䣬����������SO2��ת����Ϊp%������������SO2��ת���ʣ�������
2SO3��g�������ﵽƽ�⡣��������У�����������������䣬����������ѹǿ���䣬����������SO2��ת����Ϊp%������������SO2��ת���ʣ�������| A������p%���� | B������p�� | C��С��p�� | D�����ж� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 g��+B��g��
g��+B��g�� nC��g����H=Q���ڲ�ͬ�����·�Ӧ�������C�İٷֺ�
nC��g����H=Q���ڲ�ͬ�����·�Ӧ�������C�İٷֺ� ���ͷ�Ӧ������ʱ��Ĺ�ϵ���ߡ������й�������һ����ȷ���ǣ���
���ͷ�Ӧ������ʱ��Ĺ�ϵ���ߡ������й�������һ����ȷ���ǣ���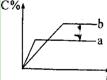
| A����ͼ����������жϣ���Ӧһ��������Ӧ����ʼ |
| B��ֻ�����¶ȣ���a��b���¶ȸߣ�Q��0 |
| C��ֻ����ѹǿ����a��b��ѹǿ��n��2 |
| D��������Ϊ���������ʾa�д�����b��ʾû�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ������ ���ͣ���ѡ��
 Ag���̣���Fe3��������Ӧ���ȣ�
Ag���̣���Fe3��������Ӧ���ȣ��鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com