
��֪X��Y��Z��QΪ�����ڷǽ���Ԫ�أ�R�dz�����Ԫ�أ�Xԭ�ӵĵ���ռ��2�����Ӳ���ԭ���гɶԵ�������δ�ɶԵ�������2����Y�Ļ�̬ԭ����7�ֲ�ͬ�˶�״̬�ĵ��ӣ�ZԪ���ڵؿ��к�����ࣻQ�ǵ縺������Ԫ�أ�R+����ֻ���������Ӳ�����ȫ�������ӡ�
�ش��������⣺������ʱ��X��Y��Z��Q��R������Ӧ��Ԫ�ط��ű�ʾ��
��1��XԪ��Ϊ ��X��Y��Z�е�һ������������ ��
��2����֪Y2Q2���Ӵ�����ͼ��ʾ�����ֽṹ�����ģ�ͣ����߲�һ��������������
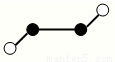
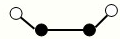
�÷�����Yԭ�ӵ��ӻ���ʽ�� ��
��3��X��YԪ�ؿ����γ�һ�ֳ�Ӳ�²��ϣ��侧�岿�ֽṹ����ͼ��ʾ���йظþ����˵����ȷ���� ����д��ĸ��ţ���

A���þ������ڷ��Ӿ��� B���˾����Ӳ�ȱȽ��ʯ����
C������Ļ�ѧʽ��X3Y4 D�������ۻ�ʱ�ƻ����ۼ�
��4����һ��AB�ͷ�����Y���ʷ��ӻ�Ϊ�ȵ����壬����һ�ֳ��õĻ�ԭ�����仯ѧʽΪ ��
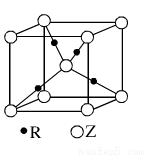
��5��R�Ļ�̬ԭ�ӵĵ����Ų�ʽΪ ��R��Z�γɵ�ij���Ӿ���ľ����ṹ����ͼ����þ���Ļ�ѧʽΪ ���þ�����ܶ�Ϊa g��cm��3����������� cm3���ú�a��NA�Ĵ���ʽ��ʾ����

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ�꽭��ʡ�߶���12���¿���ѧ�Ծ��������棩 ���ͣ�ʵ����
Ϊ�˱������������������Դ��ij�о�С��ͨ����ͼ�����̣�����ҵ���������������������Fe2O3��SiO2��Al2O3�ȣ�ת�����Ҫ�Ĺ�ҵԭ��FeSO4����Ӧ�����ԣ�
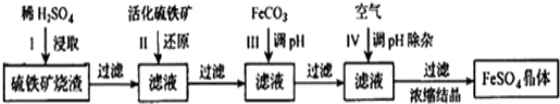
�������ԭFe3+����Ҫ��ӦΪ��FeS2+7Fe2��SO4��3+8H2O�T15FeSO4+8H2SO4��������������Ӧ����ش��������⣺
��1����1��H2SO4��Fe2O3��Ӧ�����ӷ���ʽ��_____ _____��
��2�������II����Fe3+�Ƿ���ȫ��ԭ��Ӧѡ��__________������ĸ��ţ���
A��KMnO4��Һ B��KSCN��Һ C��KCl��Һ D�� KOH
��3����III����FeCO3����ҺpH=6ʱ������������ݼ��㣬����֪Ksp Al��OH��3=1.9��10��33��������Ũ��С��1��10��5mol•L��1ʱ������Ϊ������ȫ���ж�Al3+_______����ǡ����ܳ�����ȫ��
��4��FeCO3�ڿ����м��ȷ�Ӧ���Ƶ���ϵ��������ϣ�
��֪25�棬101kPaʱ��4Fe��s��+3O2��g���T2Fe2O3��s����H=��1648kJ/mol
C��s��+O2��g���TCO2��g����H=��393kJ/mol
2Fe��s��+2C��s��+3O2��g���T2FeCO3��s����H=��1480kJ/mol
FeCO3�ڿ����м��ȷ�Ӧ����Fe2O3���Ȼ�ѧ����ʽ��__________��
��5��FeSO4��Һ�ڼ���Ũ���ᾧʱҪע��_________________________________,FeSO4��һ�������¿��Ƶ�FeS2���������������ײ��ϣ��ò��Ͽ��������������﮵�أ���طŵ�ʱ���ܷ�ӦΪ4Li+FeS2�TFe+2Li2S��������Ӧʽ��__________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ������ʡ�߶���12���¿���ѧ�Ծ��������棩 ���ͣ�ѡ����
��ͼ��ʾ��ͼ���Ǻ�ѹ�ܱ�������ͼ���Ǻ����ܱ�������������������ͬʱ���ڢ��зֱ����2 mol X��2 mol Y����ʼʱ�����������ΪV L���������·�Ӧ���ﵽƽ��״̬�� 2X(?)+Y(?)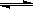 aZ(g)����ʱ����X��Y��Z�����ʵ���֮��Ϊ1��3��2�������ж���ȷ����
aZ(g)����ʱ����X��Y��Z�����ʵ���֮��Ϊ1��3��2�������ж���ȷ����
A������Z�Ļ�ѧ������a = 2
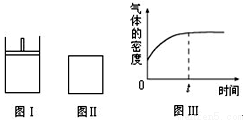
B��������������ܶ���ͼ����ʾ����X��Y��ֻ��һ��Ϊ��̬
C����X��Y��Ϊ��̬������ƽ��ʱX��ת���ʣ���
D����XΪ��̬��YΪ��̬������дӿ�ʼ��ƽ�������ʱ�䣺��>��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���������������ѧ�߶���10���¿���ѧ���������棩 ���ͣ�ѡ����
��֪��C(s)��CO2(g)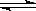 2CO(g) ��H��0���÷�Ӧ�ﵽƽ����������������ڷ�Ӧ���淽����е���
2CO(g) ��H��0���÷�Ӧ�ﵽƽ����������������ڷ�Ӧ���淽����е���
A�������¶Ⱥ�����ѹǿ B�������¶Ⱥͼ�Сѹǿ
C�������¶Ⱥ�����ѹǿ D�������¶Ⱥͼ�Сѹǿ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ���������������ѧ�߶���10���¿���ѧ���������棩 ���ͣ�ѡ����
��λͬѧ��ѧϰ����ѧ��Ӧ���ʺͻ�ѧƽ�⡱����ϵ��ҵ����ʵ���������Ĺ۵㣬����Ϊ����ȷ����
A����ѧ��Ӧ�����������о�������һ��ʱ���ڿ����Ʒ
B����ѧƽ���������о�����ʹ������ԭ�϶����Ʒ
C����ѧ��Ӧ�����������о��������ԭ��ת����
D����ѧƽ���������о�����ʹԭ�Ͼ����ܶ��ת��Ϊ��Ʒ
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016������ӳ��и����ϵ�����¿����ۻ�ѧ�Ծ��������棩 ���ͣ�ѡ����
��������Һ�У���������һ���ܹ������������
A����ʹ�㷺pH��ֽ����ɫ����Һ��K����Ba2����Cl����Br��
B��������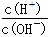 =12����Һ��Fe2����Mg2����NO3-��Cl��
=12����Һ��Fe2����Mg2����NO3-��Cl��
C�����д���Al3+����Һ�У�Na����Cl����AlO2-��OH��
D����ʹ���۵⻯����ֽ����ɫ����Һ��K+��SO42-��S2-��SO32-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪��ʡ�����ϵڶ���ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��֪��Ӧ��10AgF+5Cl2+5H2O=9AgCl+AgClO3+10HF+O2 ,���й��ڸ÷�Ӧ����������ȷ����
A���÷�Ӧ�У��������뻹ԭ�����ʵ���֮��Ϊ9��5
B������Ӧ����1mol����ת��ʱ������ԭ�������ʵ���Ϊ1/18 mol
C��ÿ����1mol O2ʱ������Ԫ�ػ�ԭ���������ʵ���Ϊ2mol
D���μӷ�Ӧ��ˮ��2/5������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2016�켪��ʡ�����ϵڶ���ģ�⻯ѧ�Ծ��������棩 ���ͣ�ѡ����
��ȼ�ױ��ж��Ļ�ѧ���������װ��Ӧ����Σ�վ����ǩ���������������˱�ǩ����
A | B | C | D | |
���ʵĻ�ѧʽ | ŨH2SO4 | CCl4 | P4 | NH4NO3 |
Σ�վ����ǩ | ��ʴƷ | ��ȼƷ | �綾Ʒ | ��ըƷ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ��2015-2016ѧ��ɽ��ʡ�߶���ѧ�����в��Ի�ѧ�Ծ��������棩 ���ͣ�ѡ����
����˵����ȷ����
A��������μӵĻ�ѧ��Ӧ��������ѹǿ�������ӻ���ӵİٷ������Ӷ�ʹ��Ӧ��������
B������Ӧ��Ũ�ȣ����������ӵİٷ������Ӷ�ʹ��λʱ������Ч��ײ��������
C���ڻ�ѧ��Ӧ�У��������ֻ����������Ӧ����
D�������¶���ʹ��ѧ��Ӧ����������Ҫԭ���������˷�Ӧ������л���ӵİٷ���
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com