
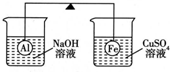
 在杠杆的两端分别挂着质量相同的铝球和铁球,此时杠杆平衡.然后将两球分别浸没在溶液质量相等的稀烧碱溶液和硫酸铜溶液中一段时间,如下图所示.下列说法正确的是( )
在杠杆的两端分别挂着质量相同的铝球和铁球,此时杠杆平衡.然后将两球分别浸没在溶液质量相等的稀烧碱溶液和硫酸铜溶液中一段时间,如下图所示.下列说法正确的是( )| A. | 铝球表面有气泡产生,且有白色沉淀生成,杠杆不平衡 | |
| B. | 铝球表面有气泡产生,溶液澄清;铁球表面有红色物质析出,溶液蓝色变浅,杠杆右边下沉 | |
| C. | 反应后去掉两烧杯,杠杆仍平衡 | |
| D. | 右边球上出现红色,左边溶液的碱性增强 |
分析 左烧杯中的铝球与NaOH溶液反应生成NaAlO2和H2,有气泡冒出,质量减小,没有沉淀生成,溶液仍为澄清,消耗了NaOH,溶液的碱性减弱;
右烧杯中铁球与CuSO4溶液反应生成FeSO4和Cu,铁球表面有红色物质析出,质量增加,溶液中Cu2+减少,溶液蓝色变浅,据此分析选项.
解答 解:A.左烧杯中发生2Al+2NaOH+2H2O=2NaAlO2+3H2↑,不生成沉淀,故A错误;
B.左烧杯中发生2Al+2NaOH+2H2O=2NaAlO2+3H2↑,右烧杯中发生Fe+CuSO4=Cu+FeSO4,观察到铝球表面有气泡产生,溶液澄清,而铁球表面有红色物质析出,溶液蓝色变浅,由反应可知左烧杯中Al的质量变小,右烧杯中Fe球上生成Cu质量变大,杠杆右边下沉,故B正确;
C.由选项B的分析可知,反应后去掉两烧杯,杠杆不能平衡,故C错误;
D.右边球上生成Cu,则出现红色,而左边溶液中消耗NaOH,则c(OH-)减小,碱性减弱,故D错误;
故选B.
点评 本题考查铝的化学性质,为高频考点,把握习题中的信息及发生的反应为解答的关键,侧重分析与应用能力的考查,注意利用差量法分析质量变化,题目难度不大.


 轻巧夺冠周测月考直通中考系列答案
轻巧夺冠周测月考直通中考系列答案科目:高中化学 来源: 题型:解答题
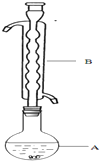 Na2S2O3俗称大苏打(海波)是重要的化工原料.用Na2SO3和硫粉在水溶液中加热反应,可以制得Na2S2O3.已知10℃和70℃时,Na2S2O3在100g水中的溶解度分别为60.0g和212g.常温下,从溶液中析出的晶体是Na2S2O3•5H2O.
Na2S2O3俗称大苏打(海波)是重要的化工原料.用Na2SO3和硫粉在水溶液中加热反应,可以制得Na2S2O3.已知10℃和70℃时,Na2S2O3在100g水中的溶解度分别为60.0g和212g.常温下,从溶液中析出的晶体是Na2S2O3•5H2O.| 滴定次数 | 滴定前读数(mL) | 滴定滴定后读数(mL) |
| 第一次 | 0.30 | 31.12 |
| 第二次 | 0.36 | 31.56 |
| 第三次 | 1.10 | 31.88 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 将等浓度、等体积的HCl和NaX溶液混合,若混合溶液pH<7,证明HX是弱酸 | |
| B. | 室温下,测1 mol/L NaX溶液的pH,若pH>7,证明HX是弱酸 | |
| C. | 室温下,测0.1 mol/L HX溶液的pH,若pH>1,证明HX是弱酸 | |
| D. | 相同条件下,对0.1 mol/L的HCl和0.1 mol/L的HX进行导电性实验,若与HX溶液相串联的灯泡较暗,证明HX为弱酸 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | C2H6+Cl2→C2H5Cl+HCl | B. | CH2═CH2+H2O→CH3CH2OH | ||
| C. |  +HO-NO2→ +HO-NO2→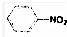 +H2O +H2O | D. | CH3CH2Cl+NaOH→CH2═CH2+NaCl+H2O |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 该反应的离子方程式为CO32-+2H+═CO2↑+H2O | |
| B. | 与同浓度的盐酸反应,块状大理石的反应速率比粉末状的大 | |
| C. | CaCO3溶于盐酸是因为H+破坏了CaCO3的沉淀溶解平衡,使其ksp增大 | |
| D. | CaCO3与适量的盐酸恰好完全反应所得溶液中c(H+)=c(OH-)+2c(CO32-)+c(HCO3-) |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 给试管里的液体加热,液体的体积一般不超过试管容积的$\frac{1}{2}$ | |
| B. | 向酒精灯里添加酒精,不可超过酒精灯容积的$\frac{2}{3}$ | |
| C. | 酒精灯使用完毕,应立即用嘴吹灭火焰 | |
| D. | 用燃着的酒精灯去点燃另一盏酒精灯 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 两溶液加入等质量的锌粉,产生氢气的速率相同 | |
| B. | 两溶液中氢氧根离子浓度均为10-13 mol/L | |
| C. | 加入醋酸钠固体,二者的pH均增大 | |
| D. | 恰好完全反应时,二者消耗氢氧化钠的质量相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
 氮元素可形成多种金属氮化物,如氮化钠(Na3N)、氮化镁(Mg3N2)和叠氮化钠(NaN3)等.
氮元素可形成多种金属氮化物,如氮化钠(Na3N)、氮化镁(Mg3N2)和叠氮化钠(NaN3)等.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | Mg2Al2(OH)4(CO3)3 | B. | Mg3Al2(OH)6(CO3)2 | C. | Mg3Al(OH)3(CO3)3 | D. | Mg3Al2(OH)8(CO3)2 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com