
【题目】钡在氧气中燃烧时得到一种钡的氧化物晶体,结构如图所示,有关说法不正确的是( )

A. 该晶体属于离子晶体
B. 晶体的化学式为Ba2O2
C. 该晶体晶胞结构与NaCl相似
D. 与每个Ba2+距离相等且最近的Ba2+共有12个
 智能训练练测考系列答案
智能训练练测考系列答案科目:高中化学 来源: 题型:
【题目】2018年9月26日,第五届硒博会在恩施州文化中心大剧院开幕。第五届硒博会主题为“健康中国·硒引天下”。硒(Se)是第四周期第VI A族元素,是人体内不可或缺的微量元素,H2Se是制备新型光伏太阳能电池、半导体材料和金属硒化物的重要原料。
(1)已知:①2H2Se(g)+O2(g) ![]() 2Se(s)+2H2O(l) △H =a kJ·mol-1
2Se(s)+2H2O(l) △H =a kJ·mol-1
②2H2 (g)+O2(g![]() 2H2O(l) △H=b kJ·mol—1
2H2O(l) △H=b kJ·mol—1
反应H2(g)+ Se(s) ![]() H2Se(g)的反应热△H=______kJ·mol-1(用含a、b的代数式表示)。
H2Se(g)的反应热△H=______kJ·mol-1(用含a、b的代数式表示)。
(2)T℃时,向一恒容密闭容器中加入3molH2和1 mol Se,发生反应H2 (g)+Se(s)![]() H2Se(g),
H2Se(g),
①下列情况可判断反应达到平衡状态的是_______(填字母代号)。
a. 气体的密度不变 b. v(H2) =v(H2Se)
c. 气体的压强不变 d.气体的平均摩尔质量不变
②当反应达到平衡后,将平衡混合气体通入气体液化分离器使H2Se气体转化为H2Se液体,并将分离出的H2再次通入发生反应的密闭容器中继续与Se反应时,Se的转化率会提高。请用化学平衡理论解释:________________________________________________。
③以5小时内得到的H2Se为产量指标,且温度、压强对H2Se产率的影响如图所示:

则制备H2Se的最佳温度和压强为________。
(3)已知常温下H2Se的电离平衡常数![]() ,则NaHSe溶液呈_______(填“酸性”或“碱性”),该溶液中的物料守恒关系式为_____________。
,则NaHSe溶液呈_______(填“酸性”或“碱性”),该溶液中的物料守恒关系式为_____________。
(4)工业上从含硒废料中提取硒的方法是用硫酸和硝酸钠的混合溶液处理后获得亚硒酸和少量硒酸,再与盐酸共热,硒酸转化为亚硒酸,硒酸与盐酸反应的化学方程式为___________,最后通入SO2析出硒单质。
(5) H2 Se在一定条件下可以制备出CuSe,已知常温时CuSe的Ksp=7.9![]() ,CuS的
,CuS的![]() ,则反应CuS(s)+Se2-(aq)
,则反应CuS(s)+Se2-(aq)![]() CuSe(s)+S2-(aq)的化学平衡常数K=_____ (保留2位有效数字)。
CuSe(s)+S2-(aq)的化学平衡常数K=_____ (保留2位有效数字)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在1L密闭容器中进行如下反应:X(g)+3Y(g)![]() 2Z(g),达到平衡时 X、Y、Z的物质的量分别为 0.1mol、0.3mol、0.2mol,保持温度和容器体积不变时,再向容器中充入X、Y、Z的物质的量0.1mol、0.3mol、0.2mol,则下列说法正确的是
2Z(g),达到平衡时 X、Y、Z的物质的量分别为 0.1mol、0.3mol、0.2mol,保持温度和容器体积不变时,再向容器中充入X、Y、Z的物质的量0.1mol、0.3mol、0.2mol,则下列说法正确的是
A. 化学平衡常数不变,平衡不移动 B. 向正反应方向移动
C. 向逆反应方向移动 D. 容器内压强始终保持原来的2倍
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】t℃时,将3 mol A和2 mol B气体通人体积为2L的密闭容器中(容积不变),发生如下反应:3A(g)+B(g) ![]() 2C(g),2 min时反应达到平衡状态(温度不变),测得C的浓度为0.2 mol/L,请填写下列空白:
2C(g),2 min时反应达到平衡状态(温度不变),测得C的浓度为0.2 mol/L,请填写下列空白:
(1)该过程用A表示的反应速率为:v(A)=_______;该温度下该反应的化学平衡常数表达式为__________。
(2)比较达到平衡时,A、B两反应物的转化率:α(A)______α(B)(填“>”、“=”或“<”)。
(3)判断反应达到平衡状态的依据是(填字母序号)__________。
a.生成C的速率与消耗B的速率相等 b.混合气体的密度不变
c.混合气体的相对平均分子质量不变 d.A的质量分数不再发生变化
(4)若升高温度,再次达平衡时,平衡常数数值变大,则该反应的![]() H_____0(填“>”、“=”或“<”)。
H_____0(填“>”、“=”或“<”)。
(5)若保持温度不变时,继续向原平衡混合物的容器中通入少量氦气(氦气和A、B、C都不反应)后,则化学反应速率会__________(填“加快”、“减慢”或“不变”),化学平衡将_________(填“正反应方向移动”、“逆反应方向移动”或“不移动”)。
(6)在恒温恒容密闭容器中进行上述反应,起始投料时各物质的浓度如下表:
A | B | C | |
投料I | 3.0 mol/L | 1.0 mol/L | 0 |
投料II | 2.0 mol/L | 1.0 mol/L | 2.0 mol/L |
按投料I进行反应,测得达到化学平衡状态时A的转化率为40%,若按投料II进行反应,起始时反应进行的方向为________(填“正向”、“逆向”或“不移动)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】第四周期过渡元素如铁、锰、铜、锌等在太阳能电池、磁性材料等科技方面有广泛的应用,回答下列问题:
(1)Fe的基态原子共有____种不同能级的电子。
(2)已知高温下CuO→Cu2O+O2,从铜原子价层电子结构(3d和4s轨道上应填充的电子数)变化角度来看,能生成Cu2O的原因是___。比较铁与锰的第三电离能(I3):铁__锰(填“>”、 “=”或“<”),原因是___。
(3)某含铜化合物的离子结构如图所示。

①该离子中存在的作用力有______________;
a.离子键 b.共价键 c.配位键 d.氢键 e.范德华力
②该离子中N原子的杂化类型有____________。
(4)如图是晶体Fe3O4的晶胞,该晶体是一种磁性材料,能导电。
①晶胞中二价铁离子处于氧离子围成的______(填空间结构)空隙。
②晶胞中氧离子的堆积方式与某金属晶体原子堆积方式相同,该堆积方式名称为________。
③解释Fe3O4晶体能导电的原因__________;若晶胞的体对角线长为anm,则 Fe3O4 晶体的密度为______g·cm-3(阿伏加德罗常数用NA表示)。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】高锰酸钾可以通过电解法进行制备,装置如图所示,下列说法错误的是
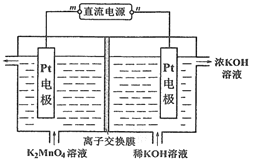
A. 阳极的电极反应式:MnO42- – e-= MnO4-
B. 该装置的离子交换膜为阳离子交换膜
C. 当电路通过a mol电子时,阴极室电解质溶液增加2a mol离子
D. 若电解流出液中KMnO4、K2MnO4和KOH物质的量之比为a∶b∶c,则流进电解池的电解液中K2MnO4和KOH的物质的量之比为 (a + b)∶( c + a )
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】菱锰矿的主要成分是MnCO3,还含有少量Fe、Al、Ca、Mg等元素。氯化铵焙烧菱锰矿制备高纯度碳酸锰的工艺流程如下:

已知:①相关金属离子[c0(Mn+)=0.1 mol/L]形成氢氧化物沉淀的pH范围如下:
金属离子 | Al3+ | Fe3+ | Fe2+ | Ca2+ | Mn2+ | Mg2+ |
开始沉淀的pH | 3.8 | 1.5 | 6.3 | 10.6 | 8.8 | 9.6 |
沉淀完全的pH | 5.2 | 2.8 | 8.3 | 12.6 | 10.8 | 11.6 |
②常温下,CaF2、MgF2的溶度积常数分别为1.46×10-10、 7.42×10-11
回答下列问题:
(1) “焙烧”时发生的主要反应的化学方程式为__________。气体X为________(填化学式),写出它生活中的一种用途_______________。
(2)焙烧时温度对锰浸出率的影响如图所示。焙烧时适应温度为_______________。

(3)浸出液“净化除杂”过程如下:首先用MnO2将Fe2+氧化为Fe3+,再调节溶液的pH将Al3+、Fe3+变成沉淀除去,溶液的pH的范围为____然后加入NH4F将Ca2+、Mg2+转化为CaF2、MgF2沉淀除去,两种沉淀共存时,溶液中![]() =________(所得结果保留两位小数)。
=________(所得结果保留两位小数)。
(4)碳化结晶的原理(用离子方程式表示): ______________________。
(5)将制得的高纯度碳酸锰溶于过量稀硫酸后用惰性电极电解,在某极得到重要的无机功能材料MnO2,该电极的电极反应式为_________。
(6)在该工艺流程中可以循环使用的物质有__________。(填化学式)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】化合物H可用于制备树脂、塑料和涂料等。其合成路线如下图所示:

已知:R—CH=CH2![]() RCH2CH2OH(其中B2H6为乙硼烷)
RCH2CH2OH(其中B2H6为乙硼烷)
请回答下列问题:
(1) 11.2 L(标准状况)的烃A在氧气中充分燃烧可以生成88 g CO2和45 g H2O。A的分子式是____________________。
(2)B和C在氢氧化钠的醇溶液中加热得到的有机物只有一种结构。B和C均为一氯代烃,它们的名称(系统命名)分别为_____________、_____________。
(3)在催化剂存在下1 mol F与2 mol H2反应,生成2甲基1丙醇。F的结构简式是_________________。其含有的官能团名称是_______________________。
(4)B→D,C→D的反应类型均为___________。请任写一个化学方程式_________________。
(5)写出F→G的化学方程式______________________________________________。
(6)写出E+G→H的化学方程式___________________________________________。
(7)写出与G具有相同官能团的G的所有同分异构体的结构简式_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温条件下,分别将SO2通入100mL(NH4)2SO3溶液、100mLNaOH溶液中,测得溶液pH与各组分物质的量分数的变化关系如图和如图,已知Kb(NH3·H2O)=1.8×10-5,下列说法不正确的是( )

图1:SO2通入(NH4)2SO3溶液中

图2:SO2通入NaOH溶液中
A. b点n(NH4+):n(HSO3-)=3:1
B. 由图1可得Ka1(H2SO3)=10-2,Ka2(H2SO3)=10-7
C. 图2中,b点溶液呈中性
D. 由图2可得NaOH溶液的浓度为10mol/L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com