
ĻĀĮŠĖµ·Ø»ņ±ķŹ¾·½·ØÕżČ·µÄŹĒ
A£®µČĮæµÄ°×Į×ÕōĘųŗĶ°×Į×¹ĢĢå·Ö±šĶźČ«Č¼ÉÕ£¬ŗóÕ߷ųöČČĮæ¶ą
B£®ŅŃÖŖ£ŗC(s£¬ŹÆÄ«)=C(s£¬½šøÕŹÆ) ”÷H=1.5kJ/mol£¬Ōņ½šøÕŹÆ±ČŹÆÄ«ĪȶØ
C£®ŌŚ101kPaŹ±£¬2g H2ĶźČ«Č¼ÉÕÉś³ÉŅŗĢ¬Ė®£¬·Å³ö285.8kJČČĮ棬ĒāĘųČ¼ÉÕµÄČČ»Æѧ·½³ĢŹ½±ķŹ¾ĪŖ£ŗ2H2(g)+O2(g)£½2H2O(l) ¦¤H=£285£®8kJ/mol
D£®ŌŚĻ”ČÜŅŗÖŠ£ŗ£Č+(aq)+OH-(aq)£½H2O(l) ¦¤H=£57.3kJ/mol£¬Čō½«ŗ¬1m olCH3COOHÓėŗ¬
olCH3COOHÓėŗ¬
£±mol NaOHµÄČÜŅŗ»ģŗĻ£¬·Å³öµÄČČĮæŠ”ÓŚ57.3kJ

| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğøŹĖąŹ”ø߶žÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
°ŃĆŗ×÷ĪŖČ¼ĮĻæÉĶعżĻĀĮŠĮ½ÖÖĶ¾¾¶£ŗ
Ķ¾¾¶I£ŗC(s)+O2(g)==CO2(g) ”÷H1<0¢Ł
Ķ¾¾¶II£ŗĻČÖĘ³ÉĖ®ĆŗĘų£ŗC(s)+H2O(g)==CO(g)+H2(g) ”÷H2>0¢Ś
ŌŁČ¼ÉÕĖ®ĆŗĘų£ŗ2CO(g)+O2(g)==2CO2(g) ”÷H3<0¢Ū
2H2(g)+O2(g)==2H2O(g) ”÷H4<0¢Ü
Ēė»Ų“šĻĀĮŠĪŹĢā:
£Ø1£©Ķ¾¾¶I·Å³öµÄČČĮæ ( Ģī”°“óÓŚ”±”°µČÓŚ”±»ņ”°Š”ÓŚ”±) Ķ¾¾¶II·Å³öµÄČČĮ攣
£Ø2£©”÷H1”¢”÷H2”¢”÷H3”¢”÷H4µÄŹżŃ§¹ŲĻµŹ½ŹĒ ”£
£Ø3£©12g Ģæ·ŪŌŚŃõĘųÖŠ²»ĶźČ«Č¼ÉÕÉś³ÉŅ»Ńõ»ÆĢ¼£¬·Å³ö110.35kJČČĮ攣ĘäČČ»Æѧ·½³ĢŹ½ĪŖ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğø£½ØŹ”øßŅ»ÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
·Ē½šŹōäåÓėĀČĘųµÄŠŌÖŹŗÜĻąĖĘ”£ŌŚĢ½¾æäåµ„ÖŹµÄŠŌÖŹŹ±£¬Ę仳±¾³ĢŠņÓ¦øĆŹĒ
A£®×öŹµŃé²¢¹Ū²ģŹµŃéĻÖĻ󔜷ÖĪö”¢½āŹĶ£¬ µĆ³ö½įĀŪ
µĆ³ö½įĀŪ
B£®¹Ū²ģäåµÄĶā¹ŪŠŌÖŹ”ś×öŹµŃé²¢¹Ū²ģŹµŃéĻÖĻ󔜷ÖĪö”¢½āŹĶ£¬µĆ³ö½įĀŪ
C£®¹Ū²ģäåµÄĶā¹ŪŠŌÖŹ”śŌ¤ ²āäåµÄ»ÆѧŠŌÖŹ”ś×öŹµŃé²¢¹Ū²ģŹµŃéĻÖĻ󔜷ÖĪö”¢½āŹĶ£¬µĆ³ö½įĀŪ
²āäåµÄ»ÆѧŠŌÖŹ”ś×öŹµŃé²¢¹Ū²ģŹµŃéĻÖĻ󔜷ÖĪö”¢½āŹĶ£¬µĆ³ö½įĀŪ
D£®Ō¤²āäåµÄŠŌÖŹ”ś×öŹµŃé²¢¹Ū²ģŹµŃéĻÖĻ󔜷ÖĪö”¢½āŹĶ£¬µĆ³ö½įĀŪ”ś¹Ū²ģäåµÄĶā¹ŪŠŌÖŹ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğø£½ØŹ”ø߶žÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
»Æѧ·“Ó¦N2+3H2 2NH3µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ŹĒ
2NH3µÄÄÜĮæ±ä»ÆČēĶ¼ĖłŹ¾£¬øĆ·“Ó¦µÄČČ»Æѧ·½³ĢŹ½ŹĒ

A£®N2(g)+3H2(g) 2NH3(l)”÷H=2(a©b©c)kJ/mol
2NH3(l)”÷H=2(a©b©c)kJ/mol
B£®N2(g)+3H2(g) 2NH3(g)”÷H=2(b©a)kJ/m
2NH3(g)”÷H=2(b©a)kJ/m ol
ol
C£®0.5N2(g)+1.5H2(g) NH3(l)”÷H=(b+c©a)kJ/mol
NH3(l)”÷H=(b+c©a)kJ/mol
D£®0.5N2(g)+1.5H2(g) NH3(g)”÷H=(a+b)kJ/mol
NH3(g)”÷H=(a+b)kJ/mol
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğø£½ØŹ”ø߶žÉĻµŚŅ»“ĪŌĀæ¼»Æѧ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
Ä³Ń§ÉśÓūĶź³É2HCl+2AgØT2AgCl+H2”ü·“Ó¦£¬Éč¼ĘĮĖĻĀĮŠĖÄøöŹµŃ飬ÄćČĻĪŖæÉŠŠµÄŹµŃéŹĒ
A£® B£® C£® D£®
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģɽ¶«Ź”ŠĀĢ©ŹŠøßČżÉĻѧʌµŚŅ»“Ī½×¶Īæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
1 Lij»ģŗĻČÜŅŗ£¬æÉÄÜŗ¬ÓŠµÄĄė×ÓČē±ķĖłŹ¾£ŗ
æÉÄÜ“óĮæŗ¬ÓŠµÄŃōĄė×Ó | K£«”¢Mg2£«”¢Al3£«”¢NH4£«”¢Fe2£«”¢Fe3£«”¢Cu2£«”¢Ba2£« |
æÉÄÜ“óĮæŗ¬ÓŠµÄŅõĄė×Ó | Cl£”¢Br£”¢I£”¢ |
£Ø1£©øł¾ŻĻĀĮŠŹµŃé²½ÖčŗĶĻÖĻó£¬ĶʶĻŹµŃé½įĀŪ
ŹµŃé²½ÖčÓėŹµŃéĻÖĻó | ŹµŃé½įĀŪ |
¢ń£®¹Ū²ģČÜŅŗ£ŗĪŽÉ«ĶøĆ÷ | ¢ŁŌČÜŅŗÖŠŅ»¶Ø²»ŗ¬µÄĄė×ÓŹĒ_________ |
¢ņ£®Č”ŹŹĮæøĆČÜŅŗ£¬¼ÓČė¹żĮæµÄNaOHČÜŅŗ£¬ÓŠĘųĢåÉś³É£¬²¢µĆµ½ĪŽÉ«ČÜŅŗ | ¢ŚŌČÜŅŗÖŠŅ»¶Øŗ¬ÓŠµÄĄė×ÓŹĒ_________£¬Ņ»¶Ø²»ŗ¬µÄĄė×ÓŹĒ_________ |
¢ó£®ŌŚ¢ņĖłµĆČÜŅŗÖŠŌŁÖšµĪ¼ÓČė¹żĮæµÄNaHSO4ČÜŅŗ£¬ĻČÉś³É°×É«³Įµķ£¬Č»ŗó³Įµķ²æ·ÖČܽā£¬×īŗóµĆ°×É«³ĮµķA”£ | ¢ŪŌČÜŅŗÖŠ»¹Ņ»¶Øŗ¬ÓŠµÄĄė×ÓŹĒ________£¬Éś³É³ĮµķAµÄĄė×Ó·½³ĢŹ½ĪŖ______________ |
£Ø2£©¾¼ģ²ā£¬øĆČÜŅŗÖŠ»¹ŗ¬ÓŠ“óĮæµÄCl£”¢Br£”¢I££¬ČōĻņ1 LøĆ»ģŗĻČÜŅŗÖŠĶØČėŅ»¶ØĮæµÄCl2£¬ČÜŅŗÖŠCl£”¢Br£”¢I£µÄĪļÖŹµÄĮæÓėĶØČėCl2µÄĢå»ż(±ź×¼×“æö)µÄ¹ŲĻµČē±ķĖłŹ¾£¬·ÖĪöŗó»Ų“šĻĀĮŠĪŹĢā£ŗ
Cl2µÄĢå»ż(±ź×¼×“æö) | 2£®8 L | 5£®6 L | 11£®2 L |
n(Cl£) | 1£®25 mol | 1£®5 mol | 2 mol |
n(Br£) | 1£®5 mol | 1£®4 mol | 0£®9 mol |
n(I£) | a mol | 0 | 0 |
¢Łµ±ĶØČėCl2µÄĢå»żĪŖ2£®8 LŹ±£¬ČÜŅŗÖŠ·¢Éś·“Ó¦µÄĄė×Ó·½³ĢŹ½ĪŖ_______________________”£
¢ŚŌČÜŅŗÖŠCl£”¢Br£”¢I£µÄĪļÖŹµÄĮæÅضČÖ®±ČĪŖ_________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģɽ¶«Ź”ŠĀĢ©ŹŠøßČżÉĻѧʌµŚŅ»“Ī½×¶Īæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
ĻņNa2CO3”¢NaHCO3»ģŗĻČÜŅŗÖŠÖšµĪ¼ÓČėĻ”ŃĪĖį£¬Éś³ÉĘųĢåµÄĮæĖęŃĪĖį¼ÓČėĮæµÄ±ä»Æ¹ŲĻµČēÓŅĶ¼ĖłŹ¾”£ŌņĻĀĮŠĄė×Ó×éŌŚ¶ŌÓ¦µÄČÜŅŗÖŠŅ»¶ØÄÜ“óĮæ¹²“ęµÄŹĒ
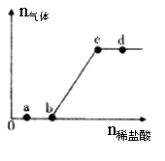
A£®aµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗNa+”¢OH-”¢SO42-”¢NO3-
B£®bµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗAl3+”¢Fe3+”¢MnO4-”¢Cl-
C£®cµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗNa+”¢Ca2+”¢NO3-”¢Cl-
D£®dµć¶ŌÓ¦µÄČÜŅŗÖŠ£ŗF-”¢NO3-”¢Fe2+”¢Ag+
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2017½ģɽ¶«Ź”øßĆÜŹŠøßČżÉĻѧʌ10ŌĀĶ³æ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗĢīæÕĢā
ŃŠ¾æ·¢ĻÖ£¬ŗ¬pm2£®5µÄĪķö²Ö÷ŅŖ³É·ÖÓŠSO2”¢NOx”¢CxHy¼°æÉĪüČėæÅĮ£µČ”£
£Ø1£©Īķö²ÖŠÄÜŠĪ³ÉĖįÓźµÄĪļÖŹŹĒ_____________”£
£Ø2£©ĪŖĻū³żNOx¶Ō»·¾³µÄĪŪČ¾£¬æÉĄūÓĆNH3ŌŚŅ»¶ØĢõ¼žĻĀÓėNO·“Ӧɜ³ÉĪŽĪŪČ¾µÄĘųĢ唣
ŅŃÖŖ£ŗ4NH3(g)+5O2(g) 4NO(g)+6H2O(g) ”÷H = -905£®48 kJ”¤mol£1
4NO(g)+6H2O(g) ”÷H = -905£®48 kJ”¤mol£1
N2(g)+O2(g) 2NO(g) ”÷H = +180£®50 kJ”¤mol£1
2NO(g) ”÷H = +180£®50 kJ”¤mol£1
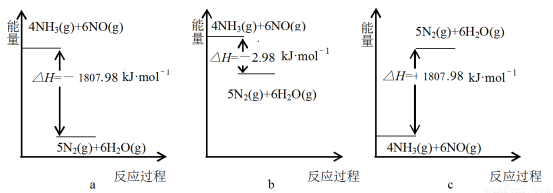
¢ŁĻĀĮŠ±ķŹ¾NH3(g)ÓėNO(g)ŌŚŅ»¶ØĢõ¼žĻĀ·“Ó¦£¬Éś³ÉĪŽĪŪČ¾ĘųĢåµÄÄÜĮæ×Ŗ»Æ¹ŲĻµŹ¾ŅāĶ¼ÕżČ·µÄŹĒ£ŗ___________(Ģī×ÖÄø)
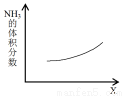
¢Ś ÓŅĶ¼ŹĒ·“Ó¦4NH3(g)+6NO(g) 5N2(g)+6H2O(g)¹ż³ĢÖŠNH3µÄĢå»ż·ÖŹżĖęX±ä»ÆµÄŹ¾ŅāĶ¼£¬X“ś±ķµÄĪļĄķĮææÉÄÜŹĒ_________£¬ŌŅņŹĒ_________”£
5N2(g)+6H2O(g)¹ż³ĢÖŠNH3µÄĢå»ż·ÖŹżĖęX±ä»ÆµÄŹ¾ŅāĶ¼£¬X“ś±ķµÄĪļĄķĮææÉÄÜŹĒ_________£¬ŌŅņŹĒ_________”£
£Ø3£©ČēĶ¼µē½ā×°ÖĆæɽ«Īķö²ÖŠµÄSO2”¢NO×Ŗ»ÆĪŖ(NH4)2SO4£¬
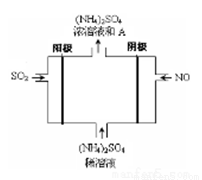
¢Ł Ņõ¼«µÄµē¼«·“Ó¦Ź½ŹĒ ”£
¢Ś ĪļÖŹAŹĒ_____________(Ģī»ÆѧŹ½)£¬ĄķÓÉŹĒ_________________________”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ2016-2017ѧğĮÉÄžŹ”ø߶žÉĻµŚŅ»“ĪŌĀæ¼»ÆѧŹŌ¾ķ£Ø½āĪö°ę£© ĢāŠĶ£ŗŃ”ŌńĢā
pH=13µÄĒæ¼īČÜŅŗÓėpH=2µÄĒæĖįČÜŅŗ»ģŗĻ£¬ĖłµĆČÜŅŗµÄpH=11,ŌņĒæ¼īÓėĒæĖįµÄĢå»ż±Č£Ø £©
A.11£ŗ1 B.9 £ŗ1 C.1 £ŗ11 D.1 £ŗ9
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com