
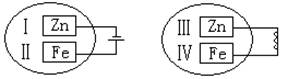


科目:高中化学 来源: 题型:阅读理解
| ||
| ||
查看答案和解析>>
科目:高中化学 来源:2011-2012学年甘肃省天水市一中高二上学期期末考试化学试卷 题型:单选题
把锌片和铁片放在盛有食盐水和酚酞的表面皿中,如图所示。
最先观察到酚酞变红的现象的区域是
| A.I和III | B.I和IV |
| C.II和III | D.II和IV |
查看答案和解析>>
科目:高中化学 来源:2013届甘肃省张掖二中高三10月月考化学试卷(奥班)(带解析) 题型:单选题
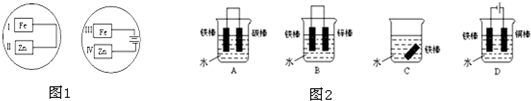
把锌片和铁片放在盛有稀食盐水和酚酞试液混合溶液的玻璃皿中(如图所示平面图),经过一段时间后,两个实验中,首先观察到溶液变红的区域是( )
| A.Ⅰ和Ⅲ附近 | B.Ⅰ和Ⅳ附近 | C.Ⅱ和Ⅲ附近 | D.Ⅱ和Ⅳ附近 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com