
| KCl | K2SO4 | ZnSO4 | ZnCl2 | |
| (1) | 0.3mol | 0.2mol | 0.1mol | - |
| (2) | 0.1mol | 0.3mol | - | 0.2mol |
| A. | Cl-的物质的量相同 | B. | SO42-的数目相同 | ||
| C. | K+的数目相同 | D. | Zn2+的物质的量不同 |
分析 体积相同的溶液,离子的物质的量浓度与离子的物质的量有关,离子的物质的量相同,物质的量浓度也相同;求出两份营养液中各种离子的物质的量,进而判断离子的物质的量浓度的关系.
第一份营养液中:n(K+)=0.3mol+0.2mol×2=0.7mol,n(SO42-)=0.2mol+0.1mol=0.3mol,n(Zn2+)=0.1mol,
n(Cl-)=0.3mol;
第二份营养液中:n(K+)=0.1mol+0.3mol×2=0.7mol,n(SO42-)=0.3mol,n(Zn2+)=0.2mol,
n(Cl-)=0.1mol+0.2mol×2=0.5mol;
两份营养液中离子浓度不完全相同.
解答 解:A、第一份营养液中,n(Cl-)=0.3mol;第二份营养液中,n(Cl-)=0.1mol+0.2mol×2=0.5mol,故A错误;
B、第一份营养液中,n(SO42-)=0.2mol+0.1mol=0.3mol;第二份营养液中,n(SO42-)=0.3mol,故B正确;
C、第一份营养液中,n(K+)=0.3mol+0.2mol×2=0.7mol,第二份营养液中:n(K+)=0.1mol+0.3mol×2=0.7mol,故C正确;
D、第一份营养液中,n(Zn2+)=0.1mol,第二份营养液中,n(Zn2+)=0.2mol,故D正确.
故选A.
点评 本题考查体积相同的溶液中离子浓度的关系,要知道离子浓度大小与离子的物质的量有关,离子的物质的量相同,物质的量浓度也相同.


 新课标同步训练系列答案
新课标同步训练系列答案 一线名师口算应用题天天练一本全系列答案
一线名师口算应用题天天练一本全系列答案科目:高中化学 来源: 题型:解答题

查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 分子总数为NA的NO2和CO2混合气体中含有的氧原子数为2NA | |
| B. | 28g乙烯(C2H4)和环丁烷(C4H8)的混合气体中含有的碳原子数为2NA | |
| C. | 常温常压下,92g的NO2和N2O4混合气体含有的原子总数为6NA | |
| D. | 17gOH-中含有的质子数为10NA |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
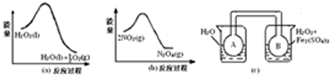
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 金属的活泼顺序为:a>c>b>d | |
| B. | 在①的溶液中,SO42-向b极移动 | |
| C. | 在③的装置中,一段时间后b电极质量将会减轻 | |
| D. | 二次电池放电时的反应和充电时的反应是可逆反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| KCl | K2SO4 | ZnSO4 | ZnCl2 | |
| (1) | 0.3mol | 0.2mol | 0.1mol | / |
| (2) | 0.1mol | 0.3mol | / | 0.1mol |
| A. | 完全相同 | B. | 完全不同 | C. | 仅c(K+)相同 | D. | 仅c(Cl-)相同 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 陈述Ⅰ | 陈述Ⅱ |
| A | 氢氟酸具有酸性 | 氢氟酸可用于雕刻玻璃 |
| B | 氯水显酸性 | 可用pH试纸测氯水的pH |
| C | NH3极易溶于水 | NH3可用作制冷剂 |
| D | ClO2具有强氧化性 | ClO2可用于自来水的杀菌消毒 |
| A. | A、 | B. | B、 | C. | C、 | D. | D、 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com