
【题目】已知:①甲醛(HCHO)与葡萄糖化学性质相似,都具有还原性。②甲醛易挥发,甲酸钙易溶于水。为探究过量的甲醛和新制Cu(OH)2反应的产物,进行如下实验:
(1)在下图装置中进行实验,向a中加入0.5mol·L-1CuSO4溶液50mL和5mol·L-1NaOH 溶液100mL,振荡,再加入40%的甲醛溶液50mL,缓慢加热20分钟后冷却至室温。

仪器a、b的名称分别是________________、_______________。
(2)上述实验有副反应发生,产生的气体为CO、H2中的一种或两种。为确认气体成分,将装置A 和如下图所示装置连接后进行实验。

依次连接的合理顺序为A→____→____→____→____→____→G。副产物中如果有CO,实验现象是:_____________________________________。
(3)已知HCHO 最终被氧化为CO32-,请写出a容器中发生的反应化学方程式:_________________________________________。
(4)反应后a中有红色固体产生,为探究其组成,提出如下假设:
假设一:只有Cu2O 假设二:只有Cu
假设三:CuO和Cu 假设四:_______________;
其中假设三明显不成立,理由是___________________________________。
(5)为了对(4)的猜想进行验证,进行如下实验(以下任步均充分反应):
已知:已知:Cu2O ![]() [Cu(NH3)4]+(无色)
[Cu(NH3)4]+(无色)![]() [Cu(NH3)4]2+ (蓝色)
[Cu(NH3)4]2+ (蓝色)
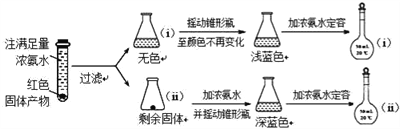
①锥形瓶ii中固体加入浓氨水后,完全溶解得到深蓝色溶液,该过程所发生的离子方程式为 __________________________________________;
②将容量瓶ii中的溶液稀释20倍后,溶液的颜色与容量瓶i相近。由此可知固体产物的组成及物质的量之比约为_________________________________。
【答案】 三颈烧瓶 (恒压)滴液漏斗 BEFDC F中黑色固体变红色,C中变浑浊(出现白色沉淀) HCHO+4Cu(OH)2+2NaOH→Na2CO3+2Cu2O↓+6H2O Cu2O和Cu CuO为黑色固体 2Cu+O2+8NH3·H2O ===2[Cu(NH3)4]2++4OH-+6H2O n(Cu2O) ∶n(Cu)=1︰40
【解析】(1) 仪器a为三颈烧瓶;仪器b为滴液漏斗;正确答案:三颈烧瓶;滴液漏斗。
(2)甲醛易挥发, 产生的气体CO、H2中含有挥发出的甲醛,因此混合气体先通入B装置除去甲醛,然后用E装置进行气体干燥,干燥后的混合气体进入F装置,与氧化铜加热反应,产生的气体进入D装置,进行水蒸气的检验,剩余气体最后进入G装置;连接合理顺序为BEFDC;一氧化碳还原氧化铜观察到现象:F中黑色固体变红色,C中变浑浊(出现白色沉淀);正确答案: BEFDC;F中黑色固体变红色,C中变浑浊(出现白色沉淀)。
(3)已知HCHO最终被氧化为CO32-,Cu(OH)2被还原为Cu2O;反应化学方程式为:HCHO+4Cu(OH)2+2NaOH→Na2CO3+2Cu2O↓+6H2O;正确答案:HCHO+4Cu(OH)2+2NaOH→Na2CO3+2Cu2O↓+6H2O。
(4)假设四为Cu2O和Cu的混合物;假设三中,CuO为黑色固体,不符合题意;正确答案:Cu2O和Cu ; CuO为黑色固体。
(5)①锥形瓶ii中固体铜与浓氨水、氧气共同作用,生成深蓝色溶液[Cu(NH3)4]2+,该过程所发生的离子方程式为2Cu+O2+8NH3·H2O ==2[Cu(NH3)4]2++4OH-+6H2O;正确答案:2Cu+O2+8NH3·H2O ==2[Cu(NH3)4]2++4OH-+6H2O。
②由上述反应过程可知固体产物的组成Cu2O和Cu;根据反应关系:容量瓶i中Cu2O→2[Cu(NH3)4]2+;容量瓶ii中2Cu→2[Cu(NH3)4]2+,将容量瓶ii中溶液稀释20倍等于容量瓶i中溶液的浓度,即两瓶溶液中c[Cu(NH3)4]2+ 相等,所以锥形瓶ii中Cu的量为Cu2O的40倍;正确答案:n(Cu2O) ∶n(Cu)=1︰40。


科目:高中化学 来源: 题型:
【题目】据报道,中国的科学家将C60分子组装在一单层分子膜表面,在﹣268℃时冻结分子的热振荡,并利用扫描隧道显微镜首次“拍摄”到能清楚分辨碳原子间单、双键的分子图象.下列化合物分子中一定既含单键又含双键的是( )
A.CO2 B.COCl2 C.C2H4O D.H2O2
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】室温下,用0.200mol·L-1NaOH溶液分别滴定20.0mL0.200 mol·L-1的盐酸和醋酸,滴定曲线如图所示。下列说法正确的是

A. Ⅱ表示的是滴定醋酸的曲线
B. pH=7时,滴定醋酸消耗的V(NaOH)小于20mL
C. V(NaOH)=20.00mL时,两份溶液中c(Cl-)=c(CH3COO-)
D. V(NaOH)=10.00mL时,醋酸溶液中c(Na+)>c(CH3COO-)> c(OH-)> c(H+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】CH4﹣O2燃料电池具有放电稳定,无污染等优点,如图为一用甲烷氧气燃料电池电解饱和氯化钠溶液的模型图。请认真读图,回答以下问题:
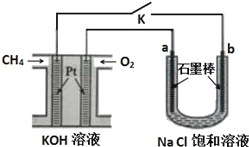
(1)请写出通入甲烷气体的一极所发生的电极反应式:____________________,其附近的pH值___(填“不变”或“变大”或“变小”)
(2)如果通入1mol的甲烷完全参与电极反应,则电路中转移_____________的电子,a电极产生的气体在标准状况下的体积为_________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列有关钠和镁的说法中正确的是( )
A.金属钠在氧气中燃烧可以生成氧化钠
B.金属钠在高温下能将TiCl4溶液中的钛置换出来
C.工业上用电解熔融氧化镁制取金属镁
D.金属镁燃烧后会发出耀眼的白光,因此常用来制造信号弹和焰火
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】氯化钠样品中含有少量的杂质Na2SO4,按下列流程进行净化,流程中的( )中是合适的试剂,在[ ]中是实验操作名称。写出有关反应的化学方程式:

(1)操作①、②、③、⑤中所需加入试剂分别为_______、______、______、_____。
(2)操作①、④、⑥的操作名称分别为_________、_______、_______。
(3)写出有关的离子反应方程式:
第②步:_____________________________。
第⑤步:_____________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铁及其化合物在有机化学中应用广泛,例如有机合成中,常用铁和盐酸将硝基(﹣NO2)还原为氨基(﹣NH2);在苯的溴代反应中用溴化铁作催化剂。
(1)N的原子结构示意图为_______,Fe基态原子核外电子排布式为_______。
(2)H、N、O 的电负性从小到大的顺序是_______。
(3)与NO2+互为等电子体的一种分子为_____(填化学式),氨基(﹣NH2)中氮原子的杂化类型为_____。
(4)1mol苯分子中含有σ键的物质的量为______。
(5)Fe 与 N 形成的某化合物晶胞如图所示,则该晶体的化学式为_______。

查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图所示与对应叙述不相符的是( )




A. 图甲表示一定温度下FeS和CuS的沉淀溶解平衡曲线,则Ksp(FeS)>Ksp(CuS)
B. 图乙表示pH=2的甲酸与乙酸溶液稀释时的pH变化曲线,则酸性:甲酸<乙酸
C. 25℃时,图丙表示用0.100mol·L-1的NaOH溶液滴定25.00mL盐酸的滴定曲线,则c(HCl)=0.080mol·L-1
D. 图丁表示反应N2(g)+3H2(g)![]() 2NH3(g)平衡时NH3体积分数随起始
2NH3(g)平衡时NH3体积分数随起始![]() 变化的曲线,则转化率:aA(H2)<aB(H2)
变化的曲线,则转化率:aA(H2)<aB(H2)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一种熔融碳酸盐燃料电池原理示意如图。下列有关该电池的说法正确的是( )

A. 反应CH4+H2O![]() 3H2+CO,每消耗1molCH4转移8mol电子
3H2+CO,每消耗1molCH4转移8mol电子
B. 电极A上H2参与的电极反应为:H2+CO32--2e-=H2O+CO2
C. 电池工作时,CO32-向电极B移动
D. 用电器上每通过4mol电子,电极B上参加反应的O2为22.4L
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com