
金刚石和石墨是碳元素的两种结构不同的单质(同素异形体)。100Kpa,1mol石墨转化成金刚石需要吸热1.895KJ。据此,试判断在100Kpa压强下,下列结论正确的为:
A.金刚石比石墨稳定
B.1mol石墨比lmol金刚石总能量高
C.1mol金刚石比1mol石墨总能量高,
D.破坏1mol金刚石中的共价键消耗能量比石墨多
科目:高中化学 来源: 题型:阅读理解
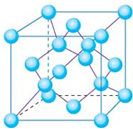 碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.
碳元素不仅能形成丰富多彩的有机化合物,而且还能形成多种无机化合物,同时自身可以形成多种单质,碳及其化合物的用途广泛.| 2880 |
| NA |
| 2880 |
| NA |
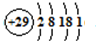
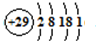
| ||
| 4 |
| 3 |
| ||
| ||
| 4 |
| 3 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、1mol石墨比1mol金刚石的总能量高 | B、在100kpa时石墨比金刚石稳定 | C、金刚石和石墨是碳元素的两种同位素 | D、破坏1mol金刚石和1mol石墨中的化学键所吸收的能量前者大于后者 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 物质的结构决定性质,性质反映其结构特点.
物质的结构决定性质,性质反映其结构特点.
| ||
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com