
A��B��X��Y��H2O(δ��ƽ����Ӧ������ȥ)����ѧ������Ӧ�Ļ�ѧ����ʽ������A��B�����ʵ���֮��Ϊ1��4����ش�
(1)��Y�ǻ���ɫ���壬��÷�Ӧ�����ӷ���ʽ��________��
(2)��AΪ�ǽ������ʣ���������ԭ�Ӻ��������������Ǵ�����������2����B����ҺΪijŨ�ᣬ��Ӧ���������뻹ԭ�������ʵ���֮����________��
(3)��AΪ�������ʣ�������A��B��Ũ��Һ�С��ۻ�������A������X��Һ��
��AԪ�������ڱ��е�λ����________������Y�Ļ�ѧʽ��________��
�ں�a molX����Һ�ܽ���һ����A������Һ�����ֽ��������ӵ����ʵ���ǡ����ȣ���ԭ��X�����ʵ���Ϊ________mol��
(4)��A��B��X��Y��Ϊ�����A����ˮ������Ľ���������ˮ���������ɾ���ˮ����A��Һ�м��������ữ��AgNO3��Һ��������ɫ������B����ɫΪ��ɫ����A��B�����ʵ���֮��1��4ǡ�÷�Ӧ��������ҺΪ��ɫʱ������Һ������Ũ�ȴӴ�С��˳����________��

| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| ||
| ||
 Fe2++Ag+����ش��������⣺
Fe2++Ag+����ش��������⣺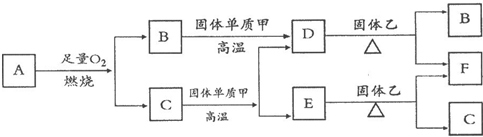
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��Ķ�����
| Ԫ�� | �����Ϣ |
| X | ��ɵ����ʵĻ���Ԫ�أ�����������ϼ���������ϼ۵Ĵ�����Ϊ2 |
| Y | �ؿ��к�����ߵ�Ԫ�� |
| Z | ����������Ϊ23��������Ϊ11�ĺ��� |
| W | �����д���ʹ����Ͻ���Ʒ����ҵ�Ͽ��õ������������ķ����Ʊ��䵥�� |
| R | �ж��ֻ��ϼۣ����ɫ���������ڿ����л�Ѹ�ٱ�ɻ���ɫ������ɺ��ɫ |




�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�

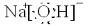
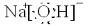
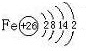
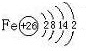
| ||
| ||
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A.X��Z��Y��M B.X��Y��Z��M C.M��Z��X��Y D.X��Z��M��Y
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
A.X��Z��Y��M B.X��Y��Z��M
C.M��Z��X��Y D.X��Z��M��Y
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com