
| A、金属易锈蚀能用金属的电子气理论加以解释 |
| B、化学式Si02能真实表示物质分子组成 |
| C、共价键、离子键和范德华力都是微粒之间的不同作用力,Na2O2、石墨、白磷均含有上述两种作用力 |
| D、CCl4与KCl晶体中,化学键种类相同,晶体类型也相同 |


科目:高中化学 来源: 题型:
| A、通入稀有气体使压强增大,平衡将逆向移动 |
| B、C的正反应速率是A的逆反应速率的3倍 |
| C、降低温度,混合气体的平均相对分子质量减小 |
| D、移走部分C,C的体积分数减小 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图表示反应X(g)+Y(g)?Z(g);△H<0,从时间0~t3s的变化,则t2~t3时间段的变化是由下列哪项条件的改变引起的( )
如图表示反应X(g)+Y(g)?Z(g);△H<0,从时间0~t3s的变化,则t2~t3时间段的变化是由下列哪项条件的改变引起的( )| A、升高温度 |
| B、迅速缩小容器体积 |
| C、增大X的浓度 |
| D、增大Y的浓度 |
查看答案和解析>>
科目:高中化学 来源: 题型:
 如图所示,把电极Al、Mg插入C的溶液中设计原电池.
如图所示,把电极Al、Mg插入C的溶液中设计原电池.查看答案和解析>>
科目:高中化学 来源: 题型:
 如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:
如图为实验室某浓盐酸试剂瓶上的标签,试根据有关数据回答下列问题:| 1000Vd |
| 36.5V+2240 |
| Vd |
| 36.5V+2240 |
| 1000d |
| 36.5V+22.4 |
| 36.5V |
| 22.4(V+1)d |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、18g | B、180g |
| C、198g | D、162g |
查看答案和解析>>
科目:高中化学 来源: 题型:
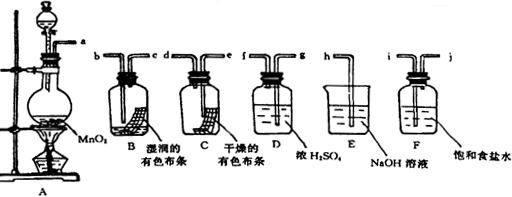
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com