
| 压强/MPa 转化率/% 温度/℃ | 0.1 | 0.5 | 1 | 10 |
| 400 | 99.2 | 99.6 | 99.7 | 99.9 |
| 500 | 93.5 | 96.9 | 97.8 | 99.3 |
| 600 | 73.7 | 85.8 | 89.5 | 96.4 |


科目:高中化学 来源: 题型:
| A、熔点:邻羟基苯甲醛>对羟基苯甲醛 |
| B、酸性:H2SO4>H2CO3>HCO3->Al(OH)3 |
| C、溶解度:Na2CO3>NaHCO3>MgCO3 |
| D、稳定性:Na2CO3>NaHCO3>H2CO3 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、糖类、油脂、蛋白质都能发生水解反应 |
| B、淀粉水解的最终产物能发生银镜反应 |
| C、蛋白质溶液中加入饱和硫酸铵溶液后产生的沉淀能重新溶于水 |
| D、脂肪能发生皂化反应,生成甘油和高级脂肪酸盐 |
查看答案和解析>>
科目:高中化学 来源: 题型:
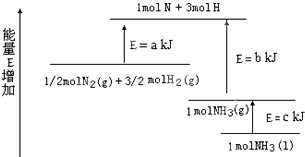
查看答案和解析>>
科目:高中化学 来源: 题型:
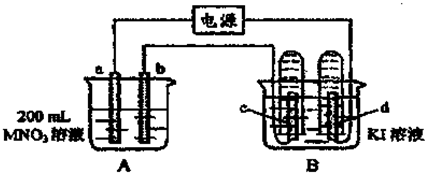
查看答案和解析>>
科目:高中化学 来源: 题型:
 (1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是
(1)事实证明,能设计成原电池的反应通常是放热反应,下列化学反应在理论上可以设计成原电池的是查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
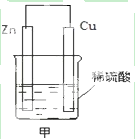 能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.阅读下列有关能源的材料,回答有关问题:
能源是人类生活和社会发展的基础,研究化学反应中的能量变化,有助于更好地利用化学反应为生产和生活服务.阅读下列有关能源的材料,回答有关问题:
查看答案和解析>>
科目:高中化学 来源: 题型:
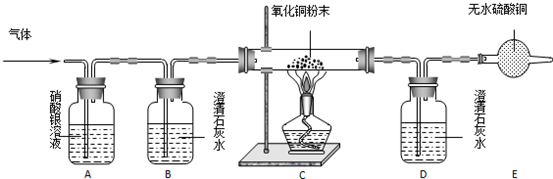
| 装置编号 | A | B | C | D | E |
| 试 剂 | 硝酸银溶液 | 澄清石灰水 | 氧化铜粉末 | 澄清石灰水 | 无水硫酸铜 |
| 现 象 | 无明显变化 | 变浑浊 | 变红色 | 无明显变化 | 变蓝色 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com