
����Ŀ����Դ�������������������ᷢչ������ء�
��1��һ���¶��£��������ݻ���Ϊ2L���ܱ������У��ֱ�����Ӧ��CO2(g)��3H2(g)![]() CH3OH(g)��H2O(g)��H=-49.0kJ��mol-1������������£�
CH3OH(g)��H2O(g)��H=-49.0kJ��mol-1������������£�
���� | �� | �� |
��Ӧ��Ͷ���� | 1molCO2(g)��3molH2(g) | 1molCH3OH(g����1molH2O(g) |
ƽ��ʱc(CH3OH) | c1 | c2 |
ƽ��ʱ�����仯 | �ų�29.4kJ | ����akJ |
�����������˵���÷�Ӧһ���ﵽƽ��״̬����_________������ĸ����
a��v(CO2)����=v(CH3OH)���� b��������ܶȲ�����ʱ��ı�
c��CO2��CH3OH��Ũ��֮�Ȳ�����ʱ��ı� d�������ƽ����Է�������������ʱ��ı�
�������������䣬�ﵽƽ������в������H2ת���ʵIJ�����_________������ĸ����
a�������¶� b����������H2 c���Ƴ��״� d�������������
��cl_________c2(����>������<������=��)��a=_________��
�ܸ��¶��·�Ӧ��ƽ�ⳣ��K=_________�������з�Ӧ10sʱ�ﵽƽ�⣬��0��10s�ڼ��е�ƽ����Ӧ����v(H2)=_________��
��2����֪��Ӧ��2NO2(����ɫ)![]() N2O4(��ɫ)��H��0����һ������NO2����ע�����к��ڣ���ͼ���������ѹ��ע�����Ĺ���������������ʱ��ı仯��������ɫԽ�����ԽС��������˵����ȷ����__________������ĸ����
N2O4(��ɫ)��H��0����һ������NO2����ע�����к��ڣ���ͼ���������ѹ��ע�����Ĺ���������������ʱ��ı仯��������ɫԽ�����ԽС��������˵����ȷ����__________������ĸ����
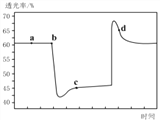
A��b��IJ�����ѹ��ע����
B��d�㣺v����v��
C��c����a����ȣ�c(NO2)����c(N2O4)��С
D������������ϵ�¶ȱ仯����û��������ʧ����Tb��Tc
���𰸡� cd bd = 19.6 2.1��25/12 0.09 mol��L-1��s-1 B
��������(1)��CO2(g)+3H2(g)CH3OH(g)+H2O(g)��H=-49.0kJmol-1��a����Ӧ����֮�ȵ��ڻ�ѧ����ʽ������֮���� v(CO2)����=v(CH3OH)����ֻ��˵����Ӧ������У�����˵����Ӧ�ﵽƽ��״̬����a����b����Ӧǰ�������������䣬������䣬�����ܶ�ʼ�ղ��䣬������ܶȲ�����ʱ��ı䣬����˵����Ӧ�ﵽƽ��״̬����b����c��CO2��CH3OH��Ũ��֮�Ȳ�����ʱ��ı䣬˵�����淴Ӧ������ͬ��˵����Ӧ�ﵽƽ��״̬����c��ȷ��d�������������䣬�������ʵ�����С�������ƽ����Է�������������ʱ��ı䣬˵����Ӧ�ﵽƽ��״̬����d��ȷ���ʴ�Ϊ��cd��
��a����ӦΪ���ȷ�Ӧ�������¶ȣ�ƽ��������У�����ת��������a�����ϣ�b����������H2 ����߶�����̼��ת���ʣ�����ת���ʼ�С����b���ϣ�c���Ƴ��״�ƽ��������У�����ת��������c�����ϣ�d���������������ѹǿ��С��ƽ�������ƶ�������ת���ʼ�С����d���ϣ��ʴ�Ϊ��bd��
��Ӧ�ú��º��������µ��ҵ�Ͷ��������ת��Ϊ���൱��Ͷ1molCO2(g)��3molH2(g)�����������ǵ�Чƽ�⣬����c1=c2���ס����ǵ�Чƽ�⣬����зų����������������յ�����֮��Ϊ49.0kJ����a=49.0kJ-29.4kJ=19.6kJ���ʴ�Ϊ��=��19.6��
�� CO2(g)+3H2(g) ![]() CH3OH(g)+H2O(g)��H=-49.0kJmol-1��
CH3OH(g)+H2O(g)��H=-49.0kJmol-1��
��ʼ��(mol) 13 0 0 49KJ
�仯��(mol/L)0.6 1.8 0.6 0.6 29.4KJ
ƽ����(mol/L)0.4 1.2 0.6 0.6
ƽ��Ũ��c(CO2)=0.2mol/L��c(H2)=0.6mol/L��c(CH3OH)=0.3mol/L��c(H2O)=0.3mol/L
K=![]() =
=![]() ��2.1�����з�Ӧ10sʱ�ﵽƽ�⣬��0��10s�ڼ��е�ƽ����Ӧ����v(H2)=
��2.1�����з�Ӧ10sʱ�ﵽƽ�⣬��0��10s�ڼ��е�ƽ����Ӧ����v(H2)= 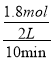 =0.09molL-1s-1���ʴ�Ϊ��
=0.09molL-1s-1���ʴ�Ϊ�� ![]() (��2.1)��0.09molL-1s-1��
(��2.1)��0.09molL-1s-1��
(2)A.b�㿪ʼ��ѹ��ע�����Ĺ��̣�������ɫ������ʱ�С����A����B.c���Ĺյ�������ע�����Ĺ��̣�d����ƽ���������������������ƶ����̣�����v(��)��v(��)����B��ȷ��C.c����ѹ��ע����������������������������������Ũ�ȶ�����C����D.b�㿪ʼ��ѹ��ע�����Ĺ��̣�ƽ�������ƶ�����Ӧ���ȣ�����T(b)��T(c)����D���ʴ�Ϊ��B��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������Ժ�CO2������Ӧ��Fe(s)��CO2(g)![]() FeO(s)��CO(g)��һ���¶��£���ij�ܱ������м����������۲�����һ������CO2���壬��Ӧ������CO2�����CO�����Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ.����˵������ȷ����
FeO(s)��CO(g)��һ���¶��£���ij�ܱ������м����������۲�����һ������CO2���壬��Ӧ������CO2�����CO�����Ũ����ʱ��Ĺ�ϵ��ͼ��ʾ.����˵������ȷ����

A. a��Ϊƽ��״̬
B. b���c��Ļ�ѧƽ�ⳣ��K��ͬ
C. �÷�Ӧ�Ļ�ѧƽ�ⳣ����ʾΪK =[CO]��[FeO]/[CO2]��[Fe]
D. ���¶����ߣ��÷�Ӧ�Ļ�ѧƽ�ⳣ��K������÷�Ӧ�� ��H �� 0
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����4mol A�����2molB��������2L�ܱ������У���Ϻ������·�Ӧ��2A��g��+B��g��2C��g��+ D��s��������2s����C��Ũ��Ϊ0.6molL-1������˵����ȷ���ǣ�������
A. ������A��ʾ�ķ�Ӧ����Ϊ0.6mol��Ls��-1 B. 2sʱ����B�ĺ���Ϊ23.3��
C. 2sʱ����A��ת����Ϊ30% D. 2sʱ����B��Ũ��Ϊ0.3molL-1
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�������£���Բ����ƿ�м���1 molC2H5OH�ͺ�1molHBr�������ᣬ��Һ�з�����Ӧ��C2H5OH+HBr![]() C2H5Br+H2O����ַ�Ӧ��ﵽƽ�⡣��֪��ѹ�£�C2H5Br��C2H5OH�ķе�ֱ�Ϊ38.4���78.5�档�����й������������
C2H5Br+H2O����ַ�Ӧ��ﵽƽ�⡣��֪��ѹ�£�C2H5Br��C2H5OH�ķе�ֱ�Ϊ38.4���78.5�档�����й������������
A. ����NaOH���������Ҵ������ʵ���
B. ����HBrŨ�ȣ�����������C2H5Br
C. ����Ӧ��������2 mol�������ַ�Ӧ��ƽ��ת����֮�Ȳ���
D. ����ʼ�¶������60�棬�����̷�Ӧ�ﵽƽ���ʱ��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��������ͼ��ʾ����װ���Ʊ������ѣ���������������ǣ�������
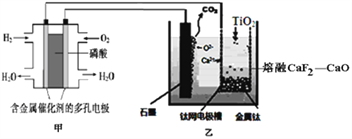
A. ��װ�ù���������pH����
B. ��װ����ʯī�缫��ӦʽΪC-4e-+2O2-=CO2��
C. ��װ����ͨ��O2�ĵ缫��ӦʽΪ��O2+4e-+4H+=2H2O
D. ��������װ�õ���ʧ���Ʊ�24.0g�����ѣ���Ҫ��������22.4L
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ�з�Ӧ�����Ʊ�SiH4��һ�ַ������丱����MgCl2��6NH3�����ʵ�þ��Դ���ش��������⣺
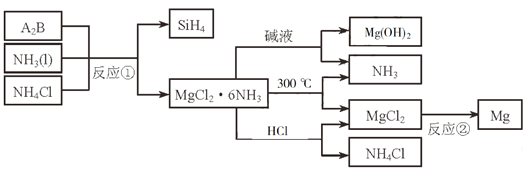
��1��MgCl2��6NH3����Ԫ�صļ����Ӱ뾶��С�����˳��H-���⣩��_________________________��Mg��Ԫ�����ڱ��е�λ�ã�_____________________��Mg(OH)2�ĵ���ʽ��____________________��
��2��A2B�Ļ�ѧʽΪ_______________����Ӧ�ڵıر�������_______________����ͼ�п���ѭ��ʹ�õ�������_______________��
��3����һ�������£���SiH4��CH4��Ӧ����H2��һ�ֹ�����ĥ����_______________��д��ѧʽ����
��4��Ϊʵ��ȼú������ú�м��뽬״Mg(OH)2��ʹȼ�ղ�����SO2ת��Ϊ�ȶ���Mg�����д���÷�Ӧ�Ļ�ѧ����ʽ��_______________��
��5����Mg�Ƴɵĸ����Լ���RMgBr���������л��ϳɣ������Ʊ��������ĺϳ�·�����£�

����������Ϣ��д���Ʊ�![]() ����ȩ�Ŀ��ܽṹ��ʽ��_______________��
����ȩ�Ŀ��ܽṹ��ʽ��_______________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ձ��и�ʢ��200mL 3mol/L�����������������Һ�������ձ��зֱ��������������ۣ���Ӧ�����������ɵ��������֮��Ϊ1:2�����������۵�����Ϊ�� ��
A. 2.7g B. 3.6g C. 5.4g D. 10.8g
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����1����(N2H4)���ӿ���ΪNH3�����е�һ����ԭ�ӱ���NH2(����)ȡ���γɵ���һ�ֵ����⻯�NH3���ӵ����幹����________��N2H4�����е�ԭ�ӹ�����ӻ�������________��
��2����OH����Ϊ�ȵ������һ�ַ���Ϊ________________(�ѧʽ)��N��O��F�ĵ�һ�������ɴ�С��˳��Ϊ________________��
��3���� H2O�����У�H��O��H�ļ�����________��H������H2O�γ�H3O����H3O����H��O��H���DZ�H2O��H��O��H���Ǵ�ԭ��Ϊ_________________________________________��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������ˮ��Ӧ��������Ƶ����������ص��ǣ� ��
A.�Ƶ��۵��B.�Ƶ��ܶ�СC.�Ƶ�Ӳ��СD.�Ƶ�ǿ��ԭ��
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com