
| A. | B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2165kJ•mol-1 | |
| B. | B2H6(g)+3O2(g)═B2O3(s)+3H2O(g)△H=-2033kJ•mol-1 | |
| C. | B2H6(g)+3O2(g)═B2O3+3H2O△H=-2165kJ•mol-1 | |
| D. | B2H6(g)+O2(g)═B2O3(s)+H2O(l)△H=-2165kJ•mol-1 |
分析 0.3mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5KJ的热量,则1mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和液态水,放出649.5kJ×$\frac{1mol}{0.3mol}$=2165kJ的热量,反应的热化学方程式为:B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165 kJ/mol①,又已知H2O(l)=H2O(g)△H=+44kJ/moL②,根据盖斯定律,①+②×3得反应:B2H6(g)+3O2(g)=B2O3(s)+3H2O(g),据此进行计算焓变,然后结合热化学方程式的书写原则进行判断.
解答 解:0.3mol的气体高能燃料乙硼烷(B2H6)在O2中燃烧,生成固态B2O3和液态H2O,放出649.5kJ的热量,则1mol气态高能燃料乙硼烷在氧气中燃烧,生成固态三氧化二硼和液态水,放出热量为:649.5kJ×$\frac{1mol}{0.3mol}$=2165kJ,反应的热化学方程式为:①B2H6(g)+3O2(g)=B2O3(s)+3H2O(l)△H=-2165kJ/mol,已知②H2O(l)=H2O(g)△H=+44kJ/moL,
根据盖斯定律,①+②×3得:B2H6(g)+3O2(g)=B2O3(s)+3H2O(g)△H=-2033kJ/mol,
故选B.
点评 本题考查热化学方程式的书写方法,题目难度不大,判断热化学方程式正误时需要分析:物质的状态、反应热的数值与单位,反应热的数值与化学方程式前面的系数成正比等,试题侧重考查学生的分析能力及灵活应用基础知识的能力.


科目:高中化学 来源: 题型:实验题
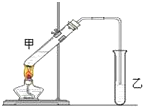 俗话说:“陈酒老醋特别香”,其原因是酒在存储过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示装置来模拟该过程,请回答下列问题:
俗话说:“陈酒老醋特别香”,其原因是酒在存储过程中生成了有香味的乙酸乙酯,在实验室里我们也可以用如图所示装置来模拟该过程,请回答下列问题:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| 选项 | 容量瓶容积 | 固体质量 | 实验操作 |
| A | 180mL | SrCl2:28.6g | 加入180mL水 |
| B | 200mL | SrCl2:31.8g | 配成200mL溶液 |
| C | 250mL | SrCl2:39.8g | 配成250mL溶液 |
| D | 250mL | SrCl2•2H2O:39.8g | 配成250mL溶液 |
| A. | A | B. | B | C. | C | D. | D |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 用到的玻璃仪器有:玻璃棒、胶头滴管、500mL容量瓶、烧杯 | |
| B. | 需要称量氢氧化钠固体1.92g | |
| C. | 没有等溶液冷却就转移将导致所配溶液浓度偏高 | |
| D. | 洗净的容量瓶不需要干燥就能使用,但使用前需检漏 |
查看答案和解析>>
科目:高中化学 来源: 题型:填空题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 称量后转移固体时不小心把少量固体洒到烧杯外 | |
| B. | 加水定容时,加水过多,倒出后并恢复到刻度线水平 | |
| C. | 转移过程中不小心把几滴溶液滴在外面 | |
| D. | 干净的容量瓶又用蒸馏水洗涤了一遍 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 铝是还原剂,其氧化产物是H2 | B. | NaOH是氧化剂,其还原产物是H2 | ||
| C. | 铝是还原剂,H2O和NaOH都是氧化剂 | D. | H2O是氧化剂,Al被氧化 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com