
 ����ݻ�ѧ��ӦFe+CuCl2=FeCl2+Cu���һ��ԭ��أ���ѡ����CuCl2��aq����FeCl2 ��aq����FeSO4��aq����CuSO4��aq����ͭƬ����Ƭ��пƬ�͵��ߣ�
����ݻ�ѧ��ӦFe+CuCl2=FeCl2+Cu���һ��ԭ��أ���ѡ����CuCl2��aq����FeCl2 ��aq����FeSO4��aq����CuSO4��aq����ͭƬ����Ƭ��пƬ�͵��ߣ����� ��1���÷�Ӧ��FeԪ�ػ��ϼ���0�۱�Ϊ+2�ۣ�CuԪ�ػ��ϼ���+2�۱�Ϊ0�ۣ�����������Ӧ�Ľ���Fe������������Fe���õĽ���ͭ��ķǽ�����������CuCl2Ϊ����ʣ������ŵ�װ��Ҫ���������Ͳμӷ�Ӧ�ĵ���ʷֿ�����˸����������Ȼ�������Һ�У�����ͭ�����Ȼ�ͭ��Һ�У��ݴ���ƣ�
��2����ԭ��ظ�����ʧ���ӷ���������Ӧ��������ͭ���ӵõ��ӷ���������Ӧ��
��3��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�
��4������ȼ�ϵ���У��������Ǽ��鷢��ʧ���ӵ�������Ӧ�������������������õ��ӵĻ�ԭ��Ӧ������Ϊ������Ǽ���Һ�������ڵ缫�Ϸų�������̼��
��� �⣺��1���÷�Ӧ��FeԪ�ػ��ϼ���0�۱�Ϊ+2�ۣ�CuԪ�ػ��ϼ���+2�۱�Ϊ0�ۣ�����������Ӧ�Ľ���Fe������������Fe���õĽ���ͭ��ķǽ�����������CuCl2Ϊ����ʣ������ŵ�װ��Ҫ���������Ͳμӷ�Ӧ�ĵ���ʷֿ�����˸����������Ȼ�������Һ�У�����ͭ�����Ȼ�ͭ��Һ�У�װ��ͼΪ��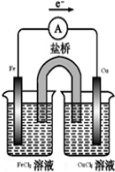 ��
��
�ʴ�Ϊ�� ��
��
��2����ԭ��ظ�����ʧ���ӷ���������Ӧ���缫��ӦʽΪ��Fe-2e-=Fe2+��������ͭ���ӵõ��ӷ���������Ӧ���缫��ӦʽΪ��Cu2++2e-=Cu��
�ʴ�Ϊ��Fe-2e-=Fe2+��Cu2++2e-=Cu��
��3��ԭ����ǽ���ѧ��ת��Ϊ���ܵ�װ�ã�
�ʴ�Ϊ����ѧ���磻
��4������ȼ�ϵ���Լ���ҺΪ�������Һʱ���������Ǽ��鷢��ʧ���ӵ�������Ӧ��������̼�ͼӦ�õ�����̼��أ���CH4+10OH--8e-=CO32-+7H2O�������������õ��ӷ�����ԭ��Ӧ���缫��ӦΪ��O2+2H2O+4e-=4OH-��
�ʴ�Ϊ��CH4+10OH--8e-=CO32-+7H2O��O2+2H2O+4e-=4OH-��
���� ���⿼����ԭ�����ƣ������¿α�Ҫ��ѧ����Ҫ���յ����ݣ���ȷ�ж�ԭ������������ϡ��������Һ�����ԭ����ѵ㣬һ����˵����ԭ�������������縺�����õĽ�����ǽ�������������������������Һ���������Һ��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� |  | B�� |  | C�� |  | D�� |  |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢۢܢ� | B�� | �ڢ٢ݢۢ� | C�� | �٢ڢۢݢ� | D�� | �ڢ٢ۢݢ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ѧ��Ӧ���ʿ����÷�Ӧ���ת���ʴ�С������ | |
| B�� | Ӱ�컯ѧ��Ӧ���ʵ���������ֻ���¶ȡ�Ũ�ȡ�ѹǿ�ʹ��� | |
| C�� | ��ѧƽ��״ָ̬���Ƿ�Ӧ���������Ũ�����ʱ��״̬ | |
| D�� | �������ܼӿ컯ѧ��Ӧ���ʣ��������ԭ�������ʻ�ת���� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ��ƶ���

�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ʵ����
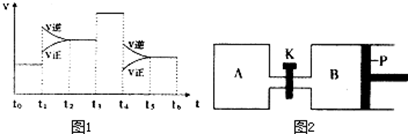
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��̼�Ͷ�����̼���� | B�� | �������ᷴӦ | ||
| C�� | ʯ��ʯ�ķֽ� | D�� | ������ԭ����ͭ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ��ˮ�У�c��Cl2��=2[c��ClO-��+c��Cl-��+c��HClO��] | |
| B�� | Na2CO3��Һ��c��OH-��-c��H+��=c��HCO3-��+2 c��H2CO3�� | |
| C�� | ��Ũ�ȵ�NaClO��NaHCO3�����Һ�У�c��HClO��+c��ClO-��=c��HCO3-��+c��H2CO3�� | |
| D�� | �����£���0.01 mol•L-1 NH4HSO4��Һ�еμ�NaOH��Һ�����ԣ�c��NH4+����c��Na+����c��SO42-����c��OH-��=c��H+�� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com