
| 11.2L |
| 22.4L/mol |


科目:高中化学 来源: 题型:
 甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g).
甲醇是一种可再生能源,具有开发和应用的广阔前景,工业上一般可采用如下反应来合成甲醇:CO(g)+2H2(g)?CH3OH(g).查看答案和解析>>
科目:高中化学 来源: 题型:
| 实验目的 | 操作 | 实验现象 | 结论 |
| ①检验Cl- | 取少许滤液于试管中, | 含有Cl- | |
| ②检验NH4+ | 取少许滤液于试管中, | 含有NH4+ | |
| ③检验Zn2+ | 取少许滤液于试管中,加入稀氨水 | 先产生白色沉淀,继续加入氨水,沉淀又溶解 | 含有Zn2+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
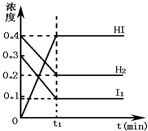 可逆反应H2(g)+I2(g)?2HI(g)在一定的条件下反应混合物中各组分的浓度(mol?L-1)与时间t(min)的变化曲线如图所示,根据图示,回答:
可逆反应H2(g)+I2(g)?2HI(g)在一定的条件下反应混合物中各组分的浓度(mol?L-1)与时间t(min)的变化曲线如图所示,根据图示,回答:查看答案和解析>>
科目:高中化学 来源: 题型:
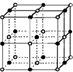 完成下列问题.
完成下列问题.| 离子晶体 | NaCl | KCl | CaO |
| 晶格能/kJ?mol-1 | 786 | 715 | 3401 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
 某学生设计了如图的方法对X盐进行鉴定:由此分析,下列结论中不正确的是( )
某学生设计了如图的方法对X盐进行鉴定:由此分析,下列结论中不正确的是( )| A、X中可以有Fe2+ |
| B、Y为AgI沉淀 |
| C、X中可以有Fe3+ |
| D、M试剂可以是H2O2 |
查看答案和解析>>
科目:高中化学 来源: 题型:
A、 根据图可判断可逆反应A2(g)+3B2(g)?2AB3(g)的△H>0 |
B、 图表示体积相等、pH=1的醋酸溶液与盐酸加入等量水稀释时的pH变化 |
C、 图可表示乙酸溶液中通入氨气至过量过程中溶液导电性的变化 |
D、 图可表示压强对可逆反应2A(g)+2B(g)?3C(g)+D(s)的影响,乙的压强大 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com