
【题目】我国古代在西汉《淮南子·万毕术》一书中有湿法炼铜的文字记载:“曾青得铁则化铜”铜金属被广泛地应用于电力、电子、交通、轻工、新兴产业等领域。
回答下列问题:
(1)铁原子的外围电子排布图为___________。
(2)向FeCl3溶液加入KSCN溶液形成K3[Fe(SCN)6]血红色溶液。
①写出与SCN-离子互为等电子体的合理分子或离子:_____________。(两个)
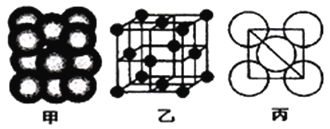
②铁原子的堆积方式如右图(甲)所示,其晶胞特征如右图(乙)所示,原子之间相互位置关系的平面图如右图(丙)所示;已知铁原子半径rpm,铁晶胞空间利用率为:____________。(用字母π表示)
(3)含有Fe2+的水溶液可以用K3[Fe(CN)6]于实验室的定性检验,检验Fe2+离子的离子方程式为:___________。
(4)一水合硫酸四氨合铜[Cu(NH3)4]SO4·H2O为蓝色正交晶体,常用作杀虫剂、媒染剂,在碱性镀铜中也常用作电镀液的主要成分,在工业上用途广泛。
①[Cu(NH3)4]SO4·H2O中非金属元素H、N、O的电负性由大到小的顺序为:___________。(用元素符号作答)
②[Cu(NH3)4]SO4·H2O晶体中存在的化学键有___________ (填编号)
a金属键 b离子键 c氢键 d配位键 e极性键 f非极性键
③NH3分子的VSEPR模型为:___________;SO42-中S为___________杂化。
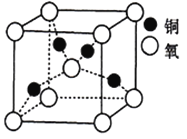
(5)铜的某种氧化物晶胞结构如图所示,若该晶胞的边长为acm,则该氧化物的密度为______g/cm3(设阿伏加德罗常数的值为NA)。
【答案】 ![]() CO2、N2O、N3-
CO2、N2O、N3- ![]() 3Fe2++2Fe(CN)63-=Fe3[Fe(CN6)]2↓ O>N>H bde 四面体 sp3
3Fe2++2Fe(CN)63-=Fe3[Fe(CN6)]2↓ O>N>H bde 四面体 sp3 ![]()
【解析】(1)铁为26号元素,原子的外围电子排布式为:3d64s2,外围电子排布图为![]() ;(2)①等电子体是指具有相同价电子数目和原子数目的分子或离子,与SCN-离子互为等电子体的分子和离子分别为CO2、N2O、N3-等;②根据图(乙)所示可知,铁原子晶胞为面心堆积,面对角线长度是原子半径的4倍。假定晶胞边长为a,则a2+a2= (4r)2,a=
;(2)①等电子体是指具有相同价电子数目和原子数目的分子或离子,与SCN-离子互为等电子体的分子和离子分别为CO2、N2O、N3-等;②根据图(乙)所示可知,铁原子晶胞为面心堆积,面对角线长度是原子半径的4倍。假定晶胞边长为a,则a2+a2= (4r)2,a=![]() r,晶胞体积V晶胞=
r,晶胞体积V晶胞=![]() r3。面心立方堆积的晶胞上占有的原子数为4,原子占有的体积为V原子=4×(
r3。面心立方堆积的晶胞上占有的原子数为4,原子占有的体积为V原子=4×(![]() )。晶胞的空间利用率等于
)。晶胞的空间利用率等于![]() =
=![]() =
=![]() ;(3)检验Fe2+离子的离子方程式为:3Fe2++2Fe(CN)63-=Fe3[Fe(CN6)]2↓;(4)①元素非金属性越强,电负性越大,故H、N、O的电负性由大到小的顺序为:O>N>H;②[Cu(NH3)4]SO4·H2O晶体中[Cu(NH3)4]2+与SO42-之间存在离子键,Cu2+与NH3之间形成的化学键为配位键,NH3、SO42-、H2O中均存在极性共价键,故[Cu(NH3)4]SO4·H2O晶体中存在的化学键有离子键、配位键、极性键,答案选bde;③NH3中,价层电子对数=σ键个数+
;(3)检验Fe2+离子的离子方程式为:3Fe2++2Fe(CN)63-=Fe3[Fe(CN6)]2↓;(4)①元素非金属性越强,电负性越大,故H、N、O的电负性由大到小的顺序为:O>N>H;②[Cu(NH3)4]SO4·H2O晶体中[Cu(NH3)4]2+与SO42-之间存在离子键,Cu2+与NH3之间形成的化学键为配位键,NH3、SO42-、H2O中均存在极性共价键,故[Cu(NH3)4]SO4·H2O晶体中存在的化学键有离子键、配位键、极性键,答案选bde;③NH3中,价层电子对数=σ键个数+![]() (a-xb)=3+
(a-xb)=3+![]() (5-3×1)=4,含孤电子对数为1,杂化轨道数4,中心原子以采取sp3杂化,分子的VSEPR模型为正四面体形;SO42-中S的价层电子对数=σ 键个数+
(5-3×1)=4,含孤电子对数为1,杂化轨道数4,中心原子以采取sp3杂化,分子的VSEPR模型为正四面体形;SO42-中S的价层电子对数=σ 键个数+![]() (a-xb)=4+
(a-xb)=4+ ![]() (6+2-4×2)=4,所以采取sp3杂化;(4)分析晶胞示意图可知该晶胞中实际拥有2个氧离子、4个铜离子,可得该铜的氧化物化学式为Cu2O,一个晶胞含有2个“Cu2O”,质量为
(6+2-4×2)=4,所以采取sp3杂化;(4)分析晶胞示意图可知该晶胞中实际拥有2个氧离子、4个铜离子,可得该铜的氧化物化学式为Cu2O,一个晶胞含有2个“Cu2O”,质量为![]() ×144 g,该晶胞的体积为a3 cm3,则该氧化物的密度为
×144 g,该晶胞的体积为a3 cm3,则该氧化物的密度为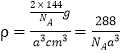 。
。


科目:高中化学 来源: 题型:
【题目】(1)在3种有机物 ① ![]() 、② CH2=CH2、③葡萄糖中,从石油中提取的重要有机溶剂是______(填序号,下同),可用作生产塑料袋的是_______。为人体提供能量的物质是_______。
、② CH2=CH2、③葡萄糖中,从石油中提取的重要有机溶剂是______(填序号,下同),可用作生产塑料袋的是_______。为人体提供能量的物质是_______。
(2)在3种无机物 ① Na2SiO3、②HNO3、③ SO2中,可用作阻燃的是______(填序号,下同),可用于漂白织物的是______, 可用作生产炸药的是______。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,0.2mol/L的一元碱BOH与等浓度的HCl溶液等体积混合后,所得溶液中部分微粒组分及浓度如图所示,下列说法正确的是( )
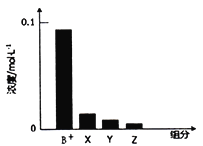
A. BOH为强碱 B. 该混合液pH=7
C. 图中X表示BOH,Y表示H+,Z表示OH- D. 该混合溶液中:c(Cl-)=c(Y)+c(B+)
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】标准状况下,现有![]() ;
;![]() 个HCl分子;
个HCl分子;![]() ;
;![]()
![]() ,对这四种气体的关系有以下四种表述:其中正确的是 ______ .
,对这四种气体的关系有以下四种表述:其中正确的是 ______ .
a.体积:![]()
b.物质的量:![]()
c.质量:![]()
d.氢原子个数:![]()
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】新兴的大脑营养研究发现大脑的生长发育与不饱和脂肪酸有密切的关系。从深海鱼油中提取的,被称作“脑黄金”的DHA就是一种不饱和度很高的脂肪酸,它的分子中含6个碳碳双键,学名叫二十六碳六烯酸,它的分子式是( )
A. C25H50COOH B. C25H39COOH C. C26H41COOH D. C26H47COOH
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】用NA表示阿伏加德罗常数的值,下列叙述正确的是( )
A. 含有NA个氦原子的氦气在标准状况下的体积约为11.2L
B. 在常温常压下,11.2L Cl2含有的分子数为0.5NA
C. 25℃,1.01×105Pa,64gSO2中含有的原子数为3NA
D. 标准状况下,11.2LH2O含有的分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】按要求对下图中两极进行必要的连接并填空:
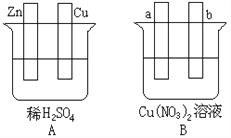
(1)在A图中,使铜片上冒气泡。请加以必要联接,则联接后的装置叫_______________。电极反应式:锌电极:________________________________;铜电极:_____________________________。
(2)在B图中(a,b都为惰性电极),使a极析出铜,则b析出:_______________。加以必要的联接后,该装置叫________________。电极反应式: b极:________________________________。经过一段时间后,停止反应并搅均溶液,溶液的pH值____________(升高、降低、不变)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】现有m g某气体,它由双原子分子构成,它的摩尔质量为M g·mol-1。若阿伏加德罗常数的值用NA表示,则:
(1)该气体的物质的量为________。
(2)该气体所含原子总数为________。
(3)该气体在标准状况下的体积为________。
(4)该气体在标准状况下的密度为________。
(5)该气体一个分子的质量为________。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com