
【题目】A与芳香族化合物B在一定条件下反应生成C,进一步反应生成有机酸D,D的二水合钠盐医学上称之为当归素,是一种治疗偏头痛的有效新药.A的相对分子质量是104,1mol A与足量的NaHCO3反应生成2mol气体. 已知:RCHO+CH2(COOH)2 ![]() RCH=C(COOH)2+H2O,
RCH=C(COOH)2+H2O,
RCH=C(COOH)2 ![]() RCH=CHCOOH+CO2
RCH=CHCOOH+CO2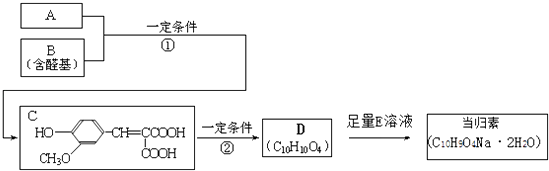
(1)C可能发生的反应是(填序号). a.氧化反应 b.水解反应 c.消去反应 d.酯化反应
(2)等物质的量的C分别与足量的Na、NaHCO3、NaOH反应消耗Na、NaHCO3、NaOH的物质的量之比是 .
(3)E的名称: .
(4)反应①的化学方程式是 .
(5)符合下列条件的D的同分异构体有种,写出其中任意一种的结构简式 . ①在苯环上只有两个取代基;②在苯环上的一氯取代物只有两种;
③1mol该同分异构体与足量的NaHCO3反应生2mol CO2 .
【答案】
(1)ad
(2)3:2:3
(3)碳酸氢钠
(4)![]()
(5)4;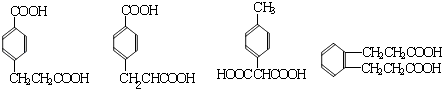
【解析】解:A的相对分子质量为104,1mol A与足量的碳酸氢钠反应生成2mol二氧化碳,则A分子含有2个﹣COOH,去掉2个﹣COOH剩余总相对原子质量为104﹣45×2=14,剩余基团为CH2 , 故A的结构简式为HOOCCH2COOH;B的结构中含有醛基,根据C结构简式结合信息知,B为 ![]() ,C在一定条件下生成有机酸D,结合D的分子式可知,C脱去1分子二氧化碳生成D,由信息可知,D的结构简式为
,C在一定条件下生成有机酸D,结合D的分子式可知,C脱去1分子二氧化碳生成D,由信息可知,D的结构简式为 ![]() ,D与足量的E反应得到当归素,由当归素的分子式可知,D中羧基发生反应生成钠盐,故E为碳酸氢钠,(1)C和酚羟基、碳碳双键,可以发生氧化反应,含有羧基,可以发生酯化反应,醚键很稳定,不易发生水解反应,不能发生消去反应,故选:ad;(2)C中酚羟基和羧基都与钠反应生成氢气,只有羧基能和碳酸氢钠反应生成二氧化碳,酚羟基和羧基都能与NaOH反应,所以等物质的量的C分别与足量的Na、NaHCO3、NaOH反应消耗Na、NaHCO3、NaOH的物质的量之比是3:2:3,所以答案是:3:2:3;(3)通过以上分析知,E名称是碳酸氢钠,所以答案是:碳酸氢钠;(4)在一定条件下,A和B反应生成C,反应方程式为:
,D与足量的E反应得到当归素,由当归素的分子式可知,D中羧基发生反应生成钠盐,故E为碳酸氢钠,(1)C和酚羟基、碳碳双键,可以发生氧化反应,含有羧基,可以发生酯化反应,醚键很稳定,不易发生水解反应,不能发生消去反应,故选:ad;(2)C中酚羟基和羧基都与钠反应生成氢气,只有羧基能和碳酸氢钠反应生成二氧化碳,酚羟基和羧基都能与NaOH反应,所以等物质的量的C分别与足量的Na、NaHCO3、NaOH反应消耗Na、NaHCO3、NaOH的物质的量之比是3:2:3,所以答案是:3:2:3;(3)通过以上分析知,E名称是碳酸氢钠,所以答案是:碳酸氢钠;(4)在一定条件下,A和B反应生成C,反应方程式为: ![]() , 所以答案是:
, 所以答案是: ![]() ;(5)阿魏酸的同分异构体符合下列条件:
;(5)阿魏酸的同分异构体符合下列条件:
①在苯环上只有两个取代基;
②在苯环上的一氯取代物只有两种,说明两个取代基处于对位位置,且两个取代基不同或者两个取代基处于邻位位置,且两个取代基相同,
③1mol该同分异构体与足量NaHCO3反应生成2mol CO2气体,含有2个﹣COOH,
所以符合条件的阿魏酸的同分异构体结构简式分别为:  ,所以符合条件的有4种,
,所以符合条件的有4种,
所以答案是:4;  .
.


科目:高中化学 来源: 题型:
【题目】设NA为阿伏伽德罗常数的值.下列有关叙述正确的是( )
A.l mol OH﹣所含电子数为10NA
B.2L0.5 molL﹣1Na2SO4溶液中阴离子所带电荷数为0.2NA
C.标准状况下,1.12 L CCl4含有的氯原子数为0.2NA
D.14 g由CO和N2组成的混合气体中含有的分子总数为NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】短周期元素X、Y、Z的原子序数依次递增,其原子的最外层电子数之和为13。X与Y、Z位于相邻周期,Z原子最外层电子数是X原子内层电子数的3倍或者是Y原子的最外层电子数的3倍。下列说法正确的是( )
A.X的氢化物溶于水显酸性
B.Y原子的电子排布式为1s22s22p63s2
C.Z元素在周期表中的位置为第三周期第Ⅵ族
D.X和Z的最高价氧化物对应水化物都是弱酸
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】吸进人体内的氧有2%转化为氧化性极强的活性氧,这些活性氧能加速人体衰老,被称为“生命杀手”。中国科学家尝试用Na2SeO3清除人体内活性氧,Na2SeO3的作用是( )
A.还原剂B.氧化剂
C.既是氧化剂又是还原剂D.既不是氧化剂又不是还原剂
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】对于密闭容器中的可逆反应:4L(g)2M(g)+N(g)△H>0,其平衡状态与温度(T)和压强(P1>P2)的关系如图所示.图中y轴是指( ) 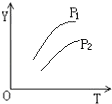
A.气体混合物的平均相对分子质量
B.气体混合物的总物质的量浓度
C.L在气体混合物的体积分数
D.气体混合物的密度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法正确的是
A. 液态氯化氢、固态氯化钠不导电,所以HCl、NaCl不是电解质
B. NH3、CO2水溶液均能导电,所以NH3、CO2均是电解质
C. 蔗糖、酒精在水溶液中或熔化时不导电,所以它们不是电解质
D. 铜、石墨均导电,所以它们是电解质
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某研究性学习小组欲测定室温下(25℃、101kPa)的气体摩尔体积,请回答以下问题.该小组设计的简易实验装置如图所示: 
该实验的主要操作步骤如下:
①配制100mL 1.0molL﹣1的盐酸溶液;
②用…………….(填仪器名称并注明规格)量取7.5mL 1.0molL﹣1的盐酸溶液加入锥形瓶中;
③称取a g已除去表面氧化膜的镁条,并系于铜丝末端,为使HCl全部参加反应,a的数值至少为,………….g;
④往广口瓶中装入足量水,按如图连接好装置,检查装置的气密性;
⑤反应结束后待体系温度恢复到室温,读出量筒中水的体积为V mL.
请将上述步骤补充完整并回答下列问题.
(1)步骤①中,配制100mL 1.0molL﹣1的盐酸溶液时,下列哪些操作会使配制浓度偏小 (填写字母).
A.用量筒量取浓盐酸时,俯视量筒的刻度
B.容量瓶未干燥即用来配制溶液
C.浓盐酸在烧杯中稀释时,搅拌时间过长
D.定容完成后,将容量瓶倒置摇匀后,发现液面低于刻度线
E.在容量瓶中定容时俯视容量瓶刻度线
F.烧杯中有少量水
(2)请填写操作步骤中的空格:步骤② , 步骤③g.
(3)实验步骤⑤中应选用 (填字母)的量筒.
A.100mL
B.200mL
C.500mL
(4)忽略水蒸气影响,在该条件下测得气体摩尔体积的计算式为Vm=L/mol.
(5)若未除去镁条表面的氧化膜,则测得该条件下气体的摩尔体积(填偏大、偏小或无影响).
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】将m1g铜铝合金投入到1LH2SO4和HNO3的混合溶液中,完全溶解后只生成VLNO气体(标准状况),向反应后的溶液中逐渐加入1mol/LNaOH溶液,生成沉淀的质量与所加NaOH溶液的体积的关系如图所示.下列说法中不正确的是( ) 
A.m1﹣m2═10.2
B.2c(H2SO4)+c(HNO3)═0.8 molL﹣1
C.原合金中铝的质量分数为34.7%
D.V=2.24
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com