
| A. | 8:3 | B. | 3:8 | C. | 27:4 | D. | 4:27 |
分析 一定质量的Cu和Cu(NO3)2的混合物在空气中加热,Cu与氧气反应生成CuO,Cu(NO3)2受热分解为CuO、NO2和O2,最后固体为CuO,结合反应前后的质量关系列式计算.
解答 解:一定质量的Cu和Cu(NO3)2的混合物在空气中加热,Cu与氧气反应生成CuO,Cu(NO3)2受热分解为CuO、NO2和O2,最后固体为CuO,
设Cu为xmol,Cu(NO3)2为ymol,
则64x+188y=80x+80y,
x:y=27:4,
故选C.
点评 本题考查混合物的计算,为高频考点,为高频考点,侧重于学生的分析能力和计算能力的考查,明确最终物质成分为解答该题的关键,题目难度不大.


科目:高中化学 来源: 题型:选择题
| A. | 1:1 | B. | 2:1 | C. | 2:3 | D. | 3:2 |
查看答案和解析>>
科目:高中化学 来源: 题型:实验题
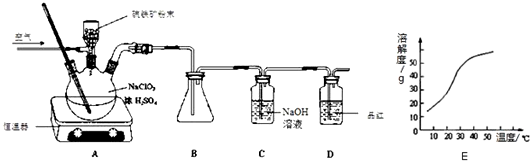
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
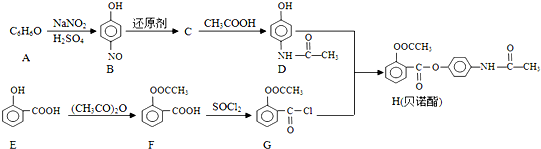
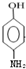 ;
;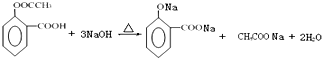 ;
;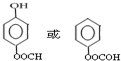 ;
;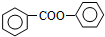 的合成路线流程图(无机试剂可任选):
的合成路线流程图(无机试剂可任选):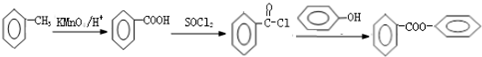 .
.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 单质硅用于制造芯片和光导纤维 | |
| B. | 84消毒液的有效成分是NaClO | |
| C. | SO2具有漂白性,通入紫色石蕊溶液中能使溶液先变红后褪色 | |
| D. | 普通玻璃的组成可用Na2O•CaO•6SiO2表示,是纯净物 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
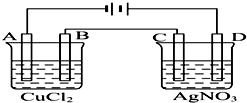 如图为以惰性电极进行电解的装置:
如图为以惰性电极进行电解的装置:查看答案和解析>>
科目:高中化学 来源: 题型:解答题
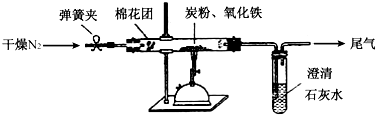
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | c(H+) | B. | Kb(NH3•H2O) | ||
| C. | $\frac{c(N{H}_{3}•{H}_{2}O)}{c(N{{H}_{4}}^{+})}$ | D. | c(NH4+) |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com