
碳酸二甲酯(DMC)是一种近年来受到广泛关注的环保型绿色化工产品。在催化剂作用下,可由甲醇和CO2直接合成DMC:CO2+2CH3OH―→CO(OCH3)2+H2O,但甲醇转化率通常不会超过1%是制约该反应走向工业化的主要原因。某研究小组在其他条件不变的情况下,通过研究温度、反应时间、催化剂用量分别对转化数(TON)的影响来评价催化剂的催化效果。
计算公式为TON=转化的甲醇的物质的量/催化剂的物质的量。
(1)已知25 ℃时,甲醇和DMC的标准燃烧热分别为ΔH1和ΔH2,则上述反应在25 ℃时的焓变ΔH3=________。
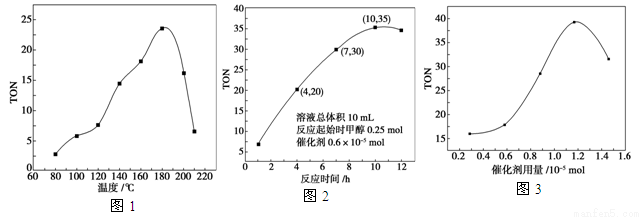
(2)根据反应温度对TON的影响图(图1)判断该反应的焓变ΔH____0(填“>”、“=”或“<”),理由是_________。
(3)根据反应时间对TON的影响图(图2),已知溶液总体积 10 mL,反应起始时甲醇0.25 mol,催化剂0.6×10-5 mol,计算该温度下,4~7 h内DMC的平均反应速率:________;计算10 h时,甲醇的转化率:________。
(4)根据该研究小组的实验及催化剂用量TON的影响图(图3),判断下列说法正确的是________。
a.由甲醇和CO2直接合成DMC,可以利用价廉易得的甲醇把影响环境的温室气体CO2转化为资源,在资源循环利用和环境保护方面都具有重要意义
b.在反应体系中添加合适的脱水剂,将提高该反应的TON
c.当催化剂用量低于1.2×10-5 mol时,随着催化剂用量的增加,甲醇的平衡转化率显著提高
d.当催化剂用量高于1.2×10-5 mol时,随着催化剂用量的增加,DMC的产率反而急剧下降
(1)2ΔH1-ΔH2 (3分)
(2)<(1分) 经过相同的反应时间,温度较低时,反应未达到平衡;温度较高时,反应已达到平衡,随着温度升高,TON减小,即平衡向左移动,说明该反应的正反应是放热反应,所以ΔH<0;
(3)1×10-3 mol·L-1·h-1(3分) 8.4×10-2%(3分);(4)a、b(3分)。
【解析】
试题分析:(1)因为在25 ℃时,甲醇和DMC的标准燃烧热分别为ΔH1和ΔH2,则可得热化学方程式是:① CH4O(l)+3/2O2(g)=CO2(g)+H2O(l) ΔH1 ;② CO(OCH3)2(l)+3O2(g)=CO2(g)+H2O(l) ΔH2 ; ①×2-②可得CO2(g)+2CH3OH(l)―→CO(OCH3)2(l)+H2O(l) ΔH =2ΔH1-ΔH2 ; (2) 经过相同的反应时间,温度较低时,反应未达到平衡;温度较高时,反应已达到平衡,随着温度升高,TON减小,即平衡向左移动,说明该反应是放热反应所以ΔH<0; (3)由于在反应开始时,n(CH3OH)=0.25mol;n(催化剂)=0.6×10-5mol;在4h、7 h时的TON分别是20、30,则在这三个小时Δn(CH3OH)=10×0.6×10-5mol=6×10-5mol,所以V(CH3OH)= 6×10-5mol÷0.01L÷3h=2×10-3mol/(L·h);则 4~7 h内DMC的平均反应速率是V(DMC)= 1/2V(CH3OH)= 1×10-3mol/(L·h). 在10 h时,甲醇的TON是35,甲醇的转化物质的量Δn(CH3OH) = 35×0.6×10-5mol=2.1×10-4mol,所以甲醇的转化率是:2.1×10-4mol÷0.25mol=8.4×10-4=8.4×10-2%;(4) a.由甲醇和CO2直接合成DMC,可以利用价廉易得的甲醇把影响环境的温室气体CO2转化为资源,在资源循环利用和环境保护方面都具有重要意义,正确;b.在反应体系中添加合适的脱水剂,即减小生成物的浓度,平衡正向移动,因此将提高该反应的TON[,正确;c.当催化剂用量低于1.2×10-5 mol时,随着催化剂用量的增加,催化剂的催化效果增大,错误;d.当催化剂用量高于1.2×10-5 mol时,随着催化剂用量的增加,催化剂的催化效果急剧下降,错误。只有在催化剂用量等于1.2×10-5 mol时,催化效果最好。
考点:考查盖斯定律的应用、热化学方程式的书写、化学反应速率的计算、温度、反应时间、催化剂的催化效果的影响因素的知识。


科目:高中化学 来源:2015届广东省惠州市高三第一次调研考试化学试卷(解析版) 题型:选择题
无色透明的酸性溶液中,能大量共存的是
A.Na+、K+、CO32-、NO3- B.K+、Fe2+、NH4+、NO3-
C.NH4+、Al3+、SO42-、NO3- D.K+、Na+、NO3-、OH-
查看答案和解析>>
科目:高中化学 来源:2015届安徽省高三九月份化学月考试卷(解析版) 题型:选择题
下列分子或离子中,能提供孤对电子与某些金属离子形成配位键的是
①H2O ②NH3 ③Cl— ④CN— ⑤CO
A.①② B.①②③ C.①②④ D.①②③④⑤
查看答案和解析>>
科目:高中化学 来源:2015届安徽省同步课时练(人教选修4)1.2 燃烧热能源试卷(解析版) 题型:填空题
工业上利用天然气(主要成分为CH4)与CO2进行高温重整制备CO,已知CH4、H2和CO的燃烧热(ΔH)分别为-890.3 kJ·mol-1、-285.8 kJ·mol-1和-283.0 kJ·mol-1,则生成1 m3(标准状况)CO所需热量为 。
查看答案和解析>>
科目:高中化学 来源:2015届安徽省同步课时练(人教选修4)1.2 燃烧热能源试卷(解析版) 题型:选择题
下列热化学方程式中的反应热下划线处表示燃烧热的是( )
A.NH3(g)+O2(g) NO(g)+H2O(g) ΔH=-a kJ·mol-1
NO(g)+H2O(g) ΔH=-a kJ·mol-1
B.C6H12O6(s)+6O2(g) 6CO2(g)+6H2O(l) ΔH=-b kJ·mol-1
6CO2(g)+6H2O(l) ΔH=-b kJ·mol-1
C.2CO(g)+O2(g) 2CO2(g) ΔH=-c kJ·mol-1
2CO2(g) ΔH=-c kJ·mol-1
D.CH3CH2OH(l)+O2(g) CH3CHO(l)+H2O(l) ΔH=-d kJ·mol-1
CH3CHO(l)+H2O(l) ΔH=-d kJ·mol-1
查看答案和解析>>
科目:高中化学 来源:2015届安徽省六校教育研究会高三第一次联考化学试卷(解析版) 题型:选择题
某有机物X的结构简式如下图所示,则下列有关说法中正确的是
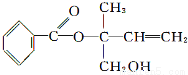
A.X的分子式为C12H16O3
B.X在一定条件下能发生加成、加聚、取代、消去等反应
C.在Ni作催化剂的条件下,1 mol X最多只能与1 mol H2加成
D.可用酸性高锰酸钾溶液区分苯和X
查看答案和解析>>
科目:高中化学 来源:2015届安徽省六校教育研究会高三第一次联考化学试卷(解析版) 题型:选择题
某溶液中可能含有H+、NH4+、Mg2+、Fe3+、Al3+、SO42-、HCO3-等离子。当向该溶液中加入一定物质的量浓度的NaOH溶液时,发现生成沉淀的物质的量随加入NaOH溶液的体积变化如右图所示,
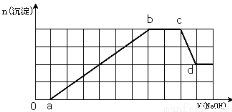
下列说法正确的是
A.d点溶液中含有的溶质只有Na2SO4
B.原溶液中含有的Fe3+和Al3+的物质的量之比为1:1
C.ab段发生的离子反应为:Al3++3OH-= Al(OH)3↓,
Mg2++2OH-= Mg(OH)2↓
D.原溶液中含有的阳离子必定有H+、NH4+、Al3+, 且Mg2+和Fe3+至少存在一种
查看答案和解析>>
科目:高中化学 来源:2015届安徽望江中学同步课时练(人教选修4)4.1原电池试卷(解析版) 题型:选择题
①②③④四种金属片两两相连浸入稀硫酸中都可组成原电池。①②相连时,外电路电流从②流向①;①③相连时,③为正极;②④相连时,②上有气泡逸出;③④相连时,③的质量减少,据此判断这四种金属活动性由大到小的顺序是( )
A.①③②④B.①③④② C.③④②①D.③①②④
查看答案和解析>>
科目:高中化学 来源:2015届安徽师大附中高二下学期期中考查化学试卷(解析版) 题型:选择题
可逆反应aA(g)+bB(g) cC(g)+dD(g)ΔH同时符合下列两图中各曲线的规律的( )
cC(g)+dD(g)ΔH同时符合下列两图中各曲线的规律的( )

A.a+b>c+d T1<T2 ΔH<0
B.a+b>c+d T1<T2 ΔH>0
C.a+b<c+d T1>T2 ΔH<0
D.a+b>c+d T1>T2 ΔH>0
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com