
���� ��1��C�ķ�Ӧ����=$\frac{\frac{��n}{V}}{��t}$��
��2��ͬһ���淴Ӧ��ͬһʱ����ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ���C�ķ�Ӧ���ʼ���A�ķ�Ӧ���ʣ�
��3����ʼ��=������+ijʱ��������ϻ�ѧ����ʽ��ʽ���㣮
��� �⣺��1��C�ķ�Ӧ����=$\frac{\frac{��n}{V}}{��t}$=$\frac{\frac{0.2mol-0}{2L}}{4s}$=0.025mol/��L��s�����ʴ�Ϊ��0.025mol/��L•s����
��2��ͬһ���淴Ӧ��ͬһʱ����ڸ����ʵķ�Ӧ����֮�ȵ����������֮�ȣ�v��A��=2v��C��=0.025mol/��L��s����2=0.05mol/��L•s����
�ʴ�Ϊ��0.05mol/��L•s����
��3��4A��g��+B��g��?2C��g��
��ʼ����mol/L�� c��A�� c��B�� 0
�仯����mol/L�� 0.2 0.05 0.1
ƽ4s����mol/L�� 0.25 0.2 0.1
��ʼ�� c��A��=0.2mol/L+0.25mol/L=0.45mol/L��c��B��=0.05mol/L+0.2mol/L=0.25mol/L
�ʴ�Ϊ��0.45mol/L��0.25mol/L��
���� ���⿼�鷴Ӧ���ʵļ��㣬���ؿ��������������ȷͬһ��Ӧ�в�ͬ���ʷ�Ӧ�������������֮��Ĺ�ϵ�ǽⱾ��ؼ�����Ŀ�ѶȲ���


 ��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д�
��У��ʦ������ҵ���Ӻ����Ծ�ϵ�д� ȫ�̽��ϵ�д�
ȫ�̽��ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | C7H16 | B�� | C5H8O2 | C�� | C4H4O3 | D�� | C6H12O |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �����ͳ�����Ϊͬ�������� | |
| B�� | CH3-CH2OH�� CH3-O-CH3��Ϊͬ���칹�� | |
| C�� | ${\;}_{2}^{3}$He��${\;}_{2}^{4}$He��Ϊͬλ�� | |
| D�� | ${\;}_{2}^{4}$He������������Ϊ2������${\;}_{2}^{3}$He���н�ǿ�Ľ����� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
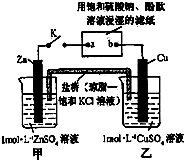
| A�� | Ƭ�̺�ɹ۲쵽��ֽa����ɫ | B�� | ������Zn��a��b��Cu·������ | ||
| C�� | Ƭ�̺�׳���c��SO42-������ | D�� | �����е�Cl-��Cu���ƶ� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | ԭ�Ӱ뾶�Ĵ�С˳��r��W����r��Z����r��Y����r��X�� | |
| B�� | X������������Ӧ��ˮ��������Ա�W���� | |
| C�� | Y����̬���⻯������ȶ��Ա�W��ǿ | |
| D�� | Y�ֱ���Z��W�γɵĻ������л�ѧ��������ͬ |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
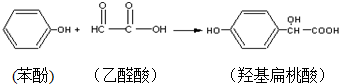
| A�� | ���Ӻ��ǻ������ụΪͬϵ�� | |
| B�� | ��״���£�22.4L�ǻ��������й��õ��ӶԵ���ĿΪ24NA | |
| C�� | ��ȩ��ĺ˴Ź�������ͼֻ��һ��� | |
| D�� | �ǻ������������������12��ԭ�ӹ�ƽ�� |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A | B | C | D | |
| ���� | Fe | Fe | Cu | Cu |
| ���� | Cu | Cu | Fe | Fe |
| �������Һ | CuSO4 | H2SO4 | CuCl2 | �ƾ� |
| A�� | A | B�� | B | C�� | C | D�� | D |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | 496 kJ•mol-1 | B�� | 431 kJ•mol-1 | C�� | 862 kJ•mol-1 | D�� | 248 kJ•mol-1 |
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�ѡ����
| A�� | �٢ڢ� | B�� | �٢ۢ� | C�� | �٢ڢ� | D�� | �٢ڢݢ� |
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com