
����Ŀ��������25��ʱ�������ܵ���ʵ��ܶȼ���ֵ��
���ܵ���� | Mg(OH)2 | Cu(OH)2 | Fe(OH)2 | Fe(OH)3 |
Ksp | 1.0��10-12 | 1.0��10-20 | 1.0��10-16 | 1.0��10-38 |
������������ᴿ�У����������ܵ���ʵ��ܽ�ƽ��ԭ����ȥijЩ���ӡ����磺��Ϊ�˳�ȥ�Ȼ���е�����Fe3�����Ƚ����������ˮ���ټ���һ�������Լ���Ӧ�����˽ᾧ���ɣ���Ϊ�˳�ȥ�Ȼ�þ�����е�����Fe3�����Ƚ����������ˮ������������������þ����ַ�Ӧ�����˽ᾧ���ɣ���Ϊ�˳�ȥ����ͭ�����е�����Fe2�����Ƚ����������ˮ������һ������H2O2����Fe2��������Fe3����������Һ��pH��4�����˽ᾧ���ɡ�
��ش��������⣺
��1�������������ӷ������ܹ��ﵽ�ܺ�Ч����Fe2����Fe3������ת��Ϊ___________(������)����ȥ��
��2�����м�����Լ�Ӧѡ��________Ϊ�ˣ���ԭ����_______________________________��
��3�����г�ȥFe3�����������ܷ�Ӧ�����ӷ���ʽ__________________________________��
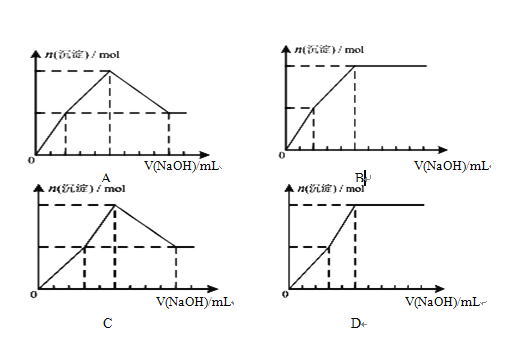
��4�� ��Ũ�Ⱦ�Ϊ0.1mol/L-1��Fe��NO3��3��Cu��NO3��2�����Һ�У���μ���NaOH������ʾ��ͼ��ʾ���ɳ����������ʵ��������NaOH������Ĺ�ϵ������������____��
��5������ijMgCl2��FeCl3��Ϊ0.1 mol��L��1�����Һ�е�pH��MgO������pH��4������Һ��![]() ��ֵԼΪ______________________��
��ֵԼΪ______________________��
���𰸡� �������� ��ˮ ���������µ����� 2Fe3��(aq)��3Mg(OH)2(s)===3Mg2��(aq)��2Fe(OH)3(s) D 107
����������1������Ϊ�˲����������������ӣ�Ӧ�Ӱ�ˮʹFe3+������������������������Һ�����и����ܽ�ȱ���֪Mg(OH)2��ת��ΪFe(OH)3��������Ȼ�þ��Һ�м���������Mg(OH)2�ɳ�ȥFe3+��������Fe(OH)2���ܽ�ȴ���Fe(OH)3������һ�㽫Fe2+��������Fe3+���ٵ�����Һ��pH=4���γ�Fe(OH)3��������2������Ϊ�˲����������������ӣ�Ӧ�Ӱ�ˮʹFe3+������������������������Һ����3�����и����ܽ�ȱ���֪Mg(OH)2��ת��ΪFe(OH)3��������Ȼ�þ��Һ�м���������Mg(OH)2�ɳ�ȥFe3+��2Fe3��(aq)��3Mg(OH)2(s)===3Mg2��(aq)��2Fe(OH)3(s)����������Ksp[Cu(OH)2]����Ksp[Fe(OH)3]�����������Һ�еμ�NaOH��Һʱ������Ӧ����Fe(OH)3��������Fe3+������ȫ��������Cu(OH)2�������ҿ�ʼ�������������ɳ��������ʵ���֮��Ϊ3��1������2��1�������μ�NaOH��Һ�������ܽ⣬��������������ʵ��������NaOH��Һ����Ĺ�ϵ��ѡ��Dͼ�����ʵ���������5��������pH��4ʱc(OH-)=10-10mol/L��![]() ��
��![]() ���ɼ���ʱþ����û������������þ��������Ϊ0.1mol/L������Һ��
���ɼ���ʱþ����û������������þ��������Ϊ0.1mol/L������Һ��![]() =
=![]() =107:1��
=107:1��


 �ŵ������ϵ�д�
�ŵ������ϵ�д�
| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���ѱ���Ϊ��������֮��ĵ����������Ʊ������ѵ�һ���������£�

��1����̬��ԭ�ӵļ۵����Ų�ͼΪ ______________����ԭ�Ӻ����_______���˶�״̬����ͬ�ĵ����� �����Ѿ�����ͼ1��ʾ��Ϊ________ �ѻ�(��ѻ���ʽ)��
��2����֪TiCl4��ͨ�����������ɫҺ�壬�۵�Ϊ-37�����е�Ϊ136�����ݴ˿�֪TiCl4�γɵľ�������Ϊ________��
��3������TiO2��һ��Ӧ�ù㷺�Ĵ����������һ��ʵ����ͼ2���������ҵķе����Ը��ڻ�����ף���Ҫԭ����______________�����������в�ȡsp3�ӻ���ԭ�ӵĵ縺���ɴ�С��˳��Ϊ______________��

��4���������Ѿ�����������Ϊ��״�ۺ���״�����ӣ��ṹ��ͼ3��ʾ����������Ti��O��ԭ����֮��Ϊ___________________���仯ѧʽΪ_________________��
��5�����ѿ���Ľṹ��ͼ4��ʾ��������λ�����������ĽǶ�����_______�������Ӱ�Χ����λ�����壻������λ���������������ģ���_________�������Ӱ�Χ�� ���ѿ���Ļ�ѧʽΪ______________��
 ��
��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��Ϊ������۳���ˮ��BOD���س�������⣬��������˵绯ѧ���ⷨ����ͼ������һ�����ォ�л��ォ��ˮ���л���[��Ҫ�ɷ���(C6H10O5)n]�Ļ�ѧ��ת��Ϊ���ܵ�װ�ã�����˵������ȷ����

A. N���Ǹ���
B. ��װ�ù���ʱ��H+���Ҳྭ�����ӽ���Ĥ�������
C. �����ĵ缫��ӦΪ��(C6H10O5)n+7H2O��24e���T6CO2��+24H+
D. ����X��OH-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��д����Ӧ�����ӷ�Ӧ����ʽ
��1����ĭ�������ԭ��:_____________________________________________________
��2���μ��(���϶�Na2CO3��NaCl)������ֲ���������μ�ز������Ե�ԭ��______________________��ũҵ����ʯ�ཱུ������Եķ�Ӧԭ����____________________��
��3��������ʴ��Ҫ��������ʴ���ø�ʴ�����е������缫��Ӧʽ: ________________��
��4��������Ϊ��������H2SO4��Һ�е�⣬���ı����γ�����Ĥ�������缫��Ӧ����ʽ��____________________________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����֪��25 ��ʱ�����ᡢ�����ᡢ̼���������ĵ���ƽ�ⳣ���ֱ�Ϊ
���� K��1.75��10��5 ������ K��2.95��10��8
̼�� K1��4.0��10��7�� K2��5.0��10��11
������ K1��1.54��10��2�� K2��1.02��10��7
��1�������£�д��̼��ĵ�һ������ƽ�ⳣ������ʽK1��__________,��0.50mol/L��Na2CO3��Һ��pH=________
��2����Ũ�ȵ�Na2CO3��NaHCO3�Ļ����Һ�и�����Ũ�ȴ�С˳��Ϊ_____________��
��3����0.01molL-1CH3COONa��Һ�зֱ��������Ũ���ᡢNa2CO3����ʹˮ��ƽ���ƶ��ķ���ֱ�Ϊ___________��________�������������������������ƶ�����
��4�����ʵ���Ũ�Ⱦ�Ϊ0.1 mol/L��CH3COONa��CH3COOH��Һ�������ϻ��Һ�е����й�ϵʽ��ȷ����________��
A��c(CH3COOH)��2c(OH��)��c(CH3COO��)��2c(H��)
B��c(Na��)��c(H��)��c(CH3COO��)��c(OH��)
C��c(CH3COO��)��c(CH3COOH)��0.2mol/L
D. c(CH3COOH) > c(Na��) > c(CH3COO��) > c(H��) > c(OH��)
��5���������ӷ���ʽ�д������________��
A������CO2ͨ�����������Һ�У�CO2��H2O��ClO��===HCO![]() ��HClO
��HClO
B������SO2ͨ����������Һ�У�2ClO����SO2��H2O===SO32-��2HClO
C��Na2CO3��Һ�м�������NaHSO3��Һ: CO32-+HSO3-=HCO3-+SO32-
D������CO2ͨ������������Һ��: SO32-+CO2+H2O=HSO3-+HCO3-
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������2.8 g Feȫ������һ��Ũ�ȡ�200 mL��HNO3��Һ�У��õ���״���µ�����1.12 L����÷�Ӧ����Һ��pHΪ1������Ӧǰ����Һ����仯���Բ��ƣ��������й��ж���ȷ����
A. ��Ӧ����Һ����Ԫ�ؿ�����Fe2+��ʽ����
B. ��Ӧ�����Һ�����ܽ�1.4 g Fe
C. ��Ӧ����Һ��c(NO3)=0.85 mol��L1
D. 1.12 L���������NO��NO2�Ļ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij������Һ(������ΪNa+)�п��ܺ���SO42-��SO32-��Cl-��Br-��CO32-��HCO3-�е�һ�ֻ���֣���������ͼ��ʾ��ʵ�飬ÿ��ʵ�������Լ�����������֪ϡHNO3����ǿ�����ԡ�����˵������ȷ����( )

A. SO42-��SO32-���ٺ���һ�� B. ����B�Ļ�ѧʽΪ BaCO3
C. �϶����ڵ��������� CO32-��HCO3-��Cl- D. Br���϶�������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ���л���H��һ�ֺϳ�ҩ����м��壬H�ĺϳɷ������£�

��֪�� ![]()
��ش��������⣺
��1��AΪ��Է�������Ϊ104�ķ�������A��ʵ��ʽΪ___________
��2���ɼ���A��C�����л�����Լ�Ϊ�����һ�ּ��ɣ�___________________________
��3��FΪһ�ȴ����˴Ź����������������շ壬��E�Ľṹ��ʽΪ________________
��4��д��B��C�Ļ�ѧ����ʽ____________________________________________________
��5��д��D��G����H�Ļ�ѧ����ʽ_____________________________________________
��6��D��ͬ���칹��������FeCl3��Һ������ɫ��Ӧ���ܷ���������Ӧ����__________�֣�д�����к˴Ź������������շ���Ŀ���ٵĽṹ��ʽ__________________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����������ж�������Ԫ�أ�������ѧ֪ʶ�ж�������������ǣ�������
A.NH3B.HClC.NaHCO3D.CH4
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com