
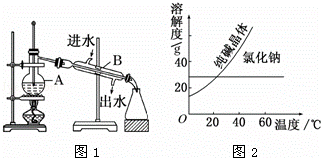
如图为实验室制取蒸馏水的装置示意图,回答下列问题:
(1)图中有两处明显的错误是:
① ;② 冷却水进口、 .
(2)A仪器的名称是 ,B仪器的名称是 .
(3)实验时A中除加入少量自来水外,还需要加入少量的 ,其作用是 .
(4)阅读、分析下列两个材料:
材料1:材料2:
| 物质 | 熔点/℃ | 沸点/℃ | 密度/g/cm | 溶解性 |
| 乙二醇(C2H6O2) | ﹣11.5 | 198 | 1.11 | 易溶于水和乙醇 |
| 丙三醇(C3H8O3) | 17.9 | 290 | 1.26 | 能跟水、乙醇以任意比互溶 |
回答下列问题(填写序号):
A.蒸馏法 B.萃取法 C.“溶解、结晶、过滤”的方法 D.分液法
将纯碱从氯化钠和纯碱的混合物中分离出来,最好应用 .将乙二醇和丙三醇分离的最佳方法是 .(填写A﹣D序号)
考点:
蒸馏与分馏.
专题:
实验题.
分析:
(1)实验室用自来水制取蒸馏水用蒸馏的方法制备,注意温度计水银球应处在蒸馏烧瓶的支管口附近,冷凝管应从下口进水,上口出水,以保证水充满冷凝管,起到充分冷凝的作用;
(2)依据仪器的构造和用途判断解答;
(3)蒸馏过程中,液体加热容易发生爆沸,应加入少量的碎瓷片;
(4)A.蒸馏可用于分离沸点不同的物质;
B.萃取法是利用一种溶质在两种互不相溶的溶剂中溶解度不同,从溶解度小的转移到溶解度大;
C.能用溶解、过滤、蒸发结晶的步骤分离,则混合物中含不溶性物质和可溶性物质,或者溶质在水中的溶解度随温度的变化不同;
D.分液法是用来分离两种互不相溶的密度不同的液体.
解答:
解:(1)温度计水银球应处在蒸馏烧瓶的支管口附近,冷凝管应从下口进水,上口出水,以保证水充满冷凝管,所以图中有两处明显的错误是①温度计水银球在溶液中 ②冷却水进口、出口方向反了;
故答案为:①温度计水银球在溶液中;②冷却水进口、出口方向反了;
(2)A的名称是蒸馏烧瓶 B的名称是冷凝管,故答案为:蒸馏烧瓶;冷凝管;
(3)蒸馏过程中,液体加热容易发生爆沸,应加入少量的碎瓷片防止产生爆沸,故答案为:碎瓷片;防止液体暴沸;
(4)纯碱溶解度随着温度的升高变化很大,氯化钠溶解度随着温度的升高变化不大,所以可以用“溶解、结晶、过滤”的方法分离;
乙二醇和丙三醇沸点不同,相互溶解,可用蒸馏法分离;
故选:C;A.
点评:
本题考查实验室制备蒸馏水操作、分离物质的方法,题目难度不大,本题注意实验操作要点,学习中注意正确操作方法和实验的注意事项.


 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g)⇌C(g)+D(g),下列叙述能表明该反应已达到平衡状态的是()
①混合气体的密度不再变化时
②容器内气体的压强不再变化时
③混合气体的总物质的量不再变化时
④B的物质的量浓度不再变化时
⑤混合气体的平均相对分子质量不再改变的状态
⑥当V正(B)=2V逆(C)
A. ①④⑤⑥ B. ②③⑥ C. ②④⑤⑥ D. 只有④
查看答案和解析>>
科目:高中化学 来源: 题型:
1)气体化合物A分子式可表示为OxFy,已知同温同压下10mL A受热分解生成15mL O2和10mL F2,则A的化学式为
(2)氯气与NaOH溶液吸收的离子方程式为
(3)实验室配制500ml 0.1mol•L﹣1的Na2CO3溶液,回答下列问题:
(a)应用托盘天平称取碳酸钠粉末 g.
(b)配制时应选用的仪器有500ml容量瓶,托盘天平、烧杯、药匙 .
(c)若实验时遇到下列情况,所配溶液的浓度偏大的是 .
A、加水定容时超过刻度线,又吸出少量水至刻度线;
B、忘记将洗涤液转入容量瓶;
C、容量瓶洗涤后内壁有水珠而未作干燥处理;
D、称量碳酸钠粉末时左盘放砝码,右盘放药品;
E、定容时俯视刻度线.
查看答案和解析>>
科目:高中化学 来源: 题型:
下列物质的分离方法中,是利用密度不同达到分离的是( )
|
| A. | 利用蒸发皿,蒸发海水获得海盐 |
|
| B. | 煎中药时用水在煮沸条件下提取中药的有效成分 |
|
| C. | 把大豆磨碎后,用水溶解其中的可溶性成分,经过滤后,分成豆浆和豆渣 |
|
| D. | 沙里淘金 |
查看答案和解析>>
科目:高中化学 来源: 题型:
有K2SO4和Al2(SO4)3的混合溶液,已知其中Al3+的物质的量浓度为0.4mol/L,SO42﹣的物质的量浓度为0.7mol/L,则此溶液中K+的物质的量浓度为( )
|
| A. | 0.1mol/L | B. | 0.15mol/L | C. | 0.2mol/L | D. | 0.25mol/L |
查看答案和解析>>
科目:高中化学 来源: 题型:
把一块钠投入预先滴入2~3滴石蕊试液的水溶液中,可观察到的现象正确的一组为( )
①钠沉到水下面;②钠浮在水面上,四处游动;③钠熔成闪亮的小球,听到滋滋的响声;④溶液变红;⑤溶液变蓝.
|
| A. | ②③⑤ | B. | ①③④ | C. | ①③⑤ | D. | ②③④ |
查看答案和解析>>
科目:高中化学 来源: 题型:
金属镍有广泛的用途.粗镍中含有少量Fe、Zn、Cu、Pt等杂质,可用电解法制备高纯度的镍,下列叙述正确的是(已知:氧化性Fe2+<Ni2+<Cu2+)()
A. 阳极发生还原反应,其电极反应式:Ni2++2e﹣═Ni
B. 电解过程中,阳极质量的减少与阴极质量的增加相等
C. 电解后,溶液中存在的金属阳离子只有Fe2+和Zn2+
D. 电解后,电解槽底部的阳极泥中只有Cu和Pt
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com