
【题目】在2A(g)+B(g)![]() 3C(g)+4D(g)中,表示该反应速率最快的是:
3C(g)+4D(g)中,表示该反应速率最快的是:
A.V(A)=0.5mol·L-1·s-1B.V(B)=0.3mol·L-1·s-1
C.V(C)=0.8mol·L-1·s-1D.V(D)=1mol·L-1·s-1
【答案】B
【解析】
根据化学反应速率之比等于化学计量数之比,把用不同物质表示的反应速率换算成用同一物质表示的化学反应速率,然后比较大小。
在2A(g)+B(g)![]() 3C(g)+4D(g)反应中都换成B的速率进行比较;
3C(g)+4D(g)反应中都换成B的速率进行比较;
A、V(A):V(B)=2:1,V(B)=0.5mol·L-1·s-1/2=0.25 mol·L-1·s-1;
B、V(B)=0.3mol·L-1·s-1;
C、V(B):V(C)=1:3,V(B)=0.8mol·L-1·s-1/3=0.27mol·L-1·s-1;
D、V(B):V(D)=1:4,V(B)=1mol·L-1·s-1/4=0.25 mol·L-1·s-1;
比较可以知道,B表示的反应速率最块,故B正确;故答案选B。


科目:高中化学 来源: 题型:
【题目】某废催化剂含SiO2、ZnO、ZnS和CuS。实验室从该废催化剂中回收锌和铜的一种流程如下图所示。
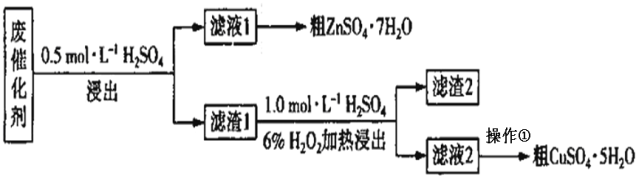
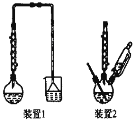
浸出使用的装置如图所示。回答下列问题:
 蒸发浓缩、冷却结晶蒸发浓缩、冷却结晶
蒸发浓缩、冷却结晶蒸发浓缩、冷却结晶
(1)第一次浸出必须选用装置 _______(填“1”或“2”),原因是 ________。滤渣1的主要成分有_______。
(2)第二次浸出时生成单质硫,写出反应的离子方程式:_______________。该步骤即使加热温度不高也可能会有副反应发生,产物之一是空气的主要成分,分析可能原因是_____________________ 。
(3)从滤液2中得到CuSO4·5H2O的操作是 __________ 、过滤、洗涤。
(4)下列叙述中涉及到与该流程中的“操作①”相同操作的是_____________ 。
A.《肘后备急方》中治疟疾:“青蒿一握,以水升渍,绞取汁,尽服之”
B.《本草衍义》中精制砒霜:“将生砒就置火上,以器覆之,令砒烟上飞着覆器”
C.《开宝本草》中获取硝酸钾:“冬月地上有霜,扫取以水淋汁后,乃煎炼而成”
D. 《本草纲目》中烧酒的制造工艺:“凡酸坏之酒,皆可蒸烧”
(5)若该废催化剂中含12.8%的CuS,实验中称取15.0g废催化剂最终得到3.0gCuSO4·5H2O,则铜的回收率为 __________________ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Weiss利用光敏剂QD制备2—环已基苯乙烯(c)的过程如图。下列说法不正确的是( )
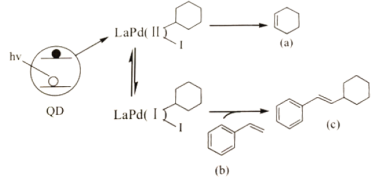
A.a的二氯代物有3种
B.1molb完全燃烧消耗10molO2
C.c具有顺式和反式2种结构
D.a、b、c均能使溴水和稀高锰酸钾溶液褪色
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】电催化合成氨法在电能的推动下不受热力学平衡限制,实现N2、H2O常温常压合成氨,如图为N2在不同电极材料表面复化的机制示意图。下列说法正确的是( )
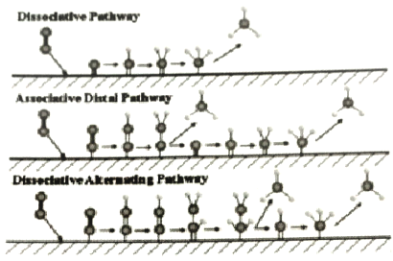
A.电极材料起吸附作用,不影响N2的氢化过程
B.N2在氢化反应之前需先解离成单独的氮原子
C.电催化合成氨原子利用率100%
D.2.8gN2理论上可以产生0.2NA个NH3分子
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】一定温度下,对可逆反应A(g)+2B(g)![]() 3C(g)的下列叙述中,能说明反应已达到平衡的是( )
3C(g)的下列叙述中,能说明反应已达到平衡的是( )
A. C生成的速率与C分解的速率相等
B. 单位时间内消耗amolA,同时生成3amolC
C. 容器内的压强不再变化
D. 混合气体的物质的量不再变化
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】海水是巨大的化学资源宝库,利用海水可以提取很多物质。
利用1:提溴工业
用海水晒盐之后的盐卤可提取溴,提取流程如图:
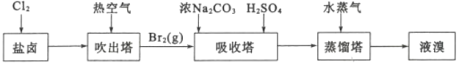
(1)吹出塔中热空气能将溴单质吹出的原因是_____。蒸馏塔中通入水蒸气进行加热,需要控制温度在90℃左右的原因是______。
利用2:提镁工业
从海水提取食盐和Br2之后的盐卤中除含有Mg2+、C1-外,还含有少量Na+、Fe2+、Fe3+、SO42-和CO(NH2)2等,还可以用来提取MgCl2、MgO、Mg(OH)2等物质,流程如图所示:
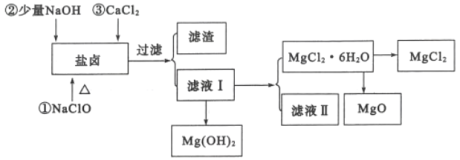
(2)用NaC1O除去尿素CO(NH2)2时,生成物除盐外,还有能参与大气循环的无毒物质,则该反应的化学方程式为_______;加入NaC1O的另一个作用是________。
利用3:淡化工业
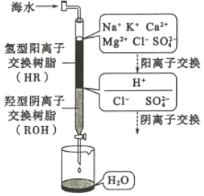
(3)海水淡化的方法主要有闪蒸法、离子交换法、电渗析法等。离子交换法淡化海水模拟过程如图所示。氢型阳离子交换原理可表示为:HR+Na+=NaR+H+;……。羟型阴离子交换树脂填充部分存在的反应有:ROH+C1-=RC1+OH-;______;________。
(4)电渗析法是一种利用离子交换膜进行海水淡化的方法,其原理如图所示:
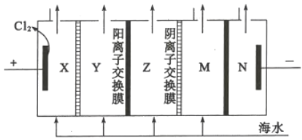
①图中的海水没有直接通入到阴极室中,其原因是_________。
②淡化水在________室(填X、Y、Z、M或N)形成后流出。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列实验操作中选用的部分仪器,不合理的是( )
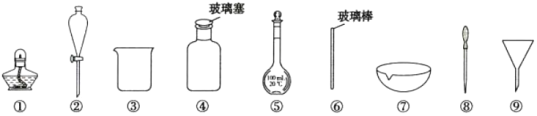
A.配制100 mL0.1 mol·L-1NaC1溶液,选用③、⑤、⑥和⑧
B.盛放NaOH溶液,选用④
C.分离I2的四氯化碳溶液和水,选用②、③
D.从食盐水中获得食盐,选用①、⑥、⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】工业上用发烟HC1O4将潮湿的CrC13氧化为棕色的烟[CrO2(C1O4)2],来除去Cr(Ⅲ),HC1O4中部分氯元素转化为最低价态。下列说法错误的是( )
A.CrO2(C1O4)2中Cr元素显+6价
B.HC1O4属于强酸,该反应还生成了另一种强酸
C.该反应中,参加反应的氧化剂与氧化产物的物质的量之比为3:8
D.该反应离子方程式为19ClO![]() +8Cr3++8OH-=8CrO2(ClO4)2+3C1-+4H2O
+8Cr3++8OH-=8CrO2(ClO4)2+3C1-+4H2O
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】某化学兴趣小组利用硫酸铁溶液与铜粉反应,又向反应后溶液中加入KSCN溶液以检验Fe3+是否有剩余,实验记录如下;
实验编号 | 操作 | 现象 |
实验1 |
| i.加入Cu粉后充分振荡,溶液逐渐变蓝; ii.取少量i中清液于试管中,滴加2滴 0.2mol/LKSCN溶液,溶液变为红色,但振荡后红色迅速褪去并有白色沉淀生成。 |
(1)写出实验1中第i步的离子方程式_______________。甲同学猜想第ii步出现的异常现象是由于溶液中的Cu2+干扰了检验Fe3+的现象。查阅相关资料如下
①2Cu2++4SCN- ![]() 2CuSCN↓(白色)+(SCN)2(黄色)
2CuSCN↓(白色)+(SCN)2(黄色)
②硫氰[(SCN)2]:是一种拟卤素,性质与卤素单质相似,其氧化性介于Br2和I2之间。
该同学又通过如下实验验证猜想
实验编号 | 操作 | 现象 |
实验2 |
| 溶液呈绿色,一段时间后后开始出现白色沉淀,上层溶液变为黄色 |
实验3 |
| 无色溶液立即变红,同时生成白色沉淀。 |
(2)经检测,实验2反应后的溶液pH值减小,可能的原因是___________________________________________。
(3)根据实验2、3的实验现象,甲同学推断实验3中溶液变红是由于Fe2+被(SCN)2氧化,写出溶液变红的离子方程式_______________________。继续将实验2中的浊液进一步处理,验证了这一结论的可能性。
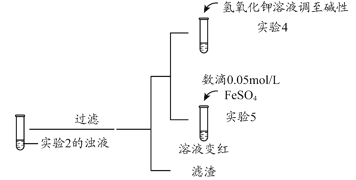
补充实验4的目的是排除了溶液存在Cu2+的可能,对应的现象是____________________________________________。
(4)乙同学同时认为,根据氧化还原反应原理,在此条件下,Cu2+也能氧化Fe2+,他的判断依据是_______。
(5)为排除干扰,小组同学重新设计如下装置。
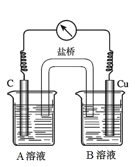
①A溶液为____________________________。
②“电流表指针偏转,说明Cu与Fe3+发生了反应”,你认为这种说法是否合理?__________________(填合理或不合理),原因是__________________________________________。
③验证
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com