
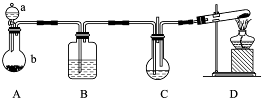
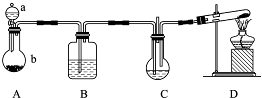
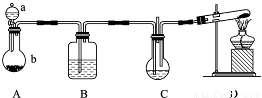
 纳米碳酸钙应用非常广泛.实验室中利用下图所示装置(部分夹持装置已略去),向饱和CaCl2溶液中通入NH3和CO2可制得纳米碳酸钙.
纳米碳酸钙应用非常广泛.实验室中利用下图所示装置(部分夹持装置已略去),向饱和CaCl2溶液中通入NH3和CO2可制得纳米碳酸钙. CaCl2+2NH3↑+2H2O;饱和NaHCO3溶液可除掉挥发出来的氯化氢,故答案为:分液漏斗;CaCO3+2H+=Ca2++H2O+CO2↑;2NH4Cl+Ca(OH)2
CaCl2+2NH3↑+2H2O;饱和NaHCO3溶液可除掉挥发出来的氯化氢,故答案为:分液漏斗;CaCO3+2H+=Ca2++H2O+CO2↑;2NH4Cl+Ca(OH)2 CaCl2+2NH3↑+2H2O; ⑧;
CaCl2+2NH3↑+2H2O; ⑧;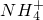 +H2O
+H2O NH3?H2O+H+,故答案为:酸;
NH3?H2O+H+,故答案为:酸; 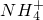 +H2O
+H2O NH3?H2O+H+;
NH3?H2O+H+;

 桃李文化快乐暑假武汉出版社系列答案
桃李文化快乐暑假武汉出版社系列答案 优秀生快乐假期每一天全新寒假作业本系列答案
优秀生快乐假期每一天全新寒假作业本系列答案 暑假接力赛新疆青少年出版社系列答案
暑假接力赛新疆青少年出版社系列答案科目:高中化学 来源: 题型:
 (2012?济南二模)纳米碳酸钙应用非常广泛.实验室中利用下图所示装置(部分夹持装置已略去),向饱和CaCl2溶液中通入NH3和CO2可制得纳米碳酸钙.
(2012?济南二模)纳米碳酸钙应用非常广泛.实验室中利用下图所示装置(部分夹持装置已略去),向饱和CaCl2溶液中通入NH3和CO2可制得纳米碳酸钙.
| ||
| ||
| H | + 4 |
| ||
| H | + 4 |
| ||
查看答案和解析>>
科目:高中化学 来源: 题型:阅读理解
| 1 |
| 2 |
| 1 |
| 2 |
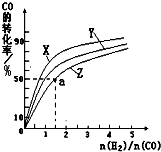
| 0min | 5min | 10min | |
| CO | 0.1 | 0.05 | |
| H2 | 0.2 | 0.2 | |
| CH3OH | 0 | 0.04 | 0.05 |
查看答案和解析>>
科目:高中化学 来源:济南二模 题型:问答题
查看答案和解析>>
科目:高中化学 来源:2012年山东省济南市高考化学二模试卷(解析版) 题型:解答题
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com