
右图是NaCl、MgSO4的溶解度曲线。下列说法正确的是( )
A.只有在t1 ℃时,NaCl和MgSO4的溶解度才相等
B.t1~t2 ℃,MgSO4的溶解度随温度升高而减小
C.在t2 ℃时,MgSO4饱和溶液的溶质质量分数最大
D.把MgSO4饱和溶液的温度从t3 ℃降至t2 ℃时,有晶体析出
 各地期末复习特训卷系列答案
各地期末复习特训卷系列答案 小博士期末闯关100分系列答案
小博士期末闯关100分系列答案 名校名师培优作业本加核心试卷系列答案
名校名师培优作业本加核心试卷系列答案科目:高中化学 来源: 题型:
下面的表格是元素周期表的一部分,其中的序号对应的是元素。

请回答下列问题:
(1) 按原子轨道的重叠方式看,元素①③形成的相对分子质量最小的分子中,含 键;元素⑤和⑧形成的化合键类型为 。
(2) 某元素的价电子排布式为 ,该元素与元素①形成的气态化合物分子的空间构型为 。
,该元素与元素①形成的气态化合物分子的空间构型为 。
(3) 表中某元素最外电子层上p电子数比s电子数少1,则该元素的元素符号为
(4) ②④⑤⑥四种元素的第一电离能由大到小的顺序是(填序号) 。
(5) 元素⑨的价电子排布式为 。
查看答案和解析>>
科目:高中化学 来源: 题型:
将10.6 g Na2CO3溶于水配成1 L溶液
(1)该溶液中Na2CO3的物质的量浓度为__________,溶液中Na+的物质的量浓度为__________。
(2)向该溶液中加入一定量NaCl固体,使溶液中Na+的物质的量浓度为0.4 mol·L-1(假设溶液体积不变)需加入NaCl的质量为__________,Cl-的物质的量浓度为________________________________________________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
标准状况下V L氨气溶解在1 L水中(水的密度近似为1 g·mL-1),所得溶液的密度为ρ g·mL-1,质量分数为w,物质的量浓度为c mol·L-1,则下列关系中不正确的是 ( )
A.ρ=(17V+22 400)/(22.4+22.4V)
B.w=17c/(1 000ρ)
C.w=17V/(17V+22 400)
D.c=1 000Vρ/(17V+22 400)
查看答案和解析>>
科目:高中化学 来源: 题型:
在a L Al2(SO4)3和(NH4)2SO4的混合溶液中加入b mol BaCl2,恰好使溶液中的SO 完全沉淀;如加入足量强碱并加热可得到 c mol NH3,则原溶液中Al3+的浓度(mol·L-1)为
完全沉淀;如加入足量强碱并加热可得到 c mol NH3,则原溶液中Al3+的浓度(mol·L-1)为
( )
A. B.
B. C.
C. D.
D.
查看答案和解析>>
科目:高中化学 来源: 题型:
已知硫酸、氨水的密度与所加水的量的关系如图所示,现有硫酸与氨水各一份,请根据表中信息,回答下列问题:
| 溶质的物质的量 浓度/mol·L-1 | 溶液的密度 /g·cm-3 | |
| 硫酸 | c1 | ρ1 |
| 氨水 | c2 | ρ2 |

(1)表中硫酸的质量分数为________(不写单位,用含c1、ρ1的代数式表示)。
(2)物质的量浓度为c1 mol·L-1的硫酸与水等体积混合(混合后溶液的体积变化忽略不计),所得溶液的物质的量浓度为________ mol·L-1。
(3)将物质的量浓度分别为c2 mol·L-1和 c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________
c2 mol·L-1的氨水等质量混合,所得溶液的密度________(填“大于”、“小于”或“等于”,下同)ρ2 g·cm-3,所得溶液的物质的量浓度________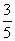 c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
c2 mol·L-1(设混合后溶液的体积变化忽略不计)。
查看答案和解析>>
科目:高中化学 来源: 题型:
一定温度下,在固定体积的密闭容器中发生下列反应:2HI(g)=H2(g)+I2(g)若C(HI) 由0.1mol/L降到0.07mol/L时,需要15S,那么C(HI)由0.07mol/L降到0.05mol/L时,所需反应时间为( )
A.等于5S B.等于10S C 大于10S D小于10S
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com