
����Ŀ����������Ũ�Ⱦ�Ϊ0.5 mol/L��������Һ��
��Na2CO3����NaHCO3����HCl����NH3��H2O
(1)������Һ�У��ɷ���ˮ�����______(����ţ���ͬ)��
(2)������Һ�У��������������Ʒ�Ӧ�����ܺ����ᷴӦ����Һ������Ũ���ɴ�С��˳��Ϊ��_______________��
(3)����м��������Ȼ�粒��壬��ʱ![]() ��ֵ________(����������������С��������������)��
��ֵ________(����������������С��������������)��
(4)�����ۺܵ͢���Һ��Ϻ���Һǡ�ó����ԣ�����ǰ�۵����________�ܵ����(��������������С��������������)
(5)ȡ10 mL��Һ�ۣ���ˮϡ�͵�500 mL�����ʱ��Һ����ˮ�������c(H��)��________��
���𰸡��٢� c(Na+)��c(HCO3-)��c(OH-)��c(H+)��c(CO32-) ���� С�� 10-12mol/L
��������
��Na2CO3=2Na++CO32-��CO32-��H2O![]() HCO3-��OH-��HCO3-��H2O
HCO3-��OH-��HCO3-��H2O![]() H2CO3+OH-��
H2CO3+OH-��
��NaHCO3=Na++HCO3-��HCO3-![]() H++CO32-��HCO3-+H2O
H++CO32-��HCO3-+H2O![]() H2CO3+OH-��
H2CO3+OH-��
��HCl=H++Cl-��
��NH3��H2O![]() NH4++OH-��
NH4++OH-��
(1)�ӷ����ɿ�����������Һ�У��ɷ���ˮ�����Na2CO3��NaHCO3��
(2)������Һ�У��������������Ʒ�Ӧ�����ܺ����ᷴӦ��ΪNaHCO3��
(3)����м��������Ȼ�粒��壬NH3��H2O![]() NH4++OH-�ĵ���ƽ�������ƶ���c(NH4+)����c(OH��)��С��
NH4++OH-�ĵ���ƽ�������ƶ���c(NH4+)����c(OH��)��С��
(4)�����ۺܵ͢���Һ��������ʱ������NH4Cl����ʱ��Һ�����ԣ�����Ҫʹ��Һ�����ԣ����ټ���һ������NH3��H2O��
(5)ȡ10 mL��Һ�ۣ���ˮϡ�͵�500 mL����ʱ��Һ����ˮ�������c(H��)��c(OH-)H2O= c(OH-)aq��
(1)�����Ϸ����ɿ�������Na2CO3����NaHCO3����HCl����NH3��H2O�ķ���Һ�У��ɷ���ˮ�����Na2CO3��NaHCO3����Ϊ���٢ڣ�
(2)������Һ�У��������������Ʒ�Ӧ�����ܺ����ᷴӦ��ΪNaHCO3����Һ������HCO3-��ˮ�⣬����Ũ��С��Na+��HCO3-�ȵ��룬��ˮ�⣬ˮ��̶ȴ��ڵ���̶ȣ�������Һ�Լ��ԣ�����Һ������Ũ�ȴ�С˳��Ϊc(Na+)��c(HCO3-)��c(OH-)��c(H+)��c(CO32-)���ʴ�Ϊ��c(Na+)��c(HCO3-)��c(OH-)��c(H+)��c(CO32-)��
(3)����м��������Ȼ�粒��壬NH3��H2O![]() NH4++OH-�ĵ���ƽ�������ƶ���c(NH4+)����c(OH��)��С��
NH4++OH-�ĵ���ƽ�������ƶ���c(NH4+)����c(OH��)��С��![]() ����Ϊ������
����������
(4)�����ۺܵ͢���Һ��������ʱ������NH4Cl����ʱ��Һ�����ԣ�����Ҫʹ��Һ�����ԣ����ټ���һ������NH3��H2O������ǰ�۵����С�ڢܵ��������Ϊ��С�ڣ�
(5)��Һ��c(H��)=![]() =0.01mol/L������Һ��c(OH-)=
=0.01mol/L������Һ��c(OH-)=![]() =10-12mol/L���Ӷ��ó���ʱ��Һ����ˮ�������c(H��)��10-12mol/L����Ϊ��10-12mol/L��
=10-12mol/L���Ӷ��ó���ʱ��Һ����ˮ�������c(H��)��10-12mol/L����Ϊ��10-12mol/L��



| �꼶 | ���пγ� | �꼶 | ���пγ� |
| ��һ | ��һ��ѿγ��Ƽ��� | ��һ | ��һ��ѿγ��Ƽ��� |
| �߶� | �߶���ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
| ���� | ������ѿγ��Ƽ��� | ���� | ������ѿγ��Ƽ��� |
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����![]() ���������ӵ�������ֵ������������ȷ���ǣ� ��
���������ӵ�������ֵ������������ȷ���ǣ� ��
A.��![]() ͨ��
ͨ��![]() ʹ������
ʹ������![]() ʱ����Ӧ��ת�Ƶ�����Ϊ
ʱ����Ӧ��ת�Ƶ�����Ϊ![]()
B.��![]() ͨ�뵽ˮ�У���
ͨ�뵽ˮ�У���![]()
C.���³�ѹ�£�![]() ����ȩ
����ȩ![]() �ı������к��е�ԭ������Ϊ
�ı������к��е�ԭ������Ϊ![]()
D.![]() ��
��![]() �к��е�
�к��е�![]() ����Ϊ
����Ϊ![]()
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����¶Ի�ѧ��Ӧ�����Ĺ۵�����ȷ���м���ٷ��ȷ�Ӧ�ڳ����¾����Է����У��ڵ������У���ѧ��ת��Ϊ���ܶ�����������������ԭ��ع���ʱ�������ķ�Ӧһ����������ԭ��Ӧ���ܼ���ʱ����ѧ��Ӧֻ�����ȷ�Ӧ������У���������ܷ���ˮ�ⷴӦ������ͬ�¶��£�ͬһ��Ӧ�Ļ�ѧƽ�ⳣ���Ĵ�С�뻯ѧ��Ӧ����ʽ����д�й�( )
A.1��B.2��C.3��D.4��
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������������̼�ܵȲ��������Ķ��ε��ԭ����ͼ��ʾ������˵����ȷ����(����)

A.���ʱ�������ĵ缫��ӦΪNi(OH)2��OH����e��=NiO(OH)��H2O
B.�ŵ�ʱ�������ĵ缫��ӦΪH2��2e����2OH��=2H2O
C.�ŵ�ʱ��OH���������缫
D.���ʱ������ص�̼�缫�����Դ����������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ������������ȷ����
A.�����£���ϡ��ˮ��μ���ϡ�����У�����Һ��![]() ʱ��
ʱ��![]()
B.���ִ�����Һ�����ʵ���Ũ�ȷֱ�Ϊ![]() ��
��![]() ��pH�ֱ�Ϊa��
��pH�ֱ�Ϊa��![]() ����
����![]()
C.�����£�![]() ��NaOH��Һ��
��NaOH��Һ��![]() �Ĵ�����Һ�������ϣ�����ʯ����Һ�ʺ�ɫ
�Ĵ�����Һ�������ϣ�����ʯ����Һ�ʺ�ɫ
D.��![]() �İ�ˮ�м�����������粒��壬����Һ��
�İ�ˮ�м�����������粒��壬����Һ��![]() ��ֵ����
��ֵ����
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ����ͼ��ʾ��ijͬѧ���һ������(CH3OCH3)ȼ�ϵ�ز�̽���ȼҵԭ���ʹ�ͭ�ľ���ԭ����������װ����XΪ�����ӽ���Ĥ��

(1)д�������ĵ缫��Ӧʽ________________________������
(2)ʯī�缫(C)�ĵ缫��ӦʽΪ___________________��
(3)��Ӧһ��ʱ�����װ��������NaOH��Ҫ�� __________(��������������ʯī����)����
(4)�����ͭ�к���п���������ʣ���װ����п���ڽ���ͭ�ŵ������Һ����Ӧһ��ʱ�䣬����ͭ��ҺŨ�Ƚ�_________ (����������������С������������)
(5)���ڱ�״���£���2.24L�����μӷ�Ӧ��������װ�������缫�����ɵ������ڱ�״���µ����Ϊ__________________
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ�����л�ѧʵ�����ע�ⰲȫ��������������ȷ���ǣ� ��
A.������Ũ��մ��Ƥ���ϣ������ô���ˮ��ϴ����Ϳ��![]() ��������Һ
��������Һ
B.�ڵ�ȼ����ȿ�ȼ����ǰ�����䴿�ȣ���ֹ������ը
C.������ȼ�յľƾ��������Ӿƾ�
D.��ȼ���Ż�Ӧ�ø����ɳ������
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��25 �棬c(HCN)+c(CN-)=0.1 mol��L��1��һ��HCN��NaCN�Ļ����Һ����Һ�� c(HCN)��c(CN-)��pH�Ĺ�ϵ��ͼ��ʾ�������й�����Ũ�ȹ�ϵ������ȷ����( )
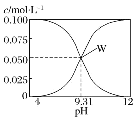
A.�� 0.1 mol��L��1 �� HCN ��Һ�� 0.1 mol��L��1NaCN��Һ��������(������Һ����仯)��c(Na��)>c(HCN)>c(CN��)>c(OH��)>c(H��)
B.W ���ʾ��Һ�У�c(Na��)=c(HCN)+c(CN-)
C.pH=8����Һ�У�c(Na��)+c(H��)+c(HCN)=0.1 mol��L-1+c(OH-)
D.��0.3 mol��L��1 HCN��Һ��0.2 mol��L��1NaOH��Һ��������(������Һ����仯)��c(CN-)+3c(OH-)=c(HCN)+3c(H��)
�鿴�𰸺ͽ���>>
��Ŀ�����л�ѧ ��Դ�� ���ͣ�
����Ŀ��ij��Һ�п��ܺ������ӣ�K+��Na+��Fe2+��Fe3+��SO32-��SO42-������Һ�и����ӵ����ʵ�����ȣ�������Һ��Ϊ���ݣ�һ�ݼӸ��������Һ������Ϊ��ɫ��ȥ����һ�ݼ��Ȼ�����Һ��������������ˮ�ij���������˵����ȷ���ǣ� ��
A.����Һ�к��������������ܺ���K+
B.����Һ�к��������������һ������K+
C.��Һ�п��ܺ���Fe3+
D.��Һ��һ������Fe2+��SO42-
�鿴�𰸺ͽ���>>
����ʡ������Υ���Ͳ�����Ϣ�ٱ�ƽ̨ | �����к���Ϣ�ٱ�ר�� | ����թƭ�ٱ�ר�� | ����ʷ���������к���Ϣ�ٱ�ר�� | ������Ȩ�ٱ�ר��
Υ���Ͳ�����Ϣ�ٱ��绰��027-86699610 �ٱ����䣺58377363@163.com