
【题目】读下列药品标签,有关分析不正确的是( )
选项 | A | B | C | D |
物品标签 |
|
|
|
|
分析 | 该试剂应装在橡 胶塞的细口瓶中 | 该药品不能与皮肤直接接触 | 受热易分解 | 该药品标签上还标有 |
A.A
B.B
C.C
D.D
科目:高中化学 来源: 题型:
【题目】在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8(过二硫酸铵)溶液会发生如下反应:Mn2++S2O82﹣+H2O→MnO4﹣+SO42﹣+H+ , 下列说法不正确的是( )
A.可以利用该反应检验Mn2+
B.氧气性比较:S2O82﹣>MnO4﹣
C.该反应中酸性介质可以为盐酸
D.若有0.1mol氧化产物生成,则转移电子0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各物质的性质比较正确的是
A. 酸性:H2SiO3 > H3PO4B. 氧化性:Cl2 > F2
C. 稳定性:H2S > HFD. 碱性:NaOH > Al(OH)3
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在酸性介质中,往MnSO4溶液里滴加(NH4)2S2O8(过二硫酸铵)溶液会发生如下反应:Mn2++S2O82﹣+H2O→MnO4﹣+SO42﹣+H+ , 下列说法不正确的是( )
A.可以利用该反应检验Mn2+
B.氧气性比较:S2O82﹣>MnO4﹣
C.该反应中酸性介质可以为盐酸
D.若有0.1mol氧化产物生成,则转移电子0.5mol
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】Ag2CrO4在水中的沉淀溶解平衡曲线如图所示,t℃时,反应Ag2CrO4(s)+2Cl﹣(aq)=2AgCl(s)+CrO42﹣(aq)的K=2.5×107 , 下列说法正确的是( )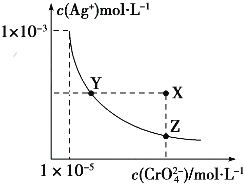
A.t℃时,Ag2CrO4的Ksp为1×10﹣12
B.t℃时,向饱和Ag2CrO4溶液中加入K2CrO4溶液,再次平衡时c2(Ag+)×c(CrO42﹣)>Ksp
C.t℃时,Ksp(AgCl)=1.56×10﹣10
D.t℃时,用0.01molL﹣1 AgNO3溶液滴定20mL 0.01molL﹣1KCl和0.01mol K2CrO4的混合溶液,CrO42﹣先沉淀
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列各组数据中,前者刚好是后者两倍的是( )
A.2 mol水的摩尔质量和1 mol水的摩尔质量
B.200 mL 1 mol/L氯化钙溶液中c(Cl﹣)和100 mL 2 mol/L氯化钾溶液中c(Cl﹣)
C.64 g二氧化硫中氧原子数和标准状况下22.4 L一氧化碳中氧原子数
D.20%NaOH溶液中NaOH的物质的量浓度和10%NaOH溶液中NaOH的物质的量浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列说法错误的是( ) ①NaHCO3溶液加水稀释,c(Na+)/c(HCO3﹣)的值保持增大
②浓度均为0.1molL﹣1的Na2CO3、NaHCO3混合溶液:2c(Na+)=3[c(CO32﹣)+c(HCO3﹣)]
③在0.1molL﹣1氨水中滴加0.lmolL﹣1盐酸,恰好完全反应时溶液的pH=a,则由水电离产生的c(OH﹣)=l0﹣amolL﹣1
④向0.1molL﹣1(NH4)2SO3溶液中加入少量NaOH固体,c(Na+)、c(NH4+)、c(SO32﹣)均增大
⑤在Na2S稀溶液中,c(OH﹣)=c(H+)+2c(H2S)+c(HS﹣)
A.①④
B.②④
C.①③
D.②⑤
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】铝镁合金是制造飞机的重要材料。为测定己除去表面氧化膜的某铝镁合金(假设不含共他元素)镁的质量分数,学习小组同学设计了如下两种实验方案。
(1)[方案1]准确称最ag铝镁合金样品与足量NaOH溶液反应,经过滤、洗涤、干燥后,称量剩余固体的质量。该样品与NaOH溶液反应的化学方程式是。若剩余固体质量为bg,则铝镁合金中镁的质量分数是(列出计算式即可)。若未洗涤过滤后的滤渣,则最终测量结果是。( 填“偏低、偏高、不影响” )。
[方案2]将铝镁合金与足量稀硫酸溶液反应,测定生成气体的体积。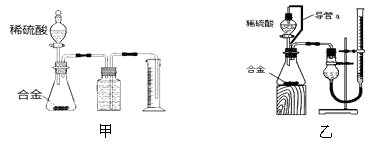
(2)同学们选用甲装置进行实验:实验开始时,先打开分液漏斗上口的玻璃塞,再轻轻打开其活塞,一会儿后稀硫酸就不能顺利滴入锥形瓶。请你帮助分析原因是。
(3)同学们经讨论认为甲装置有两个方面会引起较大误差,分别是和。
(4)于是他们设计了实验装置乙。乙中导管a的作用是。若实验前后滴定管中液面读数分别为V1mL、V2mL。则产生氢气的体积为mL。
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com