某校化学兴趣小组为探究铁与浓硫酸的反应,设计了图1、图2所示装置进行实验.
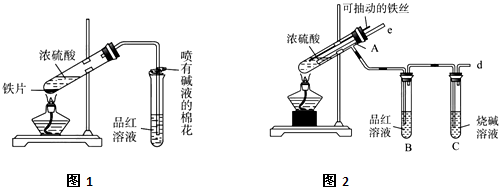
(1)比较两个实验装置,图2装置的优点是:
①能更好的吸收有毒气体SO
2防止其污染环境;
②
便于控制反应的发生和停止
便于控制反应的发生和停止
.
(2)导气管e有两个主要作用:一是在反应过程中,因导管插入液面下,可起到”液封”作用阻止SO
2气体逸出而防止污染环境;二是
停止加热时,能防止倒吸或平衡压强
停止加热时,能防止倒吸或平衡压强
.
(3)能说明有SO
2气体产生的实验现象是
品红溶液褪色
品红溶液褪色
.
(4)反应一段时间后,用滴管吸取A试管中的溶液滴入到适量水中作为试样,试样中所含金属离子的成分有以下三种可能:
Ⅰ:只含有Fe
3+;
Ⅱ:只含有Fe
2+;
Ⅲ:既有Fe
3+又有Fe
2+.
为验证Ⅱ、Ⅲ的可能性,选用如下试剂,填写下列空格:
A.稀HCl溶液 B.稀硫酸 C.KSCN溶液 D.酸性KMnO
4溶液
E.NaOH溶液 F.淀粉KI溶液 G.H
2O
2溶液
验证Ⅱ:取试样,先滴加少量的
C
C
(填试剂序号,下同),振荡,再滴加少量的
G
G
,根据溶液颜色的变化可确定假设Ⅱ是否正确.
验证Ⅲ:步骤1.取试样,滴加少量的
C(或F)
C(或F)
(填试剂序号),溶液的颜色变
红(或蓝)
红(或蓝)
色,则试样中含有Fe
3+发生反应的离子方程式为
Fe3++3SCN-═Fe(SCN)3或2I-+2Fe3+=I2+2Fe2+
Fe3++3SCN-═Fe(SCN)3或2I-+2Fe3+=I2+2Fe2+
.
步骤2.再取适量的试样滴加少量的
D
D
(填试剂序号),溶液颜色的变化为
酸性KMnO4溶液的浅红色褪去
酸性KMnO4溶液的浅红色褪去
,则试样中含有Fe
2+.

 鹰派教辅衔接教材河北教育出版社系列答案
鹰派教辅衔接教材河北教育出版社系列答案 初中暑期衔接系列答案
初中暑期衔接系列答案
