
 与
与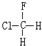 B.
B.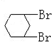 与
与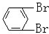 C.
C.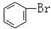 与
与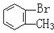 D.
D.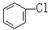 与
与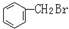 E.ClC(CH3)3与(CH3)2CHCH2Cl F.
E.ClC(CH3)3与(CH3)2CHCH2Cl F.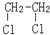 与CH3-CH2Cl.
与CH3-CH2Cl. 分析 同系物指结构相似、通式相同,组成上相差1个或者若干个CH2原子团,具有相同官能团的化合物;
具有相同分子式而结构不同的化合物互为同分异构体;
组成和结构都相同的物质为同一物质,同一物质组成、结构、性质都相同,结构式的形状及物质的聚集状态可能不同.
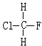
解答 解:A. 与
与 是空间四面体,结构相同,属于同一种物质;
是空间四面体,结构相同,属于同一种物质;
B. 与
与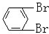 分子式不同,结构也不同,不是同分异构体,也不是同系物,更不是同种物质;
分子式不同,结构也不同,不是同分异构体,也不是同系物,更不是同种物质;
C. 与
与 通式相同,结构相似,相差1个CH2原子团,互为同系物;
通式相同,结构相似,相差1个CH2原子团,互为同系物;
D. 与
与 分子式不同,官能团不同,不是同分异构体,也不是同系物,更不是同种物质;
分子式不同,官能团不同,不是同分异构体,也不是同系物,更不是同种物质;
E.ClC(CH3)3与(CH3)2CHCH2Cl 分子式相同,结构不同,为碳链异构,互为同分异构体;
F.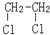 与CH3-CH2Cl分子式不同,官能团个数不同,不是同分异构体,也不是同系物,更不是同种物质,
与CH3-CH2Cl分子式不同,官能团个数不同,不是同分异构体,也不是同系物,更不是同种物质,
故答案为:C;E;A.
点评 本题考查“三同”比较,难度不大,侧重考查学生的辨别能力,根据概念逐项判断即可.


科目:高中化学 来源: 题型:选择题
| A. | 放电过程中KOH的物质的量浓度不变 | |
| B. | 负极反应为14H2O+7O2+28e-=28OH- | |
| C. | 放电一段时间后,负极周围的pH升高 | |
| D. | 每消耗1mol C2H6,则电路上转移的电子为14mol |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 使pH试纸显深蓝色的溶液:Na+、K+、I-、NO${\;}_{3}^{-}$ | |
| B. | 0.1mol•L-1的Ca(ClO)2溶液:K+、Na+、I-、Cl- | |
| C. | 能使甲基橙显红色的溶液:K+、Fe2+、Cl-、NO${\;}_{3}^{-}$ | |
| D. | 加KSCN显红色的溶液:Na+、Mg2+、I-、SO${\;}_{4}^{2-}$ |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
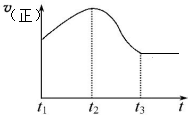 四种短周期元素在周期表中的相对位置如下所示,其中Y元素原子最外层电子数是其电子层数的3倍.
四种短周期元素在周期表中的相对位置如下所示,其中Y元素原子最外层电子数是其电子层数的3倍.| X | Y | |
| Z | W |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 3种 | B. | 4种 | C. | 5种 | D. | 6种 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
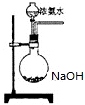 氨在国民经济中占有重要地位.
氨在国民经济中占有重要地位.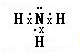 .
.查看答案和解析>>
科目:高中化学 来源: 题型:填空题
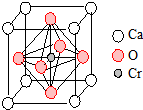 重铬酸钾(K2Cr2O7)是一种重要的氧化剂,可以检验司机是否酒后驾驶.
重铬酸钾(K2Cr2O7)是一种重要的氧化剂,可以检验司机是否酒后驾驶.查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 在c(H+)=1.0×10-13 mol•L-1的溶液中:Na+、S2-、AlO2-、SO32- | |
| B. | pH<7的溶液中:SO42-、CO32-、Na+、K+ | |
| C. | 有NO3-存在的强酸性溶液中:NH4+、Ba2+、Fe2+、Br- | |
| D. | 在pH=1的溶液中:NH4+、K+、ClO-、Cl- |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com