
| 实验编号 | 盐酸体积( mL ) | 标准NaOH溶液的体积(mL) |
| 1 | 20.00 | 18.20 |
| 2 | 17.10 | |
| 3 | 16.90 |
| c(标准)×V(标准) |
| V(待测) |
| 17.10+16.90 |
| 2 |
| c(标准)×V(标准) |
| V(待测) |
| 0.5mol/L×0.01700L |
| 0.0200L |


科目:高中化学 来源: 题型:
| A、常用丁达尔效区分溶液与胶体 |
| B、在铜锌原电池中,负极上发生Zn-2e-═Zn2+ |
| C、常温下,稀释0.1 mol/L的氨水,溶液中c(OH-)、c(NH4+)、c(H+)均减少 |
| D、向AgCl沉淀中滴加KI溶液,沉淀变为黄色,说明Ksp(AgCl)>Ksp(AgI) |
查看答案和解析>>
科目:高中化学 来源: 题型:

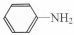 与DMC1:1发生类似反应①的反应,请写出反应方程式
与DMC1:1发生类似反应①的反应,请写出反应方程式查看答案和解析>>
科目:高中化学 来源: 题型:
| 滴定序号 | 待测溶液体积(单位:mL) | 所消耗盐酸体积(单位:mL) | ||
| 滴定前读数 | 滴定后读数 | 消耗盐酸体积 | ||
| 1 | 20.00 | 0.50 | 20.60 | V(平)= |
| 2 | 20.00 | 6.00 | 26.00 | |
| 3 | 20.00 | 4.50 | 24.50 | |
查看答案和解析>>
科目:高中化学 来源: 题型:

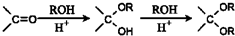
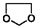 的合成路线流程图(无机试剂任选).
的合成路线流程图(无机试剂任选).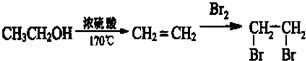
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、OH-、SO42-、Fe3+ |
| B、NH4+、OH-、NO3- |
| C、Na+、Cl-、SO42- |
| D、H+、HCO3-、K+ |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、制备Fe(OH)3胶体的方法是在浓FeCl3溶液中加入大量浓NaOH溶液,并不断搅拌 |
| B、Fe(OH)3胶体中的胶体粒子大小在1~100nm之间 |
| C、可用丁达尔效应区分Fe(OH)3胶体和蔗糖溶液 |
| D、当光束通过有尘埃的空气或稀豆浆时都能观察到丁达尔效应 |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、Al起始反应的离子方程式为2Al+6H+=2Al3++3H2↑ |
| B、滤液I中一定含有Cu2+、Al3+;一定含有Fe2+和Fe3+中的一种或两种 |
| C、滤渣I的主要成分是Au与Pt,由此可以回收贵重的金属 |
| D、加入稀硫酸可以提高硝酸的利用率,使硝酸根离子完全反应 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com