
(1) 将一定量的Fe粉、Cu粉、FeCl3溶液、CuCl2溶液混合于某容器中充分反应(假定容器不参与反应),判断下列情况下容器中金属离子与金属单质的存在情况:(用符号表示)
①若Fe粉有剩余,则容器中不可能有____________;
②若FeCl3有剩余,则容器中不可能有___________;
③若CuCl2有剩余,则容器中还可能有____________
(2)有一瓶无色澄清溶液,可能含NH4+、K+、Na +、Mg2+、Ba2+、 Al3+、 Fe3+、SO42-、CO32-、Cl-、I-中的一种或几种,取该溶液进行如下实验:
①用pH试纸检验,表明溶液呈酸性;
②取部分溶液,加入少量CCl4及数滴新制的氯水,经振荡后静置,CCl4层呈紫红色;
③取部分溶液,逐滴加入稀NaOH溶液,使溶液从酸性逐渐转变为碱性,在滴加过程中及滴加完毕后,溶液中均无沉淀生成;
④取部分上述呈碱性的溶液,加Na2CO3溶液,有白色沉淀生成;
⑤将③得到的碱性溶液加热,有气体放出,该气体能使湿润的红色石蕊试纸变蓝。
根据上述实验事实确定并回答:在溶液中肯定存在的离子有 ,肯定不存在的离子有 ,要确定是否存在的阴离子的实验方法是____________ 。
 名校课堂系列答案
名校课堂系列答案科目:高中化学 来源: 题型:
下列各组物质中,化学键的类型相同的是 ( )
A. HCl、MgCl2、NH4Cl B. H2O、Na2O、CO2
C. CaCl2、NaOH、H2O D. NH3、H2O、CO2
查看答案和解析>>
科目:高中化学 来源: 题型:
海水中富含镁,可经过加碱沉淀、过滤、酸溶、结晶及脱水等步骤得到无水氯化镁,
最后电解得到金属镁。
(1)加碱沉淀镁离子时,生成的Mg(OH)2在分散系中处于沉淀溶解平衡,其溶度积常数表达式
Ksp= ▲ 。
(2)MgCl2溶液显酸性,其水解的离子方程式为 ▲ 。
(3)除去MgCl2酸性溶液中少量的FeCl3,可加入的试剂有 ▲
a.MgO b.Mg(OH)2 c.MgCO3 d.MgSO4
(4)若在空气中加热MgCl2·6H2O,可生成Mg(OH)Cl或MgO,写出相关的化学方程式之一
▲ 。
(5)MgCl2·6H2O在干燥的HCl气流中加热可得到无水氯化镁,其原因是 ▲ 。
(6)电解熔融的MgCl2,阳极的电极反应式为: ▲ ;阴极的电极反应式为 ▲ 。
查看答案和解析>>
科目:高中化学 来源: 题型:
在加入铝粉能放出氢气的溶液中,下列各组离子可能大量共存的是
A. NH4+、NO3-、CO32-、Na+ B. Na+、Ba2+、HCO3-、AlO2-
C. NO3-、K+、AlO2-、OH- D. NO3-、Mg 2+、K+、CH3COO-
查看答案和解析>>
科目:高中化学 来源: 题型:
某种混合气体,可能含有N2、HCl和CO,把混合气体依次通过足量的NaHCO3溶液和灼热的CuO,气体体积都没有变化,经干燥后再通过足量的Na2O2固体,气体体积减少,最后通过灼热的铜网,经充分反应后,气体体积又减少,但还有剩余气体,以下对混合气体区分的判断,正确的是( )
A.一定没有N2,CO和HCl中至少有一种 B.一定没有N2,CO和HCl都有
C.一定有N2,CO和HCl中至少有一种 D.一定有N2和HCl,肯定没有CO
查看答案和解析>>
科目:高中化学 来源: 题型:
下列反应既属于氧化还原反应,又是吸热反应的是( )
A.锌粒与稀硫酸的反应
B.灼热的木炭与CO2反应
C.甲烷在氧气中的燃烧反应
D.Ba(OH)2·8H2O晶体与NH4Cl晶体的反应
查看答案和解析>>
科目:高中化学 来源: 题型:
下列有关反应速率的说法正确的是 ( )
A.用铁片和稀硫酸反应制氢气时,改用98﹪的硫酸可以加快反应速率
B.100ml 2mol·L-1 的盐酸跟锌片反应,加入适量的氯化钠溶液,反应速率不变
C.SO2的催化氧化反应是一个放热的反应,所以升高温度,反应速率变慢
D.汽车尾气中的NO和CO可以缓慢反应生成N2和CO2,减小压强反应速率变慢。
查看答案和解析>>
科目:高中化学 来源: 题型:
某同学在用稀硫酸与锌制取氢气的实验中,发现加入少量硫酸铜溶液可加快氢气的生成速率。请回答下列问题:
⑴.上述实验中发生反应的化学方程式有 、
;
⑵.硫酸铜溶液可以加快氢气生成速率的原因是通过一系列反应构成了Cu/Zn原电池,该原电池的电极反应式,负极: ;正极:
。
⑶.要加快上述实验中气体产生的速率,还可采取的措施有
(答两种)。
⑷.为了进一步研究硫酸铜的量对氢气生成速率的影响,该同学设计了如下一系列实验。将表中所给的混合溶液分别加入到6个盛有过量Zn粒的反应瓶中,收集产生的气体,记录获得相同体积的气体所需时间。
| 实验 混合溶液 | A | B | C | D | E | F |
| 4mol·L-1 H2SO4/mL-1 | 30 | V1 | V2 | V3 | V4 | V5 |
| 饱和CuSO4溶液/mL-1 | 0 | 0.5 | 2.5 | 5 | V6 | 20 |
| H2O/mL-1 | V7 | V8 | V9 | V10 | 10 | 0 |
①.请完成此实验设计,其中:V1= ,V6= ,V9= ;
②.该同学最后得出的结论为:当加入少量CuSO4溶液时,生成氢气的速率会大大提高。但当加入的CuSO4溶液超过一定量时,生成氢气的速率反而会下降。请分析氢气生成速率下降的主要原因
。
查看答案和解析>>
科目:高中化学 来源: 题型:
漆酚( 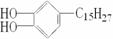 )是我国特产生漆的主要成分,通常情况下为黄色液体,
)是我国特产生漆的主要成分,通常情况下为黄色液体,
能溶于有机溶剂,生漆涂在物体的表面,在空气中干燥后变成黑色的漆膜。将漆酚放入下列物质中:①空气 ②溴水 ③小苏打溶液 ④氯化铁溶液 ⑤通入过量的二氧化碳,不能发生化学反应的是
A.①②⑤ B.③④ C.②⑤ D.③⑤
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com