
冬季是雾霾天气高发的季节,其中汽车尾气和燃煤尾气是造成雾霾的原因之一.
(1)汽车尾气净化的主要原理为:2NO(g)+2CO(g)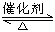 2CO2(g)+N2(g)
2CO2(g)+N2(g)
①一定条件下,在一个容积固定为2L的密闭容器中充入0.8mol NO和1.2mol CO,开始反应至2min时测得CO转化率为20%,则用N2表示的平均反应速率为v(N2)=_________。
②对于气相反应,用某组分(B)的平衡压强(PB)代替物质的量浓度(CB)也可以表示平衡常数(记作KP),则该反应平衡常数的表达式KP=_________。
③该反应在低温下能自发进行,该反应的△H_________0(填“>”、“<”)
④在某一绝热、恒容的密闭容器中充入一定量的NO、CO发生上述反应,测得正反应的速率随时间变化的曲线如图所示(已知:t2-t1=t3-t2)则下列说法不正确的是_________(填编号)
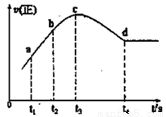
A.反应在c点未达到平衡状态
B.反应速率a点小于b点
C.反应物浓度a点大于b点
D.NO的转化率:t1~t2>t2~t3
(2)使用甲醇汽油可以减少汽车尾气对环境的污染.某化工厂用水煤气为原料合成甲醇,恒温条件下,在体积可变的密闭容器中发生反应CO(g)+2H2(g)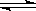 CH3OH(g)到达平衡时,测得CO、H2、CH3OH分别为1mol、1mol、1mol,容器的体积为3L,现往容器中继续通入3mol CO,此时v(正)_________v(逆)(填“>”、“<”或“=”),判断的理由_________。
CH3OH(g)到达平衡时,测得CO、H2、CH3OH分别为1mol、1mol、1mol,容器的体积为3L,现往容器中继续通入3mol CO,此时v(正)_________v(逆)(填“>”、“<”或“=”),判断的理由_________。
(3)二甲醚也是清洁能源.用合成气在催化剂存在下制备二甲醚的反应原理为:2CO(g)+4H2(g)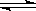 CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比
CH3OCH3(g)+H2O(g),已知一定条件下,该反应中CO的平衡转化率随温度、投料比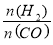 的变化曲线如图:
的变化曲线如图:
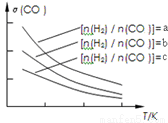
①a、b、c按从大到小的顺序排序为_________。
②某温度下,将某温度下,将2.0molCO(g)和6.0molH2(g)充入容积为2L的密闭容器中,反应到达平衡时,改变压强和温度,平衡体系中CH3OCH3(g)的物质的量分数变化情况如图3所示,关于温度和压强的关系判断正确的是_________
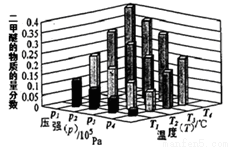
A.P3>P2,T3>T2B.P1>P3,T1>T3
C.P2>P4,T4>T2D.P1>P4,T2>T3
③在恒容密闭容器里按体积比为1:3充入一氧化碳和氢 气,一定条件下反应达到平衡状态.当改变反应的某一个条件后,下列变化能说明平衡一定向逆反应方向移动的是_________
A.正反应速率先增大后减小 B.逆反应速率先增大后减小
C.化学平衡常数K值增大 D.反应物的体积百分含量增大
E.混合气体的密度减小 F.氢气的转化率减小.
科目:高中化学 来源:2015-2016学年安徽黄山屯溪一中高一下期中化学试卷(解析版) 题型:选择题
下列各组物质所含化学键类型完全相同的是
A.HNO3和NH4NO3 B.NaOH和KCl C.NaN3和CaO2 D.AlCl3和MgCl2
查看答案和解析>>
科目:高中化学 来源:2016届西藏日喀则一中高三下学期二模考试理综化学试卷(解析版) 题型:选择题
NA为阿伏加德罗常数的值.下列说法正确的是( )
A.1 mol-OH(羟基)与l mol NH4+中所含电子数均为10NA
B.25℃时,100 mL pH=l的稀硫酸中,含有的H+数目为0.01 NA
C.室温下,1 L pH=13的NaOH溶液中,由水电离的OH-离子数目为0.1 NA
D.标准状况下,2.24LNO2和N2O4混合气体中含0.2 NA个氧原子
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:实验题
硫化锌(ZnS)是一种重要的化工原料,难溶于水,可由炼锌的废渣锌灰制取,其工艺流程如图:
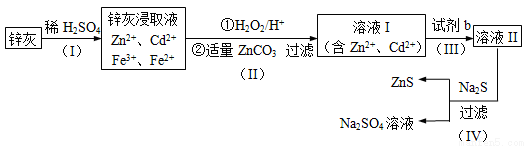
(1)为提高锌灰的浸取效率,不采用的方法是______________(填序号)
①研磨 ②搅拌 ③多次浸取 ④升高温度 ⑤加压
(2)步骤Ⅱ所得滤渣中的物质是______________(写化学式)。
(3)步骤Ⅲ中可得Cd单质,为避免引入新的杂质,试剂b应为______________。
(4)步骤Ⅳ还可以回收Na2SO4来制取Na2S。
①检验ZnS固体是否洗涤干净的方法是______________;
②Na2S可由等物质的量的Na2SO4和CH4在高温、催化剂条件下制取.化学反应方程式为______________。
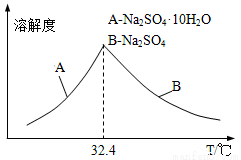
③已知Na2SO4•10H2O及Na2SO4的溶解度随温度变化曲线如图。从滤液中得到Na2SO4•10H2O的操作方法是______________。
(5)若步骤Ⅱ加入的ZnCO3为b mol,步骤Ⅲ所得Cd为d mol,最后得到VL、物质的量浓度为c mol/L的Na2SO4溶液.则理论上所用锌灰中含有锌元素的质量为______________g。
查看答案和解析>>
科目:高中化学 来源:2016届宁夏六盘山高中高三第四次模拟理综化学试卷(解析版) 题型:选择题
下列事实不能用元素周期律解释的是
A.向Na2SO3溶液中加盐酸,有气泡产生
B.0.1 mol•L-1溶液的pH:NaOH>LiOH
C.Mg、Al与同浓度盐酸反应,Mg更剧烈
D.气态氢化物的稳定性:HBr>HI
查看答案和解析>>
科目:高中化学 来源:2016届内蒙古赤峰二中高三第四次模拟理综化学试卷(解析版) 题型:选择题
已知A、B为单质,C为化合物,能实现下述转化关系的是( )
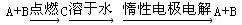
①若C溶于水后得到强碱溶液,则A可能是Na
②若C溶液遇Na2SO3,放出SO2气体,则A可能是H2
③若C溶液中滴加KSCN溶液显红色,则B可能为Fe.
④若C溶液中滴加NaOH溶液有蓝色沉淀生成,则B可能为Cu
A.①② B.①③ C.②④ D.③④
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:填空题
W、X、Y、Z是原子序数依次增大的同一短周期主族元素,W、X是金属元素,Y、Z是非金属元素。W、X两者的最高价氧化物对应的水化物可以起反应生成盐和水。
(1)W的名称是______________,上述反应的离子方程式为______________。
(2)W与Y可形成化合物W2Y,Y的离子结构示意图为______________,该化合物的电子式为______________。
(3)X与Z可形成化合物是共价化合物而不是离子化合物,设计一个实验证明之:______________。
(4)Y的低价氧化物和Z的单质在水溶液中反应的化学方程式是:______________。
(5)Y与Z能形成一种化合物,其所有原子都满足8电子结构,其分子式为______________。
查看答案和解析>>
科目:高中化学 来源:2015-2016学年四川省高一下期中化学试卷(解析版) 题型:选择题
下列有关物质性质的比较顺序中,不正确的是( )
A.微粒半径:Na+>Al3+>S2->Cl-
B.沸点:F2<Cl2<Br2<I2
C.碱性:LiOH<NaOH<KOH<RbOH
D.熔点:Li>Na>K>Rb
查看答案和解析>>
科目:高中化学 来源:2015-2016学年河北省高二下期中化学试卷(解析版) 题型:选择题
原子轨道的杂化不但出现在分子中,原子团中同样存在杂化轨道的。在 SO42-中S原子的杂化方式为( )
A.sp B.sp2 C.s p3 D.无判法断
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com