
【题目】室温下,用0.1mol·L-1的NaOH溶液分别滴定20mL、浓度均为0.1mol·L-1的HCl溶液和HCOOH溶液,溶液中由水电离出的氢离子浓度的对数[1gc(H+)水]随加入NaOH溶液体积的变化如图所示(忽略溶液体积变化),下列说法正确的是( )
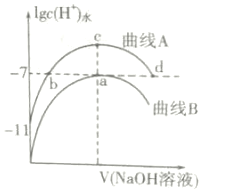
A.该温度下HCOOH的电离常数为Ka=1×10-5
B.a、c两点对应溶液同时升高相同温度,![]() 增大
增大
C.在c点溶液中有:c(HCOO-)+c(HCOOH)=0.1mol·L-1
D.在a、b、c、d四点中对应的溶液呈中性的为a、b、d
【答案】AB
【解析】
A. 未加NaOH时,HCOOH的1gc(H+)水 =11,c(H+)水 =1011 molL1,c(OH-)=c(OH-)水=c(H+)水 =1011 molL1,c(H+) =103 molL1,该温度下HCOOH的电离常数为![]() ,故A正确;
,故A正确;
B. a、c两点对应溶液同时升高相同温度,c(Cl-)基本不变,HCOO-水解程度增大,c(HCOO-)减小,因此![]() 增大,故B正确;
增大,故B正确;
C. 在c点,加入NaOH溶液的体积为20mL,溶液总体积约为40mL,因此溶液中有:c(HCOO-) + c(HCOOH) = 0.05mol·L1,故C错误;
D. 在a溶质为NaCl,呈中性,b溶质为HCOOH和HCOONa的混合溶液,电离程度等于水解程度,溶液呈中性,c溶液为HCOONa,HCOO-水解呈碱性,d点溶质为HCOONa和NaOH,溶液呈碱性,因此呈中性的为a、b,故D错误。
综上所述,答案为AB。


科目:高中化学 来源: 题型:
【题目】根据下列信息合成含五元环有机化合物N的路线如图:
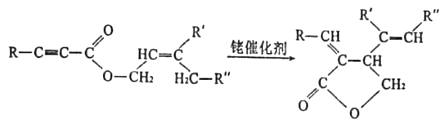
(R、R’、R”表示氢、烷基或芳基)
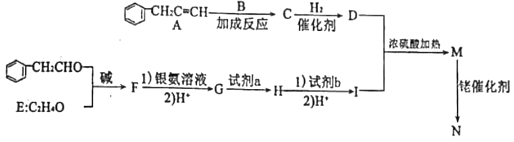
已知: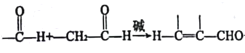 +H2O,B是E同系物,最大质荷比是30
+H2O,B是E同系物,最大质荷比是30
请回答下列问题:
(1)有机物A的系统命名___;
(2)C、D均为不饱和醇,D中含有官能团名称是___;
(3)设计实验,写出检验F中所含官能团的方法___;
(4)试剂a是___,H→I加入试剂b的反应方程式为___;
(5)写出满足下列条件G的所有(包含G)同分异构体有___种
①与G含有相同的官能团②苯环上最多有两个取代基
(6)写出N的结构简式___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】300℃下,在一容积为2 L的恒容密闭容器中加入0.2 mol CO和0.4 mol H2,发生如下反应:CO(g)+2H2(g) ![]() CH3OH(g) 。下列各物理量随反应时间变化趋势的曲线不正确的是
CH3OH(g) 。下列各物理量随反应时间变化趋势的曲线不正确的是
A. 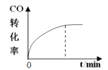 B.
B. 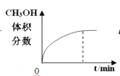
C.  D.
D. 
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】“花卉保鲜剂”是一种可以延长花期的试剂。如表是500mL“鲜花保鲜剂”中含有的成分,阅读后回答下列问题:
成分 | 质量(g) | 摩尔质量(gmol1) |
蔗糖 | 25.00 | 342 |
硫酸钾 | 0.87 | 174 |
阿司匹林 | 0.17 | 180 |
高锰酸钾 | 0.316 | 158 |
硝酸银 | 0.0075 | 170 |
(1)下列“花卉保鲜剂”的成分中,属于非电解质的是______,可做杀菌剂的是____
A. 高锰酸钾B. 硫酸钾C. 蔗糖D. 硝酸银E. 水
(2) 配制1L上述“鲜花保鲜剂”需要高锰酸钾______mol。
(3)在溶液配制过程中,下列操作会使配制结果无影响的是______。
A.定容时俯视容量瓶刻度线
B.容量瓶在使用前未干燥,里面有少量蒸馏水
C.容量瓶在使用前刚配制完一定物质的量浓度的氯化钠溶液未洗涤
D.定容摇匀后发现液面低于容量瓶的刻度线,但未做任何处理
(4)“鲜花保鲜剂”中K+(阿司匹林中不含K+)的物质的量浓度为______mol/L。
(5)如果用高铁酸钾(K2FeO4)代替高锰酸钾效果会更好,湿法制备高铁酸钾的反应体系中有六种微粒:Fe(OH)3、ClO-、OH-、FeO42-、Cl-、H2O.碱性条件下,氧化剂与还原剂的物质的量的比为3:2发生反应,写出并配平湿法制备高铁酸钾的离子反应方程式___________________________________________________________
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】常温下,Ksp(BaSO4)=1×10-10,Ksp(BaCO3)=1×10-9。向20mL0.1mol·L-1BaCl2溶液中滴入0.1mol·L-1的Na2SO4溶液,溶液中pBa2+[pBa2+=-lgc(Ba2+)]与Na2SO4溶液体积的关系如图所示。下列叙述错误的是( )

A.图像中,n=1,m=5
B.若起始时c(BaCl2)=0.2mol·L-1,m不变,b点向d点移动
C.若用同浓度的Na2CO3溶液替代Na2SO4溶液,可使b点向c点移动
D.V。时,向溶液中滴加Na2CO3溶液,产生BaCO3沉淀的条件是![]() >10
>10
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】A、B、C三个烧杯中分别盛有相同物质的量浓度的稀硫酸。
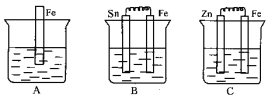
(1)A中反应的离子方程式为_________________________________。
(2)B中Fe极为_______极,电极反应式为_______________________。C中Fe极为_______极,电极反应式为__________________________,电子从_______极流出(填“Zn”或“Fe”)。
(3)比较A、B、C中铁被腐蚀的速率,由快到慢的顺序是___________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】有机物M是一种重要的医药活性中间体,其合成路线如图:
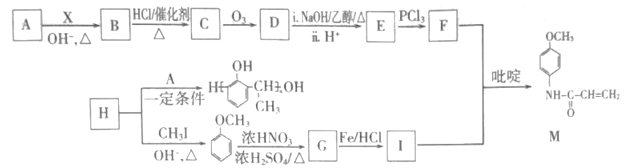
已知:ⅰ.2CH3CHO![]() CH3CH=CHCHO
CH3CH=CHCHO
ⅱ.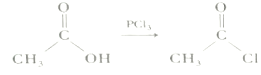
ⅲ.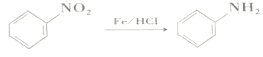 (在空气中极易被氧气氧化)
(在空气中极易被氧气氧化)
请回答以下问题:
(1)B中官能团名称为___,检验其官能团所需试剂先后顺序为___(填字母)。
a.银氨溶液 b.NaOH溶液 c.稀硫酸 d.稀盐酸 e.酸性高锰酸钾溶液
(2)F与I的反应类型是___,吡啶是一种有机碱,其作用为___。
(3)写出![]() 与A反应的化学方程式___。
与A反应的化学方程式___。
(4)N是G的同分异构体,写出满足下列条件N的两种结构简式___。
①苯环上的一氯代物有两种②含有两种官能团③能发生银镜反应
(5)写出以![]() 为原料制备
为原料制备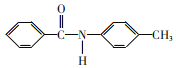 的合成路线(其它无机试剂任选)___。
的合成路线(其它无机试剂任选)___。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列反应不属于四种基本反应类型,但属于氧化还原反应的是
A.Zn+CuSO4=ZnSO4+CuB.3CO+Fe2O3![]() 2Fe+3CO2
2Fe+3CO2
C.AgNO3+KCl=AgCl↓+KNO3D.2KMnO4![]() K2MnO4+MnO2+O2↑
K2MnO4+MnO2+O2↑
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下列判断正确的是( )
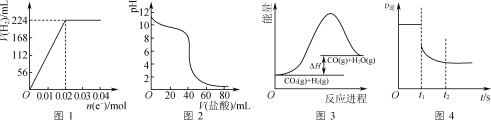
A.图1可表示电解200 mL 0.1 mol·L-1 NaCl溶液过程中,产生氢气体积(标准状况)与转移电子物质的量的关系曲线
B.图2可表示常温下0.1 mol·L-1盐酸滴加到40 mL 0.1 mol·L-1 NaOH溶液的滴定曲线
C.高温下能自发进行的反应CO2(g)+H2(g)![]() CO(g)+H2O(g)的能量变化如图3所示,则该反应的ΔS>0
CO(g)+H2O(g)的能量变化如图3所示,则该反应的ΔS>0
D.图4可表示反应N2(g)+3H2(g)![]() 2NH3(g)在t1时刻扩大容器体积时,v逆随时间的变化曲线
2NH3(g)在t1时刻扩大容器体积时,v逆随时间的变化曲线
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com