
【题目】高炉炼铁过程中发生的主要反应为:1/3Fe2O3(s)+CO(g)![]() 2/3Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
2/3Fe(s)+CO2(g),已知该反应在不同温度下的平衡常数如下:
温度/℃ | 1000 | 1150 | 1300 |
平衡常数 | 4.0 | 3.7 | 3.5 |
(1)该反应的平衡常数表达式K=_____________,ΔH________0(填“>”、“<”或“=”);
(2)在一个容积为5L的密闭容器中,1000℃时加入Fe、Fe2O3、CO、CO2各1.0mol,此时比较v(正)___v(逆) (填“>” “=” “<”),反应经过2min后达到平衡。求该时间范围内反应的平均反应速率v(CO2)=____,CO的平衡转化率=____________;
(3)欲提高(2)中CO的平衡转化率,可采取的措施是________。
A、减少Fe的量 B、增加Fe2O3的量 C、移出部分CO2 D、提高反应温度 E、减小容器的容积 F、加入合适的催化剂
【答案】(1)、c(CO2)/ c(CO) ,< (2)、 > , 0.06mol.L-1.min-1 ,60%;(3)、C
【解析】
试题(1)平衡常数是指在一定条件下的可逆反应中,当达到平衡状态时,生成物浓度的幂之积和反应物难得的幂之积的比值,所以其表达式为K=c(CO2)/ c(CO)。根据有关数据可知,温度越高平衡常数越小,所以升高温度,平衡向逆反应方向移动,即正反应是放热反应。
(2)设平衡时CO的物质的量浓度是x,则消耗CO的浓度是0.2-x,生成CO2也是0.2-x,平衡是CO2就是0.2-x+0.2=0.4-x。根据平衡常数知 (0.4-x)/x=4,解得x=0.08mol/L,所以消耗CO是0.2mol/L-0.08mol/L=0.12mol/L,则其转化率是0.06÷0.1×100%=60%。CO2的反应速率是0.12mol/L÷2min=0.06mol/(L·min)。
(3)固体质量的变化,不影响平衡状态,AB不正确。C是解得生成物浓度,平衡向正反应方向移动,转化率增大。正反应放热,升高温度平衡向逆反应方向移动,转化率降低。反应前后体积不变,改变压强,平衡不移动。同样催化剂也不能影响平衡状态,所以正确的答案是C。


科目:高中化学 来源: 题型:
【题目】现有下列四个图像:

下列反应中全部符合上述图像的反应是 ( )
A. N2(g)+3H2(g)![]() 2NH3(g) ΔH1<0
2NH3(g) ΔH1<0
B. 2SO3(g)![]() 2SO2(g)+O2(g) ΔH2>0
2SO2(g)+O2(g) ΔH2>0
C. 4NH3(g)+5O2(g)![]() 4NO(g)+6H2O(g) ΔH3<0
4NO(g)+6H2O(g) ΔH3<0
D. H2(g)+ CO(g)![]() C(s)+H2O(g) ΔH4>0
C(s)+H2O(g) ΔH4>0
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】T ℃时,在容积为1 L的密闭容器中发生某一反应,且测得不同时间容器中四种物质A、B、C、D的物质的量变化如图所示。已知:物质A、B、C、D均为气态。根据要求回答下列问题:
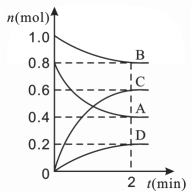
(1)容器中反应的化学方程式为__________________________________________。
(2)前2 min,v(A)=______mol·(L·min)-1。
(3)能说明该反应已达到平衡状态的是_____________________
A.混合气体的压强不变
B.混合体系中A、B、C、D四种物质同时存在
C.消耗0.1mol的B同时生成0.1mol的D
D.B的物质的量不变
(4)T ℃时,该反应的平衡常数K=___(保留小数点后两位)。
(5)下列措施能增大该反应的反应速率的是_______________________________(填选项字母)。
A.容器容积不变,加入与反应无关的氖气
B.升高反应体系的温度
C.容器压强不变,加入与反应无关的氖气
D.把容器的体积缩小一倍
(6)T ℃时,容积为1 L的密闭容器中,起始时充入0.2 mol A、0.4 mol B、0.3 mol C、0.5 mol D,此时v(正)_______v(逆)(填“>”“<”或“=”)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】下图是部分短周期元素的原子序数与其某种常见化合价的关系图,若用原子序数代表所对应的元素,则下列说法正确的是

A. 31d和33d属于同种核素
B. 气态氢化物的稳定性:a>d>e
C. b、c的最高价氧化物对应水化物可以反应
D. a和b形成的化合物不可能含共价键
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】在一体积为1L的密闭容器中,通入一定量的CO和H2O,在T1℃时发生如下反应:CO (g)+H2O(g) ![]() CO2(g)+H2(g) △H<0,CO和H2O浓度变化如图,则
CO2(g)+H2(g) △H<0,CO和H2O浓度变化如图,则
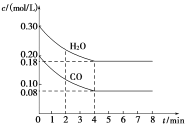
(1) 0~4 min CO的平均反应速率v(CO)=___________mol/(L.min)。
(2)达平衡时CO的转化率为____________,T1℃时该反应的平衡常数K=_______________。
(3)T2℃(高于T1℃)时,在相同容器中发生上述反应,容器内各物质的浓度变化如下表:
时间(min) | CO | H2O | CO2 | H2 |
0 | 0.200 | 0.300 | 0 | 0 |
2 | 0.138 | 0.238 | 0.062 | 0.062 |
3 | C1 | C2 | C3 | C3 |
4 | C1 | C2 | C3 | C3 |
5 | 0.116 | 0.216 | 0.084 | C4 |
①表中3~4 min时,反应v正__________v逆(填“>”、“<”或“=”); C1___________0.08mol/L(填“>”、“<”或“=”)。
②4~5 min时,平衡向逆反应方向移动,可能的原因是__________(填字母)。
a.增加水蒸气 b.降低温度 .增大了CO2浓度 d.增加了氢气浓度
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】设阿伏加德罗常数为NA,则下列说法正确的是
A.15g甲基(-CH3)所含有的电子数是9NA
B.7.8g ![]() 中含有的碳碳双键数为0.3NA
中含有的碳碳双键数为0.3NA
C.1mol C2H5OH和1mol CH3CO18OH反应生成水的中子数为8NA
D.标准状况下,11.2L己烷所含分子数为0.5NA
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】镍与第VA族元素形成的化合物是重要的半导体材料,其中应用最广泛的是砷化镓(GaAs)。回答下列问题:
(1)基态N原子的核外电子排布式为___________,基态Ga原子核外有___________个未成对电子。
(2)镓失去电子的逐级电离能(单位:kJ·mol-1)的数值依次为577、1985、2962、6192,由此可推知镓的主要化合价为___________和+3。砷的电负性比镓___________(填“大”或“小”)。
(3)二水合草酸镓的结构如图所示,其中镓原子的配位数为___________。
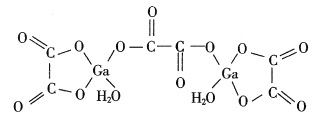
(4)砷化镓可由(CH3)3Ga和AsH3在700℃时制得。(CH3)3Ga中镓原子的杂化方式为___________。
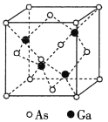
(5)GaAs为原子晶体,密度为ρg·cm-3,其晶胞结构如图所示。Ga与As以___________键键合。Ga和As的原子半径分别为apm和bpm,设阿伏加德罗常数的值为NA,则GaAs晶胞中原子的体积占晶胞体积的百分率为___________(列出计算式,可不化简)。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】为了探究NO2与过氧化钠反应的情况,甲、乙两位同学设计了如下实验,其装置如图。
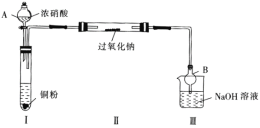
已知:2NO2+2NaOH==NaNO3+NaNO2+H2O
试回答下列问题:
(1)仪器A的名称是________________,仪器B的作用是________________________。
(2)装入药品前必须检查装置的气密性,具体操作方法是________________________。
(3)试管中生成NO2反应的离子方程式是________________________________________。
(4)实验过程中,两位同学通过检验得知气体产物中含有较多氧气。该同学通过查阅资料了解NO2具有氧化性,据此甲同学判断NO2与过氧化钠反应可得到氧气,而乙同学认为该结论不合理,理由是__________。为验证自己的想法,乙同学对上述装置进行了改进,具体做法是________________。
(5)改进装置后,再进行实验,两位同学发现过氧化钠的颜色由淡黄色逐渐变成白色,且检验不出氧气的生成,该反应的化学方程式为________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
【题目】如图:A处通入氯气。关闭B阀时,C处干燥红色布条无变化;打开B阀时,C处干燥红色布条褪色。则D中盛放的试剂不可能的是
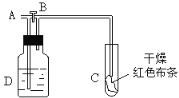
A.饱和食盐水B.浓硫酸
C.溴化钠溶液D.氢氧化钙溶液
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com