
”¾ĢāÄæ”æ(1)ČēĶ¼ŹĒŅ»øö»Æѧ¹ż³ĢµÄŹ¾ŅāĶ¼”£
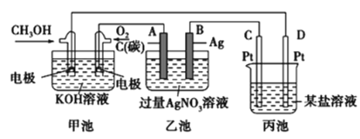
¢ŁŅŅ³ŲÖŠ×Ü·“Ó¦µÄĄė×Ó·½³ĢŹ½____________”£
¢Śµē½āŅ»¶ĪŹ±¼äŗó£¬ĻņŅŅ³ŲµÄČÜŅŗÖŠ¼ÓČė________________æÉ»Öø“ĪŖŌČÜŅŗ”£
¢Ūµ±ŅŅ³ŲÖŠB(Ag)¼«µÄÖŹĮæŌö¼Ó5.40g£¬“ĖŹ±±ū³Ųijµē¼«Īö³ö1.60gij½šŹō£¬Ōņ±ūÖŠµÄijŃĪČÜŅŗæÉÄÜŹĒ________”£
A.MgSO4 B.CuSO4 C.NaCl D.AgNO3
(2)ĄūÓĆ·“Ó¦Cu£«2FeCl3=CuCl2£«2FeCl2Éč¼Ę³ÉČēĶ¼ĖłŹ¾Ōµē³Ų£¬»Ų“šĻĀĮŠĪŹĢā£ŗ

¢ŁŠ“³öøŗ¼«µÄµē¼«·“Ó¦Ź½£ŗ___________”£
¢ŚĶ¼ÖŠXČÜŅŗŹĒ________”£
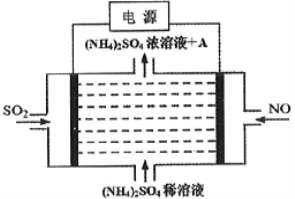
¢ŪĄūÓĆĶ¼ÖŠÉč¼ĘµÄŌµē³ŲĪŖµēŌ“æɽ«Īķö²ÖŠµÄNO”¢SO2µē½ā·Ö±š×Ŗ»ÆĪŖNH4+ŗĶSO42-£¬ČēĶ¼ĖłŹ¾£¬ŌņĪļÖŹAµÄ»ÆѧŹ½ĪŖ_____________£¬Ņõ¼«µÄµē¼«·“Ó¦Ź½ĪŖ______________”£
”¾“š°ø”æ4Ag++2H2O![]() 4Ag+O2”ü+4H+ Ag2O BD Cu-2e-=Cu2£« FeCl3ČÜŅŗ H2SO4 NO+5e-+6H+=NH4++H2O
4Ag+O2”ü+4H+ Ag2O BD Cu-2e-=Cu2£« FeCl3ČÜŅŗ H2SO4 NO+5e-+6H+=NH4++H2O
”¾½āĪö”æ
(1)¼×³ŲĪŖ¼×“¼Č¼ĮĻµē³Ų£¬ĶØČė¼×“¼µÄŅ»¼«ĪŖøŗ¼«£¬ĶØČėŃõĘųµÄĪŖÕż¼«£»ŅŅ³ŲĪŖµē½ā³Ų£¬AÓėČ¼ĮĻµē³ŲµÄÕż¼«ĻąĮ¬£¬ĪŖŃō¼«£¬BĪŖŅõ¼«£»±ūĪŖµē½ā³Ų£¬DÓėČ¼ĮĻµē³ŲµÄøŗ¼«ĻąĮ¬£¬ĪŖŅõ¼«£¬CĪŖŃō¼«£»
(2)ĄūÓĆ·“Ó¦Cu£«2FeCl3=CuCl2£«2FeCl2Éč¼Ę³ÉŌµē³Ų£¬CuŌŖĖŲ»ÆŗĻ¼ŪÉżøߣ¬ĪŖøŗ¼«£¬FeŌŖĖŲ»ÆŗĻ¼Ū½µµĶ£¬FeCl3ŌŚÕż¼«·“Ó¦£¬XČÜŅŗĪŖFeCl3ČÜŅŗ”£
(1)¢ŁŅŅ³ŲĪŖµē½ā³Ų£¬AĪŖŃō¼«£¬Ė®Ź§µē×ÓÉś³ÉO2ŗĶH+£¬BĪŖŅõ¼«£¬Ag+µĆµē×ÓÉś³ÉAg£¬×Ü·“Ó¦ĪŖ£ŗ4Ag++2H2O![]() 4Ag+O2”ü+4H+£¬¹Ź“š°øĪŖ£ŗ4Ag++2H2O
4Ag+O2”ü+4H+£¬¹Ź“š°øĪŖ£ŗ4Ag++2H2O![]() 4Ag+O2”ü+4H+£»
4Ag+O2”ü+4H+£»
¢Ś“Ó×Ü·“Ó¦Ą“æ“£¬µē½ā¹ż³ĢAgŌ×ÓŗĶOŌ×Ó°“2:1ŅŌAgŗĶO2µÄŠĪŹ½Īö³öĮĖ£¬ĖłŅŌ£¬¼ÓŅ»¶ØĮæµÄAg2OÄÜ»Öø“ĪŖŌČÜŅŗ£¬¹Ź“š°øĪŖ£ŗAg2O£»
¢ŪŅŅ³ŲÖŠB(Ag)¼«µÄµē¼«·“Ó¦Ź½ĪŖ£ŗAg++e-=Ag£¬µ±Ag¼«Ōö¼Ó5.4g£¬¼“n(Ag)=![]() =0.05molŹ±£¬ÓÉAg++e-=AgæÉÖŖ£¬ĶعżµēĀ·ÖŠµÄµē×ÓµÄĪļÖŹµÄĮæn(e-)=0.05mol”£±ū³ŲĪŖµē½ā³Ų£¬Ņõ¼«±ķĆęĪö³ö½šŹō£¬øĆ½šŹōµÄŃōĄė×ӵķŵēĖ³ŠņŅŖŌŚĖ®µēĄėµÄH+Ē°Ćę£¬·ńŌņ²»»įĪö³ö½šŹō”£ŅŖÉś³É1.6g¹ĢĢ壬ŌņÉś³É1.6g¹ĢĢå×ŖŅʵĵē×ÓµÄĪļÖŹµÄĮæ±ŲŠėŠ”ÓŚµČÓŚ0.05mol£ØÉś³É1.6g¹ĢĢåŗó£¬Čō½šŹōĄė×ÓŅŃ·“Ó¦Ķź£¬H2OµēĄėµÄH+¼ĢŠųµĆµē×Ó¼“æÉ£©”£
=0.05molŹ±£¬ÓÉAg++e-=AgæÉÖŖ£¬ĶعżµēĀ·ÖŠµÄµē×ÓµÄĪļÖŹµÄĮæn(e-)=0.05mol”£±ū³ŲĪŖµē½ā³Ų£¬Ņõ¼«±ķĆęĪö³ö½šŹō£¬øĆ½šŹōµÄŃōĄė×ӵķŵēĖ³ŠņŅŖŌŚĖ®µēĄėµÄH+Ē°Ćę£¬·ńŌņ²»»įĪö³ö½šŹō”£ŅŖÉś³É1.6g¹ĢĢ壬ŌņÉś³É1.6g¹ĢĢå×ŖŅʵĵē×ÓµÄĪļÖŹµÄĮæ±ŲŠėŠ”ÓŚµČÓŚ0.05mol£ØÉś³É1.6g¹ĢĢåŗó£¬Čō½šŹōĄė×ÓŅŃ·“Ó¦Ķź£¬H2OµēĄėµÄH+¼ĢŠųµĆµē×Ó¼“æÉ£©”£
A£®Mg2+µÄ·ÅµēĖ³ŠņŌŚH+Ö®ŗ󣬲»»įĪö³ö½šŹōMg£¬A“ķĪó£»
B£®Cu2+µÄ·ÅµēĖ³ŠņŌŚH+Ö®Ē°£¬Cu2++2e-=Cu£¬ŌņĪö³öCuµÄÖŹĮæ=1.6g£¬ŌņĶعżµēĀ·µÄµē×ÓµÄĪļÖŹµÄĮæn(e-)=0.05mol£¬·ūŗĻĢāŅā£¬BÕżČ·£»
C£®Na+µÄ·ÅµēĖ³ŠņŌŚH+Ö®ŗ󣬲»»įĪö³ö½šŹōNa£¬C“ķĪó£»
D£®Ag+µÄ·ÅµēĖ³ŠņŌŚH+Ö®Ē°£¬Ag++e-=Ag£¬Īö³ö1.6g¹ĢĢå(Ag)Ź±£¬¼“n(Ag)=![]() =
=![]() £¬ŌņĶعżµēĀ·µÄµē×ÓµÄĪļÖŹµÄĮæn(e-)=n(Ag)=
£¬ŌņĶعżµēĀ·µÄµē×ÓµÄĪļÖŹµÄĮæn(e-)=n(Ag)=![]() ”Ö0.0148mol£¼0.05mol£¬·ūŗĻĢāŅā£¬DÕżČ·£»
”Ö0.0148mol£¼0.05mol£¬·ūŗĻĢāŅā£¬DÕżČ·£»
¹Ź“š°øĪŖ£ŗBD£»
(2)¢ŁCuŹ§µē×Ó£¬»ÆŗĻ¼ŪÉżøߣ¬×÷øŗ¼«£¬µē¼«·“Ó¦Ź½ĪŖ£ŗCu-2e-=Cu2£«£¬¹Ź“š°øĪŖ£ŗCu-2e-=Cu2£«£»
¢ŚCu×÷øŗ¼«£¬ŌņC×÷Õż¼«£¬FeCl3ŌŚÕż¼«µĆµē×ÓÉś³ÉFeCl2£¬ŌņXČÜŅŗĪŖFeCl3ČÜŅŗ£¬¹Ź“š°øĪŖ£ŗFeCl3ČÜŅŗ£»
¢ŪNOµĆµē×Ó£¬×Ŗ»ÆĪŖNH4+£¬Ōņµē½ā³ŲÓŅ±ßµē¼«ĪŖŅõ¼«£¬µē¼«·“Ó¦Ź½ĪŖ£ŗNO+5e-+6H+=NH4++H2O£¬SO2Ź§µē×Ó£¬×Ŗ»ÆĪŖSO42-£¬×ó±ßµē¼«ĪŖŃō¼«£¬µē¼«·“Ó¦Ź½ĪŖ£ŗSO2-2e-+2H2O=SO42-+4H+£¬×Ü·“Ó¦ĪŖ£ŗ![]() £¬ĖłŅŌ£¬ĪļÖŹAĪŖH2SO4£¬¹Ź“š°øĪŖ£ŗH2SO4£»NO+5e-+6H+=NH4++H2
£¬ĖłŅŌ£¬ĪļÖŹAĪŖH2SO4£¬¹Ź“š°øĪŖ£ŗH2SO4£»NO+5e-+6H+=NH4++H2


 ŌĶĮæģ³µĻµĮŠ“š°ø
ŌĶĮæģ³µĻµĮŠ“š°ø
| Äź¼¶ | øßÖŠæĪ³Ģ | Äź¼¶ | ³õÖŠæĪ³Ģ |
| øßŅ» | øßŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” | ³õŅ» | ³õŅ»Ćā·ŃæĪ³ĢĶĘ¼ö£” |
| ø߶ž | ø߶žĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õ¶ž | ³õ¶žĆā·ŃæĪ³ĢĶĘ¼ö£” |
| øßČż | øßČżĆā·ŃæĪ³ĢĶĘ¼ö£” | ³õČż | ³õČżĆā·ŃæĪ³ĢĶĘ¼ö£” |
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĢ½¾æĪļÖŹµÄ½į¹¹ÓŠÖśÓŚ¶ŌĪļÖŹµÄŠŌÖŹ½ųŠŠŃŠ¾æ”£
£Ø1£©¢Ł ĻĀĮŠĪļÖŹÖŠŗ¬ÓŠōČ»łµÄŹĒ__________________(Ģī×ÖÄø)”£
a£®![]() b£®
b£®![]() c£®
c£®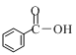
¢Ś ĻĀĮŠĪļÖŹ·Ö×ÓÖŠĖłÓŠŌ×Ó“¦ÓŚĶ¬Ņ»Ę½ĆęµÄŹĒ__________________(Ģī×ÖÄø)”£
a£®±½ b£®±ūĻ© c£®¼×“¼
£Ø2£©ŅŅĻ©Ź¹äåĖ®»ņäåµÄĖÄĀČ»ÆĢ¼ČÜŅŗĶŹÉ«µÄ»Æѧ·½³ĢŹ½_____________________£¬ŹōÓŚ________·“Ó¦£¬
£Ø3£©×ĘČȵÄĶĖæ¶ą“Ī·“ø“µŲ²åČėŅŅ“¼ÖŠµÄĻÖĻóŹĒ£ŗ___________________________£¬ŹōÓŚ_______·“Ó¦”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”擼ĖįŹ÷Ö¬ŹĒŅ»ÖÖ³ÉĤŠŌŗƵď÷Ö¬£¬ĻĀĆęŹĒŅ»ÖÖ“¼ĖįŹ÷Ö¬µÄŗĻ³ÉĻßĀ·£ŗ
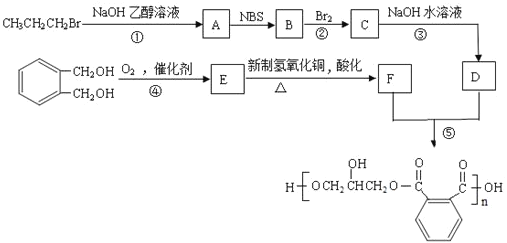
ŅŃÖŖ£ŗRCH2CH=CH2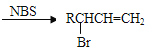
£Ø1£©Š“³öBµÄ½į¹¹¼ņŹ½ŹĒ___”£
£Ø2£©·“Ó¦¢Ł”«¢ŻÖŠŹōÓŚČ”“ś·“Ó¦µÄŹĒ___(ĢīŠņŗÅ)”£
£Ø3£©Š“³öÓÉC”śDµÄ»Æѧ·½³ĢŹ½___”£
£Ø4£©Š“³öÓÉEÓėŠĀÖĘĒāŃõ»ÆĶ·“Ó¦µÄ»Æѧ·½³ĢŹ½___£¬ĻÖĻó___”£
£Ø5£©ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ___(Ģī×ÖÄø)”£
a£®1molEÓė×ćĮæµÄŅų°±ČÜŅŗ·“Ó¦ÄÜÉś³É2molAg
b£®1molFÄÜÓė×ćĮæµÄNaHCO3·“Ó¦²śÉś1molCO2
c£®¶”Ķ锢1©±ū“¼ŗĶDÖŠ·Šµć×īøßµÄĪŖD
£Ø6£©Š“³ö·ūŗĻĻĀĮŠĢõ¼žµÄÓė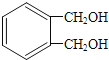 »„ĪŖĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½___”£
»„ĪŖĶ¬·ÖŅģ¹¹ĢåµÄ½į¹¹¼ņŹ½___”£
a£®ÄÜÓėÅØäåĖ®·“Ӧɜ³É°×É«³Įµķ
b£®±½»·ÉĻŅ»ĀČ“śĪļÓŠĮ½ÖÖ
c£®ÄÜ·¢ÉśĻūČ„·“Ó¦
£Ø7£©·“Ó¦¢ŻµÄ»Æѧ·½³ĢŹ½ŹĒ___”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æijŠ”×éĪŖŃŠ¾æµē»ÆѧŌĄķ£¬Éč¼ĘČēĶ¼×°ÖĆ”£ĻĀĮŠŠšŹö²»ÕżČ·µÄŹĒ
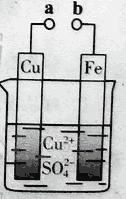
A. aŗĶb²»Į¬½ÓŹ±£¬ĢśĘ¬ÉĻ»įÓŠ½šŹōĶĪö³ö
B. aŗĶbÓƵ¼ĻßĮ¬½ÓŹ±£¬ĶʬÉĻ·¢ÉśµÄ·“Ó¦ĪŖ£ŗCu2£«+2e-= Cu
C. ĪŽĀŪaŗĶbŹĒ·ńĮ¬½Ó£¬ĢśĘ¬¾ł»įČܽā£¬ČÜŅŗ“ÓĄ¶É«Öš½„±ä³ÉĒ³ĀĢÉ«
D. aŗĶb·Ö±šĮ¬½ÓÖ±Į÷µēŌ“Õż”¢øŗ¼«£¬µēŃ¹×ć¹»“óŹ±£¬Cu2£«ĻņĶµē¼«ŅʶÆ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ¶ĢÖÜĘŚÖ÷×åŌŖĖŲ A”¢B”¢C”¢D”¢E µÄŌ×ÓŠņŹżŅĄ“ĪŌö“󔣳£ĪĀĻĀ£¬A”¢C ×é³ÉµÄ»ÆŗĻĪļŹĒ³£¼ūŅŗĢ壬B Ō×Ó×īĶā²ćµē×ÓŹżµČÓŚ“ĪĶā²ćµē×ÓŹżµÄ 2 ±¶£¬D Óė C Ķ¬Ö÷×唣»Ų“šĻĀĮŠĪŹĢā£ŗ
£Ø1£© A µÄµ„ÖŹµÄµē×ÓŹ½ĪŖ ______ £»B ŌŚŌŖĖŲÖÜĘŚ±ķÖŠµÄĪ»ÖĆĪŖµŚ____ÖÜĘŚµŚ_____ ×唣
£Ø2£© B”¢C ÖŠ£¬Ō×Ó°ė¾¶“óµÄŹĒ______£ØĢīŌŖĖŲ·ūŗÅ£©£»D”¢E µÄ¼ņµ„Ēā»ÆĪļÖŠ£¬ĪČ¶ØŠŌ½ĻĒæµÄŹĒ______£ØĢī»ÆѧŹ½£©”£
£Ø3£© A”¢C ×é³ÉµÄŌ×ÓøöŹż±ČĪŖ 1:1 µÄ»ÆŗĻĪļ³£ÓĆÓŚÖʱø C µÄµ„ÖŹ£¬·“Ó¦µÄ»Æѧ·½³ĢŹ½ĪŖ _______ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æĻĀĮŠĖµ·Ø²»ÕżČ·µÄŹĒ£Ø £©
A.ŅŃÖŖ±łµÄČŪ»ÆČČĪŖ6.0kJ”¤mol-1£¬±łÖŠĒā¼ü¼üÄÜĪŖ20kJ”¤mol-1”£¼ŁÉčĆæĦ¶ūĖ®ÖŠÓŠ2molĒā¼ü£¬ĒŅČŪ»ÆČČĶźČ«ÓĆÓŚ“ņĘʱłµÄĒā¼ü£¬Ōņ×ī¶ąÖ»ÄÜĘĘ»µ±łÖŠ15%µÄĒā¼ü
B.ŹµŃé¼ģ²āµĆ»·¼ŗĶé(l)”¢»·¼ŗĻ©(l)ŗĶ±½(l)µÄ±ź×¼Č¼ÉÕČČ·Ö±šĪŖ-3916kJ”¤mol-1”¢-3747kJ”¤mol-1ŗĶ-3265kJ”¤mol-1£¬æÉŅŌÖ¤Ć÷ŌŚ±½·Ö×ÓÖŠ²»“ęŌŚ¶ĄĮ¢µÄĢ¼Ģ¼Ė«¼ü
C.ŅŃÖŖŅ»¶ØĪĀ¶ČĻĀ£¬“×ĖįČÜŅŗµÄĪļÖŹµÄĮæÅضČĪŖc£¬µēĄė¶ČĪŖ¦Į£¬Ka=![]() ”£Čō¼ÓČėÉŁĮæCH3COONa¹ĢĢ壬ŌņµēĄėĘ½ŗāCH3COOHCH3COO-£«H£«Ļņ×óŅĘ¶Æ£¬¦Į¼õŠ”£¬Ka±äŠ”
”£Čō¼ÓČėÉŁĮæCH3COONa¹ĢĢ壬ŌņµēĄėĘ½ŗāCH3COOHCH3COO-£«H£«Ļņ×óŅĘ¶Æ£¬¦Į¼õŠ”£¬Ka±äŠ”
D.”°Ė®”±µē³ŲŹĒŅ»ÖÖÄÜĄūÓƵĖ®Óėŗ£Ė®Ö®¼äŗ¬ŃĪĮæ²ī±š½ųŠŠ·¢µēµÄ×°ÖĆ£¬ŌŚŗ£Ė®ÖŠµē³Ų×Ü·“Ó¦æɱķŹ¾ĪŖ£ŗ5MnO2£«2Ag£«2NaCl=Na2Mn5O10£«2AgCl”£ŌņĆæÉś³É1molNa2Mn5O10×ŖŅĘ2molµē×Ó
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŗ£ŃóÖ²ĪļČēŗ£“ų”¢ŗ£ŌåÖŠŗ¬ÓŠ·įø»µÄµāŌŖĖŲ”£µāŌŖĖŲŅŌµāĄė×ӵĊĪŹ½“ęŌŚ”£ŹµŃéŹŅ“Óŗ£ŌåÖŠĢįČ”µāµÄĮ÷³ĢČēĻĀ£ŗ
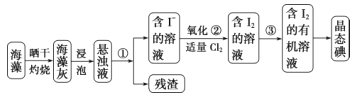
£Ø1£© Öø³ö“Óŗ£ŌåÖŠĢįČ” I2 µÄŹµŃé²Ł×÷Ćū³Ę£ŗ¢Ł _______ £¬¢Ū_______£»Š“³ö¢ŚµÄĄė×Ó·½³ĢŹ½£ŗ______ ”£
£Ø2£© ĢįČ”µāµÄ¹ż³ĢÖŠ£¬æɹ©Ń”ŌńµÄÓŠ»śČܼĮŹĒ________”£
A ¾Ę¾« B ĖÄĀČ»ÆĢ¼ C “×Ėį D øŹÓĶ
£Ø3£© ĪŖŹ¹ŗ£ŌåÖŠ I£×Ŗ»ÆĪŖµāµÄÓŠ»śČÜŅŗ£¬ŹµŃéŹŅĄļÓŠŪįŪö”¢ÉÕ±”¢²£Į§°ō”¢¼ÆĘųĘ攢¾Ę¾«µĘ”¢µ¼¹Ü”¢Ō²µ×ÉÕĘ攢ŹÆĆŽĶųŅŌ¼°±ŲŅŖµÄ¼Š³ÖŅĒĘ÷£¬»¹Č±ÉŁµÄŅĒĘ÷ŹĒ _____ ”£
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æ»ÆѧÓėČĖĄąÉś²ś”¢Éś»ī”¢»·¾³µČĆÜĒŠĻą¹Ų£¬ĻĀĮŠĖµ·ØÕżČ·µÄŹĒ![]()
A.ÓĆ¼ÓĆøĻ“ŅĀ·ŪĻ“ŅĀ·žŹ±Ė®µÄĪĀ¶ČŌ½øßŌ½ŗĆ
B.”°¹ā»ÆѧŃĢĪķ”±”¢”°ĻõĖįŠĶĖįÓź”±µÄŠĪ³É¶¼ÓėµŖŃõ»ÆĪļÓŠ¹Ų
C.Š”ĖÕ“ņŹĒÖĘ×÷ĀųĶ·µÄÅņĖɼĮ£¬ĖÕ“ņŹĒÖĪĮĘĪøĖį¹ż¶ąµÄæ¹Ėį¼Į
D.ŅŅ“¼”¢¹żŃõ»ÆĒā”¢“ĪĀČĖįÄʵČĻū¶¾ŅŗµÄĻū¶¾ŌĄķ¶¼ŹĒĄūÓĆĘäĒæŃõ»ÆŠŌ
²éæ““š°øŗĶ½āĪö>>
æĘÄæ£ŗøßÖŠ»Æѧ Ą“Ō“£ŗ ĢāŠĶ£ŗ
”¾ĢāÄæ”æŠæʬŗĶ“æĶʬ°“Ķ¼Ź¾·½Ź½²åČėĶ¬ÅØ¶ČµÄĻ”ĮņĖįÖŠŅ»¶ĪŹ±¼ä£¬ŅŌĻĀŠšŹöÕżČ·µÄŹĒ

A.Į½ÉÕ±ÖŠĶʬ±ķĆę¾łĪŽĘųÅŻ²śÉś
B.¼×ÖŠĶʬŹĒÕż¼«£¬ŅŅÖŠĶʬŹĒøŗ¼«
C.²śÉśĘųÅŻµÄĖŁ¶Č¼×±ČŅŅĀż
D.Į½ÉÕ±ÖŠČÜŅŗµÄ H£«µÄÅØ¶Č¾ł¼õŠ”
²éæ““š°øŗĶ½āĪö>>
°Ł¶ČÖĀŠÅ - Į·Ļ°²įĮŠ±ķ - ŹŌĢāĮŠ±ķ
ŗž±±Ź”»„ĮŖĶųĪ„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±ØĘ½ĢØ | ĶųÉĻÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | µēŠÅÕ©Ę¾Ł±Ø×ØĒų | É꥜Ź·ŠéĪŽÖ÷ŅåÓŠŗ¦ŠÅĻ¢¾Ł±Ø×ØĒų | ÉęĘóĒÖČؾŁ±Ø×ØĒų
Ī„·ØŗĶ²»Į¼ŠÅĻ¢¾Ł±Øµē»°£ŗ027-86699610 ¾Ł±ØÓŹĻä£ŗ58377363@163.com