
| A.0.01mol/L CH3COOH | B.0.01mol/L HNO3 |
| C.pH=2的H2SO4溶液 | D.pH=2的CH3COOH溶液 |
科目:高中化学 来源:不详 题型:填空题
查看答案和解析>>
科目:高中化学 来源:不详 题型:实验题
| 实验编号 | 待测NaOH溶液的体积/mL | HCl溶液的体积/mL |
| 1 | 25.00 | 24.41 |
| 2 | 25.00 | 24.39 |
| 3 | 25.00 | 22.60 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.原HA溶液中,c(H+)=c(OH-)+c(A-) |
| B.当滴入少量的NaOH溶液时,促进了HA的电离,溶液的pH降低 |
| C.当恰好完全中和时,溶液呈中性 |
| D.当NaOH溶液过量时,可能出现:c(A-)>c(Na+)>c(OH-)>c(H+) |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.常温下,0.01mol·L-1醋酸溶液pH=2 |
| B.95℃纯水的pH<7,说明加热可导致水呈酸性 |
| C.常温下,将pH=3的醋酸溶液稀释至10倍后溶液pH=4 |
| D.常温下,将0.2 mol·L-1的盐酸与等体积水混合后溶液pH=1 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
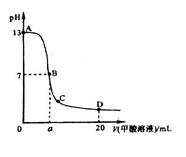
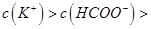
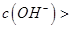
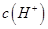
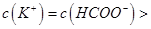
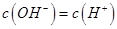 ,且a=7.5
,且a=7.5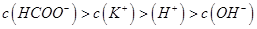
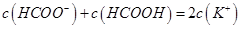
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
| A.①⑤ | B.③④ | C.②⑤ | D.②④ |
查看答案和解析>>
科目:高中化学 来源:不详 题型:单选题
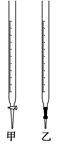
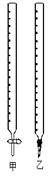
| 选项 | 锥形瓶中溶液 | 滴定管中溶液 | 选用指示剂 | 选用滴定管 |
| A | 碱 | 酸 | 石蕊 | 甲 |
| B | 酸 | 碱 | 酚酞 | 甲 |
| C | 碱 | 酸 | 甲基橙 | 乙 |
| D | 酸 | 碱 | 酚酞 | 乙 |
查看答案和解析>>
科目:高中化学 来源:不详 题型:填空题
| 温度 / ℃ | 25 | t1 | t2 |
| 水的离子积常数 | 1×10-14 | α | 1×10-12 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com