
运用下列装置和操作能达到实验目的和要求的是( )
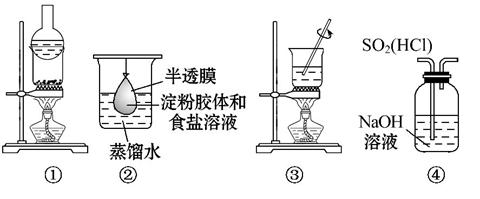
A.用①分离氯化铵和单质碘
B.用②除去淀粉溶液中的氯化钠
C.用③加热胆矾(CuSO4·5H2O)制取无水硫酸铜
D.用④装置除去SO2中的HCl
 阅读快车系列答案
阅读快车系列答案科目:高中化学 来源: 题型:
根据如图描述,完成下列问题:
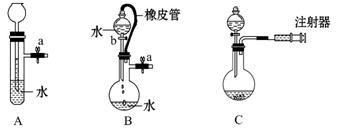
(1)关闭图A装置中的止水夹a,从长颈漏斗向试管中加入一定量的水,静止后如图,判断A装置是否漏气 (填“漏气”“不漏气”或“无法确定”),理由是_______________________________________________________________。
(2)关闭B装置中的止水夹a后,开启活塞b,水不断往下流,至全部流入烧瓶,判断B装置是否漏气 (填“漏气”“不漏气”或“无法确定”),理由是__________________________________________________________________。
(3)用简单的方法检验C装置的气密性__________________________________。
查看答案和解析>>
科目:高中化学 来源: 题型:
我国湘黔渝三地交界地区是中国电解锰企业最集中的地区,被称为中国的“锰三角”。金属锰的熔点很高,常用铝热法制得粗锰,再用电解法制得纯的金属锰。铝被用于冶炼金属锰,是因为铝 ( )
A.熔点低
B.具有还原性
C.具有两性
D.冶炼反应中放出大量的热
查看答案和解析>>
科目:高中化学 来源: 题型:
Al2O3、Al(OH)3都是重要化工原料。根据要求回答问题:
Ⅰ、电解法制高品质Al(OH)3装置如右(中间用离子交换膜隔开):
 4Na[Al(OH)4]+2H2O 4Al(OH)3↓+4NaOH+O2↑+2H2↑
4Na[Al(OH)4]+2H2O 4Al(OH)3↓+4NaOH+O2↑+2H2↑
(1)产物Al(OH)3在 区(填“阴极”或“阳极”)沉积;
(2)电解中转移2mol e—时,将制得__________mol的Al(OH)3。
Ⅱ、制取纳米Al2O3需要纯净的硫酸铝。现有0.05mol·L-1硫酸铝溶液,经检测,含有Fe2+、Fe3+。可按下述操作提纯:往溶液中加足量H2O2充分反应,再用试剂X调节溶液pH=3.5。(室温下,0.1mol·L-1的Fe2+、Al3+开始沉淀的pH分别为7.0和3.7,Fe3+完全沉淀的pH=3.2)
(3)纳米氧化铝分散在分散剂中将形成胶体。则纳米氧化铝的直径约为 m。
(4)检验硫酸铝溶液含有Fe3+时,所采用的试剂及现象是 。
(5)往溶液中加入H2O2的作用是 (用离子方程式表示)。
(6)加入的X试剂(填选项编号)是 。
A.CuO B.Al(OH)3 C.NaOH D.NaHCO3
若调节后溶液的pH偏离3.5,可能带来的后果是
。
查看答案和解析>>
科目:高中化学 来源: 题型:
下列各组溶液中,用括号内的试剂及物质间相互反应不能鉴别的一组
是( )
A.Ba(OH)2、KSCN、NaCl、Mg(NO3)2(FeCl3溶液)
B.NaNO3、NaHCO3、(NH4)2SO3、Na2SiO3(H2SO4溶液)
C.NH4Br、K2CO3、NaI、CaCl2(AgNO3溶液)
D.(NH4)3PO4、NaBr、CuSO4、AlCl3(KOH溶液)
查看答案和解析>>
科目:高中化学 来源: 题型:
实验室制氯气有如下几步操作:
①在烧瓶内装入MnO2粉末;②塞好带导管和分液漏斗的双孔塞;③由分液漏斗向烧瓶中注入浓盐酸;④用铁夹固定圆底烧瓶;⑤检查气密性;⑥放好酒精灯;⑦点燃酒精灯;⑧放好铁圈和石棉网,正确的操作顺序是( )
A.①②③④⑧⑤⑥⑦
B.⑤①②③⑧④⑥⑦
C.⑤⑥⑧①②③④⑦
D.⑥⑧⑤①②④③⑦
查看答案和解析>>
科目:高中化学 来源: 题型:
下列实验方案不能达到实验目的的是( )
| 实验目的 | 实验方案 | |
| A | 证明溴乙烷发生消去反应有乙烯生成 | 向试管中加入适量的溴乙烷和NaOH的乙醇溶液,加热,将反应产生的气体通入溴的四氯化碳溶液 |
| B | 证明Mg(OH)2沉淀可以转化为Fe(OH)3沉淀 | 向2 mL 1 mol·L-1NaOH溶液中先加入3滴1 mol·L-1MgCl2溶液,再加入3滴 1 mol·L-1FeCl3溶液 |
| C | 检验蔗糖水解产物具有还原性 | 向蔗糖溶液中加入几滴稀硫酸,水浴加热几分钟,然后加入足量稀NaOH溶液,再向其中加入新制的银氨溶液,并水浴加热 |
| D | 探究温度对化学平衡的影响 | 将NO2球浸泡在冷、热水中,观察颜色的变化 |
查看答案和解析>>
科目:高中化学 来源: 题型:
已知A(g)+B(g)  C(g)+D(g)反应的平衡常数和温度的关系如下:
C(g)+D(g)反应的平衡常数和温度的关系如下:
| 温度/℃ | 700 | 800 | 830 | 1 000 | 1 200 |
| 平衡常数 | 1.7 | 1.1 | 1.0 | 0.6 | 0.4 |
请回答下列问题:
(1)该反应平衡常数表达式为K=________;ΔH________0(填“>”“<”或“=”)。
(2)830 ℃时,向一个5 L的密闭 容器中充入0.20 mol的A和0.80 mol的B,若测得反应初始至6 s内A的平衡反应速率v(A)=0.003 mol·L-1·s-1,则6 s时c(A)=________mol·L-1;C的物质的量为________mol。
(3)在与(2)相同的温度、容器及A、B配比下反应经一段时间后达到平衡,此时A的转化率为________;如果这时向该密闭容器中再充入1mol氩气,则平衡时A的转化率________(填“增大”“减小”或“不变”)。
(4)判断该反应是否达到平衡的依据为________(填正确选项的字母)。
A.压强不随时间改变
B.气体的密度不随时间改变
C.c(A)不随时间改变
D.单位时间里生成C和D的物质的量相等
(5)1 200 ℃时反应C(g)+D(g)  A(g)+B(g)的平衡常数的值为________。
A(g)+B(g)的平衡常数的值为________。
查看答案和解析>>
科目:高中化学 来源: 题型:
“绿色化学”的核心理念是:原子经济性原则。即力求反应物分子中的所有原子全都转化到目标产物中,理想状态的原子利用率为100%。在合成1,2—二溴乙烷时,原子利用率最高的途径是
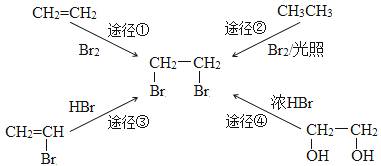
A.途径① B.途径② C.途径③ D.途径④
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com