


 智趣寒假作业云南科技出版社系列答案
智趣寒假作业云南科技出版社系列答案科目:高中化学 来源: 题型:
| A、2NaBr+Cl2═2NaCl+Br2 | ||||
B、2KMnO4
| ||||
| C、2H2S+SO2═3S↓+2H2O | ||||
| D、2FeCl3+H2S═2FeCl2+S↓+2HCl |
查看答案和解析>>
科目:高中化学 来源: 题型:
| A、c(Na+)=2c(R2-)+c(HR-) |
| B、c(Na+)=10-2mol/L |
| C、c(R2-)+c(OH-)+c(HR-)=C(Na+)+C(H+) |
| D、c(R2-)>c(Na+)>c(H+)>c(OH-) |
查看答案和解析>>
科目:高中化学 来源: 题型:
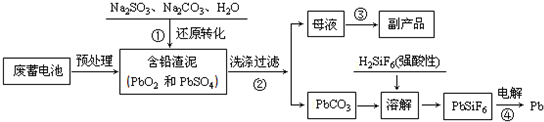

| 离子 | Pb2+ | Ca2+ | Fe3+ | Mn2+ | Cl- |
| 处理前浓度/(mg?L-1) | 0.100 | 29.8 | 0.120 | 0.087 | 51.9 |
| 处理后浓度/(mg?L-1) | 0.004 | 22.6 | 0.040 | 0.053 | 49.8 |
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:
查看答案和解析>>
科目:高中化学 来源: 题型:

查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com