

 .
.分析 由元素在周期表中的位置可知,①为H,②为C,③为N,④为O,⑤为Na,⑥为Al,⑦为Si,⑧为S,⑨为Cl.
(1)②为C元素,其中子数为8的核素的质量数为14,其氢化物甲为14CH4;
(2)所有元素中H原子半径最小,同主族自上而下原子半径增大,同周期自左而右原子半径减小;非金属性越强,最高价氧化物对应的水化物酸性越强;
(3)②的单质为C,③的最高价氧化物对应水化物的浓溶液为浓硝酸,碳与浓硝酸在加热条件下反应生成二氧化碳、二氧化氮和水;
(4)元素④、⑤组成X,元素②、④形成Y,X与Y的反应是潜水艇和呼吸面具中氧气的来源,则X为Na2O2,Y为CO2;
(5)根据装置腿可知,利用强酸制备弱酸判断元素非金属性,A中产生二氧化碳,B除去二氧化碳中HCl气体,C中是二氧化碳与硅酸钠反应生成硅酸与碳酸氢钠.
解答 解:由元素在周期表中的位置可知,①为H,②为C,③为N,④为O,⑤为Na,⑥为Al,⑦为Si,⑧为S,⑨为Cl.
(1)②为C元素,其中子数为8的核素的质量数为14,其氢化物为甲为14CH4,摩尔质量为18g/mol,故答案为:18g/mol;
(2)所有元素中H原子半径最小,同主族自上而下原子半径增大,同周期自左而右原子半径减小,故原子半径:Na>Al>C>H;由于非金属性:Cl>S>Si,则酸性大小为:HClO4>H2SO4>H2SiO3,
故答案为:Na>Al>C>H; HClO4>H2SO4>H2SiO3;
(3)②的单质为C,③的最高价氧化物对应水化物的浓溶液为浓硝酸,二者在加热条件下反应生成二氧化碳、二氧化氮和水,反应的化学方程式为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O,
故答案为:C+4HNO3(浓)$\frac{\underline{\;\;△\;\;}}{\;}$CO2↑+4NO2↑+2H2O;
(4)元素④、⑤组成X,元素②、④形成Y,X与Y的反应是潜水艇和呼吸面具中氧气的来源,则X为Na2O2,Y为CO2,二氧化碳分子中含有共价键,过氧化钠电子式为 ,
,
故答案为:共价键; ;
;
(5)根据装置腿可知,利用强酸制备弱酸判断元素非金属性,A中产生二氧化碳,B除去二氧化碳中HCl气体,C中是二氧化碳与硅酸钠反应生成硅酸与碳酸氢钠,反应方程式为:SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3-,
故答案为:强酸制弱酸;除去CO2中的 HCl气体;SiO32-+2CO2+2H2O═H2SiO3↓+2HCO3-.
点评 本题考查了元素周期律和元素周期律的综合应用、性质实验方案的设计等,题目难度中等,熟练掌握元素周期表结构与元素周期律,注意掌握金属性、非金属性强弱比较实验事实.


 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案科目:高中化学 来源: 题型:解答题
 如图是元素周期表中各主族(A)及零族的部分元素符号代码(阴影处为族序数)
如图是元素周期表中各主族(A)及零族的部分元素符号代码(阴影处为族序数)查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | ①②③⑤ | B. | ①②③⑤⑥⑦ | C. | ①②④⑤ | D. | 全部 |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 青苹果只含淀粉不含糖类 | B. | 熟苹果中只含葡萄糖不含淀粉 | ||
| C. | 苹果转熟时葡萄糖合成淀粉 | D. | 苹果转熟时淀粉水解为葡萄糖 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
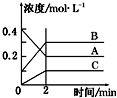
| A. | A是反应物 | |
| B. | 前2 min A的分解速率为0.1 mol•L-1•min-1 | |
| C. | 达平衡后,若升高温度,平衡向正反应方向移动 | |
| D. | 反应的方程式为:2A(g)?2B(g)+C(g) |
查看答案和解析>>
科目:高中化学 来源: 题型:解答题
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
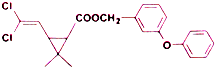
| A. | 分子式为C21H20O3Cl2 | |
| B. | 醚键上的氧原子至少与另外11个原子共面 | |
| C. | 分子中不存在手性碳原子 | |
| D. | 在一定条件下可发生加成、取代、氧化反应 |
查看答案和解析>>
科目:高中化学 来源: 题型:选择题
| A. | 1mol•L-1 NaOH溶液 | B. | 2 mol•L-1HCl溶液 | ||
| C. | 3 mol•L-1 NaCl溶液 | D. | 酒精 |
查看答案和解析>>
湖北省互联网违法和不良信息举报平台 | 网上有害信息举报专区 | 电信诈骗举报专区 | 涉历史虚无主义有害信息举报专区 | 涉企侵权举报专区
违法和不良信息举报电话:027-86699610 举报邮箱:58377363@163.com